
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Железо и его соединения
Железо является вторым после алюминия металлом по распространенности в природе. Характерные степени окисления железа, электронные формулы соответствующих ионов, химические свойства и примеры соединений приведены в таблице.
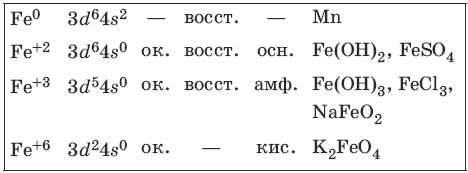
Соединения железа (+8) малохарактерны.
Получение и свойства железа
3Fe2O3 + CO → t → 2Fe3O4 + CO2
Fe3O4 + CO → t → 3FeO + CO2
FeO + CO → t → Fe + CO2
3Fe3O4 + 8Al → t → 9Fe + 4Al2O3
Fe + I2 → t → FeI2
2Fe + ЗCl2 → t → 2FeCl3
4Fe + 3O2 + 2Н2O = 4FeO(OH)↓ (коррозия на воздухе)
Fe + 2HCl = FeCl2 + Н2
Fe + H2SO4 (разб.) = FeSO4 + H2
Fe + 4HNO3 (разб.) = Fe(NO3)3 + NO + 2H2O
Концентрированные серная и азотная кислоты пассивируют железо на холоду. При нагревании реакция идет.
2Fe + 6H2SO4(конц.) → t → Fe2(SO4)3 + 3SO2 + 6Н2O
Fe + 6НNO3(конц.) → t → Fe(NO3)3 + 3NO2 + 3H2O
Свойства соединений железа (+2)
FeO + Н2O ≠
FeO + H2SO4 = FeSO4 + H2O
FeSO4 + 2NaOH = Fe(OH)2↓ + Na2SO4
Гидроксид железа(II) сразу окисляется кислородом воздуха.
4Fe(OH)2↓ + 2Н2O + O2 = 4Fe(OH)3↓
Fe(OH)2↓ + H2SO4 = FeSO4 + 2Н2O
Fe(OH)2↓ + 2NaOH *
FeSO4 + 6KCN = K4[Fe(CN)6] + K2SO4
FeSO4 + K3[Fe(CN)6] = KFe[Fe(CN)6]↓ + K2SO4
Свойства соединений железа (+3)
FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
Fe(OH)3↓ + 3HCl = FeCl3 + 3H2O
Fe(OH)3↓ + NaOH ≠ не идет в разбавленном растворе
Fe(OH)3↓ + NaOH → сплавление → NaFeO2 + 2H2O
FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl
FeCl3 + 6KCN = K3[Fe(CN)6] + 3KCl
FeCl3 + K4[Fe(CN)6] = KFe[Fe(CN)6]↓ + 3KCl
FeCl3 + 3KCNS = Fe(SCN)3 + 3KCl
Свойства соединений железа (+6)
Феррат калия – окислитель.
Fe2O3 + 3KNO3 + 4KOH → сплавление → 2K2FeO4 + 3KNO2 + 2H2O
4K2FeO4 + 10H2SO4(разб.) = 2Fe2(SO4)3 + 3O2↑ + 4K2SO4 + 10H2O
Не нашли, что искали? Воспользуйтесь поиском: