
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Учебный год. Задания для 11 класса (Решения)
Учебный год. Задания для 11 класса.
Задача 1.
Студентка I курса Химического института им. A.M. Бутлерова Казанского государственного университета Антонина Позднякова получила по почте конверт с таинственным зеленым порошком. Она не стала пробовать его на вкус, а отнесла в лабораторию на анализ. При растворении навески порошка массой 5,54 г в избытке дистиллированной воды не растворилось 2,22 г зеленого вещества. Полученный раствор был отделен от зеленого осадка фильтрованием (фильтрат А ). Фильтрат А представляет собой бесцветный раствор. При его выпаривании из раствора выделяются бесцветные кристаллы, окрашивающие бесцветное пламя газовой горелки в фиолетовый цвет.
Еще одна порция фильтрата А, также полученная из 5,54 г зеленого порошка, была обработана раствором нитрата свинца(II). В результате этого выпал желтый осадок В массой 4,61 г. Помещение этого осадка в горячую воду приводит к его частичному растворению. Резкое охлаждение полученного раствора приводит к повторному осаждению осадка В в виде красивых золотистых чешуек.
В ходе дальнейших экспериментов над фильтратом А стало ясно, что он образует осадки при обработке нитратом серебра (желтый осадок С), хлорной кислотой (белый осадок D)), гексанитрокобальтатом(III) натрия (желтый осадок Е).
Прокаливание исходного зеленого порошка приводит к образованию бесцветного газа F, не имеющего запаха и бесцветной жидкости G. Газ F вызывает помутнение известковой воды; газ, выделяющийся при прокаливании 5,54 г исходного зеленого порошка, при пропускании через баритовую воду даст 1,97 г осадка. Эта же масса исходного порошка выделит 0,18 г жидкости Си 1,6 г черного твердого вещества Н. Восстановление обозначенного выше количества вещества Н водородом приводит к образованию 1,28 г красного простого вещества I.
?1. Определите веществам A-I. Запишите уравнения упомянутых в задаче реакций.
?2. Используя численные данные, приведенные в условии задачи, определите количественный и качественный состав таинственного зеленого порошка.
?3. Что могло произойти, если бы Антонина решила попробовать таинственный зеленый порошок на вкус?
Задача 2.
Вещество А широко использовалось в СССР в качестве болеутоляющего. Его промышленное получение было основано на следующей схеме:
Б + NaOH à В+ Н2О (реакция протекает при 150-160° С)
В + СО2 à Г (реакция протекает при 110-150° С и давлении 5-6 атмосфер)
Г (раствор) + H2S04 à Д + Na2S04
Д + (СН3СО)2О à А
Известно, что вещество Б можно получить несколькими способами. Один из них основан на щелочном гидролизе хлорбензола. Интересен тот факт, что для получения тринитропроизводного вещества Б его раствор в бензоле необходимо сначала обработать диоксидом азота на холоду, а затем реакционную смесь обрабатывают нитрующей смесью, в качестве основного продукта этой реакции получают темно-зеленую маловзрывчатую жидкость Е. В разное время вещества Б и Д называли кислотами, но только Д является карбоновой кислотой.
?1. Приведите структурные формулы и названия веществ А, Б, В, Г, Д.
?2. Запишите уравнения или схемы всех упомянутых в условии задачи реакций.
Задача 3.
Расшифруйте цепочку превращений:

Дополнительно известно, что А встречается в природе в основном в виде простого вещества
и обладает следующими характеристиками:
радиус атома = 0.144 нм; Тпл = 1063°С; Ткип = 2880°С.
Древневавилонское название вещества А - hurasu (хуре-шу).
?1. Приведите формулы веществ А -I и назовите их.
?2. Запишите все уравнения реакций.
Задача 4.
Как известно, оптическую активность могут проявлять вещества, содержащие ассиметричный (т.е. имеющий 4 разных заместителя) атом углерода. Но это правило не всегда верно. Критерием для проявления оптической активности является отсутствие плоскости симметрии.
Вам даны десять веществ. Вы должны будете сделать вывод о наличии у них оптической активности.
1. Транс-дихлорэтан. 2. СН3СНС1Вr 3. СН2ВrСН2Вr 4. D-глюкоза



10. метилэтиламин
Задача 5.
В энзимологии существует понятие об активном центре фермента - фрагменте структуры белка-катализатора, осуществляющего связывание молекулы органического соединения-субстрата на цепи фермента и подготовку субстрата к реакции. Образование комплекса фермент—субстрат при этом происходит с участием всех известным межмолекулярных взаимодействий.
Одной из стадий гликолиза является превращение 2-фосфоглицериновой кислоты в фосфое-нолпировиноградную кислоту, протекающее по схеме:
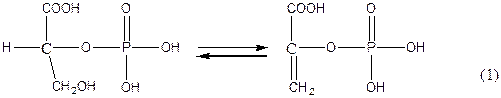
Это превращение катализируется ферментом енолазой. Известно, что енолаза работает без участия кофакторов и образования промежуточных продуктов.
? 1. Предложите гипотетическую схему активного центра енолазы (типы группировок, отвечающих за связывание субстрата и их ориентация относительно него).
? 2. Какие аминокислотные остатки могут принимать участие в образовании предложенного Вами активного центра?
Активность фермента может быть выражена двумя способами: молярная активность фермента (измеряется в каталах на моль [кат/моль]) и удельная активность фермента. Один катал фермента соответствует количеству фермента (в молях), способному вызвать превращение 1 моля субстрата в продукт в течение 1 секунды. Удельная активность фермента представляет собой число каталов на 1 килограмм активного белка.
?З.Одна молекула каталазы, содержащейся в эритроцитах, в течение 1 минуты способна расщепить 5·106 молекул перекиси водорода. Определите молярную активность каталазы. Фермент панкреатическая рибонуклеаза может быть выделен из желудочных клеток млекопитающих. При этом молярная активность панкреатической рибонуклеазы практически не зависит от организма, из которого она получена. Удельная же активность панкреатической рибонуклеазы различается в зависимости от типа организма, из которого выделялся препарат фермента.
? 4. В двух-трех фразах объясните причины равенства молярной и неравенства удельной активности фермента.
XLIII республиканская олимпиада школьников по химии
учебный год. Задания для 11 класса (Решения)
Не нашли, что искали? Воспользуйтесь поиском: