
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Подведение итогов и оценка результатов
Преподаватель проводит анализ проделанной работы, отмечает положительные и отрицательные стороны проделанной работы.
Итогом теоретического занятия является оценка по пятибалльной системе с учетом работы студента, записей в тетради, а также выполнения теста.
Заключение
Теоретические занятия, проводимые с использованием новых компьютерных технологий и аппаратуры, позволяет обобщить материал, сделать его более наглядным, доступным широкой аудитории.
Данный материал может быть использован для самоподготовки студентов по изложенной теме, т.к. изложен в электронном виде.
4.Литература
1. Габриелян О.С. Химия: учеб. для студ. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов. - М., 2007
2. Габриелян О.С., Остроумов И.Г. Химия: Пособие для поступающих вузы. - М., 2010
3. Ерохин Ю.М. Химия. - М., 2008
- Рудзитис Г. Е., Фельдман Ф. Г., Химия 11, М., Просвещение, 1989
- Семёнов И. Н., Химия, пособие для поступающих в ВУЗ. Л., ЛГУ, 1996
- Хомченко Г. П., Цитович И. К., Неорганическая химия, М., Высшая Школа, 1998
- Хомченко И.Г. Общая химия: Учебник. – М.: ООО «Издательство Новая волна», 1997. – 464 с.
- Химия, справочные материалы, под ред. Третьякова Ю. Д., М., Просвещение, 1999
5. Приложение 1






































Приложение 2
Выберите один правильный вариант ответа
1.Образует щелочь при взаимодействии с водой
а)СuO
б)K2O
в)Fe2O3
г)ZnO
2.При взаимодействии натрия с водой образуется:
а) Водород и оксид натрия
б)Кислород и оксид натрия
в)Гидроксид натрия и водород
г) Гидроксид натрия и кислород
3. Соляная кислота при обычных условиях взаимодействует с
а) ртутью
б) медью
в) магнием
г) серебром
4. Каким веществом надо подействовать на хлорид цинка ZnCl2, чтобы получить гидроксид цинка Zn(OH)2:
а) H2O
б) HCl
в) Fe(OH)2
г) КОН
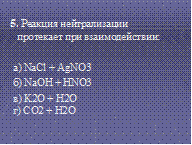
5.Реакция нейтрализации протекает при взаимодействии:
а) NaCl + AgNO3
б) NaOH + HNO3
в) K2O + H2O
г) CO2 + H2O
6. Хлорид бария BaCl2 взаимодействует с:
а) HNO3
б) H2SO4
в) HCl
г) H2О
7. Может вытеснить цинк из раствора его соли:
а) Fe
б) Cu
в) Al
г) Na
8.Реакция обмена протекает до конца между:
а) хлоридом бария и нитратом натрия
б) нитратом цинка и сульфатом калия
в) карбонатом натрия и хлоридом кальция
г) нитратом бария и хлоридом натрия
9. Водород выделяется при взаимодействии:
а) Cu + HNO3
б) Zn + H2SO4
в) Ag + HCl
г) Hg + H3PO4
10. Гидроксид натрия при обычных условиях взаимодействует с
а) оксидом углерода (IV)
б) оксидом кальция
в) медью
г) водой
Приложение 3
Алгоритм «Составление формулы соли, кислоты, основания»
Задание: Составить формулу сульфата алюминия
| № п/п | Последовательность действий | Выполнение действий |
| 1. | Для составления формул солей, кислот и оснований необходимо воспользоваться таблицей растворимости солей. На первом месте необходимо поставить формулу катиона. На втором месте формулу аниона. | Al3+ SO42- |
| 2. | Молекула соли, кислоты или основания должна быть электронейтральным соединением. Поэтому число положительных зарядов в молекуле должно быть равно числу отрицательных зарядов. С этой целью определить наименьшие целые корни в уравнении: x·3=y·2, где х и y - минимальные целые корни уравнения, а 3 и 2 абсолютные значения заряда катиона и аниона. | 3·2=2·3 |
| 3. | Подставить определенные индексы в формулу сульфата алюминия | Аl2(SO4)3 |
| 4. | Проверить правильность составления формулы, сравнивая количество отрицательных и положительных зарядов в молекуле |
Приложение 4
Классификация неорганических веществ
Простые
· Металлы (Ca, Na)
· Неметаллы(P, N2, O2)
Сложные
· Оксиды
ü Солеобразующие
o Основные(CaO, Na2O)
o Амфотерные(AI2O3, ZnO)
o Кислотные(SO3)
ü Несолеобразующие (NO, N2O)
· Кислоты
o Одноосновные(HCI)
o Двухосновные(H2SO4)
o Трехосновные(H3PO4)
o Четырехосновные (H4P2O7)
· Гидроксиды
o Основные (основания – NaOH)
o Амфотерные(AI(OH)3)
o Нерастворимые(Cu(OH)2)
· Соли
o Средние (нормальные): Na2CO3
o Кислые(NAHCO3)
o Основные(MqOHCI)
o Двойные(KAI(SO4))
o Смешанные(HqBrI)
Название солей
| Название | формула | Название кислотного остатка | Пример |
| Азотная кислота | HNO3 | NO3 - нитрат | Na NO3 |
| Азотистая | HNO2 | NO2 -нитрит | Na NO2 |
| Соляная | HCI | CI - хлорид | NaCI |
| Серная | H2SO4 | SO4 - сульфат | Na2SO4 |
| Сернистая | H2SO3 | SO3 - сульфит | Na2SO3 |
| Сероводородная | H2S | S - сульфид | Na2S |
| Угольная | H2СO3 | СO3 - Карбонат | Na2СO3 |
| Кремниевая | H2SiO3 | SiO3 -силикат | Na2 SiO3 |
| Фосфорная | H3PO4 | PO4 фосфат | Na3 PO4 |
| Борная | H3BO3 | BO3 - борат | Na3 BO3 |
РЕЦЕНЗИЯ
На методическую разработку урока «Основные классы неорганических соединений»
Автор: Степанова Н.В., преподаватель ГАОУ СПО «Сортавальский колледж»
Представленная разработка имеет краткую аннотацию, оглавление, введение, основную часть, включающую план урока, заключение, литературу и приложение.
В краткой аннотации показано предназначение данной разработки. Во введении автором отмечено значение данной темы для подготовки будущих ветеринарных специалистов, подчеркнуто наиболее яркое достоинство данной разработки: большое количество наглядного материала, представленного средствами компьютерных технологий.
В основной части разработки представлен непосредственно план урока. План составлен в соответствии с основными требованиями к его составлению, включает в себя все необходимые элементы. Структура плана достаточно четкая.
Содержание соответствует теме занятия. Изложение материала сопровождается красочными иллюстрациями презентации. Это обогащает материал и облегчает его восприятие.
Предлагаемая разработка урока интересна своей динамичностью, широтой охвата материала.
Данная методическая разработка, действительно, может быть использована в работе преподавателей химических дисциплин, так как позволяет организовать успешное проведение занятия, нацеленного на закрепление студентами глубоких теоретических знаний об основных классах неорганических соединений
Таким образом, предлагаемая методическая разработка урока «Основные классы неорганических соединений» по дисциплине «Химия» может быть рекомендована к использованию в данном образовательном учреждении.
Рецензент: Крылова Н.Б., председатель
предметной комиссии
зооветеринарных дисциплин
20.10.2012.
Не нашли, что искали? Воспользуйтесь поиском: