
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Кольцевые соединения
Вторая основная группа органических соединений – кольцевые соединения. И вновь, кольцевые структуры делятся на три подгруппы. В двух из них положительными компонентами магнитно-нейтральных групп являются атомы углерода. Первая подгруппа – это циклические или алициклические соединения, у которых преимущественная валентность углерода равна 2. Вторая подгруппа – это ароматические соединения, у которой валентность углерода равна 1. У третьей подгруппы - гетероциклические соединения - один или больше атомов углерода в кольце заменяется атомом какого-то другого элемента. Эти три подгруппы подразделяются еще на мононуклеарные и полинуклеарные подразделения; базовая структура последних формируется посредством уплотнения (сгущения) или слияния двух или более колец. Следует понять, что подразделения не исключают друг друга. Соединение может состоять из кольца, присоединенного к одной или более цепей; цепное соединение может обладать одной парафиновой и одной олефиновой ветвью; циклическое кольцо может присоединяться к ароматическому кольцу, и так далее.
Как и у цепных соединений, классификация делит кольцевые соединения на семейства, характеризующиеся природой отрицательных компонентов, - углеводороды, спирты, амины и так далее. Обыкновенный циклический углеводород циклан или циклопарафин – это простое кольцо нейтральных групп CH2. Общую формулу можно выразить как -(CH2)n. Начиная с циклопропана (n= 3), обыкновенные цикланы создаются всеми величинами n, вплоть до более 30. У колец нейтральные группы идентичны нейтральным группам CH2 у цепных соединений и могут расширяться тем же способом – прибавлениями CH2. Следовательно, разветвленным цепным соединениям соответствуют разветвленные кольца, такие как этилциклогексан -(CH2)5 (CH • CH2 • CH3)- и 1-метил-2-этил циклопентан -CHCH3 • (CH • CH2 • CH3) • (CH2)3.
В последующих обозначениях нейтральные группы будут четко определены скобками или другими средствами, и (как и в нейтральных группах цепных соединений) внутри групп будет сохраняться положительно-отрицательных порядок. Чтобы определить вещество как кольцевое соединение и показать, что конечные положения в прямой строке формулы не имеют такой особой значимости, как в цепных соединениях, на каждом конце кольцевой формулы будет использоваться тире, как в вышеприведенных примерах. Если имеются два или более кольца или если часть соединения находится вне кольца, на это будут указывать положения тире. Поскольку при выражении формулы единичного кольца ни одна группа не может считаться стартовой точкой, по возможности, мы будем следовать порядку обычной системы нумерации, чтобы снизить до минимума отклонения от известной практики. То есть, названия ветвей, например, 1-метил-2этил, будут ясно указываться формулой.
У циклического кольца замещение всех двухвалентных групп одновалентными группами там, где замещение реально, преобразовывает циклическое соединение в ароматическое. Однако отдельные ароматические характеристики не появляются до тех пор, пока не завершится замещение. Поэтому в циклическую классификацию будут включены промежуточные структуры, у которых CH или ее эквивалент замещены на CH2 только в части кольцевых положений. Поскольку присутствие оставшихся групп CH2 является главным определителем молекулярных свойств, превалирующей валентностью углерода, в том смысле, в каком этот термин используется для определения классов кольцевых соединений, будет 2, даже если в молекуле имеется больше групп СН, чем CH2.
Как уже упоминалось, в молекулярных соединениях вероятности благоприятствуют объединению подобных сил. Группы CH2 обладают достаточной гибкостью геометрической компоновки для компенсации существенных вариаций. Следовательно, единичные группы CH2 могут без труда увязываться с молекулярной структурой. Группы СН обладают небольшим геометрическим дрейфом, и поэтому они почти всегда существуют в парах. Это не значит, что индивидуальная группа не может существовать отдельно, и в некоторых более сложных структурах можно обнаружить единичные группы СН. Но у простых колец пары настолько вероятнее, чем нечетные количества групп, что последние исключаются.
Первое двухгрупповое замещение в цикланах создает циклены или циклоолефины. Типичное соединение - циклогексан -(CH2)4 • (CH)2. Исходя из выводов этой работы, производные циклопарафина и циклоолефина невозможны, поскольку циклопарафины не содержат атомов углерода с характеристиками валентности парафина. Циклоолефины формируются замещением двухвалентных групп ацетилена на кольца CH2. Поэтому предпочтительнее названия циклан и циклен.
Замещение еще двух групп СН в кольце создает циклодиены. Существование двух пар CH • CH в этих соединениях вносит новый фактор - положения пар внутри кольца могут меняться. В связи с циклопентадиеном (CH)Q•CH2 - первым соединением в этих сериях - вопроса не возникает, но у циклогексадиена возможны две разные компоновки: -(CH)4• (CH2)2, известная как 1,3-циклогексадиен, и -(CH)2 • CH2 • (CH)2 • CH2, являющаяся 1,4-циклогексадиеном.
У циклических соединений отрицательные атомы водорода могут замещаться эквивалентными атомами или группами так же, как отрицательные атомы водорода, содержащиеся в магнитно-нейтральных группах цепных соединений. Конечные продукты, такие как циклогексил хлорид -(CH2)5 • CHCI-, циклогексанол -(CH2)5 • CHOH-, циклогексаламин -(CH2)5 • CHNH2, и так далее, обладают свойствами, похожими на свойства эквивалентных цепных соединений - хлоридов, спиртов, аминов и так далее.
У обычных циклических колец нет атомных групп, обладающих свободой геометрической компоновки, сравнимой со свободой радикалов на обоих концах алифатических цепей. И заменители (у цепей ограниченные радикалами) совсем не появляются у циклических соединений до тех пор, пока ветвь не становится достаточно длинной для того, чтобы поместить конечную группу вне действия сил, возникающих в кольце. В этом случае структура действует как комбинация цепного и кольцевого соединения. Из-за геометрического ограничения область заменителей у обычных видов циклических соединений значительно уже, чем у цепей. Кроме вышеупомянутых CI, OH и NH2 список включает оставшиеся галогены, кислород, CN и CO • OH.
Соединения, образованные прямым замещением двух атомов водорода группы CH2 на кислород называются кетонами, но они не обладают кетонной структурой, поскольку возникающая группа СО становится частью кольца и магнитно-нейтральной группой. Первое замещение создает циклогексанон -(CH2)5 • CO-. Второе замещение создает соединение 1,3-циклогександион -CO • CH2 • CO • (CH2)3-. Замещение СО может расширяться до циклогексан гексона -(CO)6, у которого уже не остается водорода. Также кислород может быть одновалентным, вместо двухвалентного; в таком случае мы получаем такое соединение как циклогексил метил эфир -(CH2)5 • (CH • OCH3)-.
Дополнительные семейства соединений создаются как вторичными замещениями, выливающимися в структуры порядка циклогексил ацетата -(CH2)5 • CH(O • CO • CH3)-, так и параллельными замещениями двух или более нейтральных групп. Примером вида структуры, создающейся множественными замещениями, является 1,2,3-циклопропанэтрикарболсиловая кислота -(CH • CO • OH)3-. Естественно возникающие соединения этого циклического класса являются сильно ветвящимися кольцами, начиная с таких соединений как ментол -CHCH3 • CH2 • CHOH • (CH • CHCH3 • CH3) • (CH2)2 и кончая очень сложными структурами. Но все они следуют тем же общим структурным паттернам, что и более простые циклические соединения. Поэтому дополнительное обсуждение не требуется.
Как уже упоминалось, группы CH2 обладают значительной степенью структурной широты за счет трехатомного состава. Угол между действующими линиями силы варьируется от почти 120º у циклопропана до менее 15º у самых больших циклических колец, изученных до настоящего момента. Двухатомные группы, такие как СН, не обладают такой структурной свободой и ограничены узкой областью вблизи 60º. Теоретически, точные пределы еще не установлены, но трудности, связанные с созданием производных циклооктатэтрина -(CH)8, указывают, что это соединение пребывает на пределе устойчивости. Это допускало бы максимальное отклонение почти 15º от угла в 60º у кольца, состоящего из шести членов. Атомы, из которых состоят молекулярные соединения, обладают ограниченной областью, в которой они могут принимать положения выше или ниже центральной плоскости молекулы. Поэтому реальные углы между действующими линиями силы слегка отклоняются от вышеприведенных цифр, основанных на положениях в центральной плоскости. Но это не влияет на следующий вывод: циклическое кольцо очень гибкое, а ароматическое кольцо практически жесткое.
До тех пор, пока у кольца имеется хотя бы одна группа CH2, оно обладает циклической гибкостью. Несмотря на жесткость части кольца, занимаемой четырьмя группами СН, циклопентадиен существует потому, что группа CH2, завершающая структуру, может приспосабливаться к положению, необходимому для закрытия кольца. Но если все трехатомные группы замещены двухатомными группами или единичными атомами, кольцо становится таким же жестким, как ароматическое. Например, циклобутадиен состоял бы только из четырех групп CH2, и максимальное отклонение линий силы СН (где-то рядом с 75º) меньше, чем 90º, которое потребовалось бы для закрытия циклобутадиенового кольца. Поэтому все попытки создать такое соединение потерпели неудачу.
Свойства разных кольцевых соединений в значительной степени зависят от следующего фактора: ограничиваются ли члены колец некими определенными положениями или обладают существенным диапазоном изменчивости, внутри которого они могут приспосабливаться к требованиям для соединения. В свете естественной пограничной линии ароматическая классификация (как она используется в этой работе) ограничивается жесткими структурами, особенно соединениями, полностью состоящими из одновалентных групп СН или их одновалентных заместителей, исключая структуры, связанные с вероятно присутствующими атомами углерода.
Из-за ограничений на положения атомов ароматические соединения (за исключением циклооктатэтрана) ограничиваются шестичленными кольцами, одновалентными эквивалентами циклогексана и его производными, а циклобутан, циклогептан и так далее не имеют ароматических аналогов. Структурная жесткость в значительной степени ограничивает подвижность атоматических колец в образовании соединений, но это компенсируется другими влияниями того же фактора. Положения в цепных соединениях, открытые наибольшему разнообразию положений, - это концы цепи и более длинные ветви, если таковые имеются.
У ароматических колец положение каждого кольца до некоторой степени обладает свойствами конца. Вследствие негибкости кольца максимальное расстояние между группами 1-3 в кольце на 10% меньше, чем расстояние между эквивалентными группами в алифатической цепи после принятия в расчет небольшой существующей гибкости. Это позволяет некоторые дополнительные комбинации элементов в пределах действия свободных электрических смещений. У этих колец мы находим не только группы COH, CCI, CNH2 и так далее - одновалентные эквиваленты комбинаций, составляющих циклические кольца и внутренние части цепных соединений, но и другие комбинации, такие как CNO2 и CSH, пребывающие выше магнитно-нейтральных пределов у неароматических структур. Количество доступных комбинаций, у которых нейтральная группа СО сопровождает отрицательный радикал, тоже увеличивается.
Вторичные замещения увеличивают длину и расширяют разнообразие магнитно-нейтральных групп кольца, что создает широкое разнообразие одноветвистых соединений порядка изобутил бензола -(CH)5 • (C • CH2 • CHCH3 • CH3)- и N-этила анилина -(CH)5 • (C • NH • CH2 • CH3)-. Основная причина разнообразия мононуклеарных ароматидов - способность к множественному ветвлению. Ароматические кольца обладают не только б о льшим разнообразием доступных заместителей, чем любой другой вид молекулярного соединения, но и б о льшим количеством положений, куда можно вводить эти заместители. Такая подвижность осложняется тем, что у колец, как и у цепей, порядок последовательности групп обладает определенным влиянием на свойства соединения. Например, поведение 1,2-дихлорбензола -(CCl)2•(CH)4, во многих отношениях сильно отличается от поведения 1,4-дихлорбензола -CCl • (CH)2 • CCl • (CH)2.
Значимой характеристикой ароматических колец является способность использовать большее количество менее подвижных заместителей. Например, сведение таких групп, как NO2, к роли отрицательного радикала в цепях означает, что в любом цепном соединении может существовать лишь одна такая группа до тех пор, пока ветвь не становится настолько длинной, что соединение действует как союз двух цепей. У ароматического кольца такое ограничение отсутствует, и весьма распространены соединения с тремя или четырьмя высоко реактивными азотными группами у кольца из шести членов. Список включает такие известные вещества как пикриновая кислота (2,4,6-тринитрофенол) -COH • CNO2 • CH • CNO2 • CH • CNO2-, и тротил (2,4,6-тринитротолуол) -CH3 • CNO2 • CH • CNO2 • CH • CNO2-.
У ароматических колец, поскольку в группе СН имеется лишь один атом водорода, заместители ограничены одновалентными, отрицательными компонентами. Для установления валентного равновесия с двухвалентным атомом или радикалом требуется два ароматических кольца. Поэтому двухвалентные атомы или группы создают способы объединения двух колец. Например, дифенил эфир обладает структурой -(CH)5 • C-OC • (CH)5-, у которой атом кислорода не является членом ни одного кольца, но участвует в валентном равновесии. Аналогично, двухвалентный, отрицательный радикал NH создает дифенил амин
-(CH)5 • C-NH-C • (CH)5-.
Каждое из колец является очень устойчивой структурой с минимум одиннадцатью заменяющими атомами и вероятностью значительного увеличения посредством замещения. Таким образом, такой способ объединения колец - довольно доступный процесс строительства молекул большого размера. Дальнейшие прибавления и замещения можно делать не только в кольцах и их ветвях, но и в связующих звеньях между ними. Так, прибавление двух групп CH2 к дифениловому эфиру создает дибензил эфир -(CH)5 • CCH2 • O • CH2 C • (CH)5-.
Согласно определению ароматического соединения, такие многокольцевые структуры не являются чисто ароматическими, поскольку под определение не подходят связующие звенья. Мы столкнемся с этой ситуацией, несмотря на то, как создаются разные органические классификации, поскольку более сложные соединения являются преимущественно комбинациями разных основных видов структуры. Обычно соединение классифицируется как кольцевая структура, если оно содержит кольцо любого вида, даже если кольцо может быть лишь небольшим придатком на длинной цепи. Соединение считается ароматическим, если присутствует, по крайней мере, одно ароматическое кольцо.
У многокольцевых соединений комбинация (CH)5 • C - бензоловое кольцо меньше одного атома водорода - действует как одновалентный, положительный радикал - радикал фенила, и простые замещенные соединения могут называться либо производными бензола, либо соединениями фенила; то есть, хлорбензолом или фенил хлоридом. Общая положительная одновалентность – это валентное условие, при котором кольцо сохраняется, если убирается атом водорода; но общая валентность создается в основном за счет валентности +1 одного атома углерода, от которого отделяется атом водорода. Все остальные группы остаются нейтральными, но из этого необязательно следует, что валентность углерода останется +1. Как уже подчеркивалось, валентность – просто вопрос ориентации вращения, и, действуя в одиночку, любой атом может принимать любую из возможных валентностей, если в окружающей среде не существует никаких определенных препятствий. Поэтому один атом углерода свободно приспосабливается к разной окружающей среде посредством переориентации на основе любой из альтернативных валентностей: +2, +4 или –4.
Если соединяются два радикала фенила, межатомные силы будут стремиться установить равновесие. Предпосылка для равновесия сил - равновесие валентности. Следовательно, атомы углерода будут переориентироваться так, чтобы сбалансировать валентности. Имеются два возможных способа достижения результата. Поскольку углерод обладает лишь одной отрицательной валентностью (–4), один атом углерода принимает эту валентность, второй атом должен принимать валентность +4, чтобы прийти к равновесию. У комбинации двух фениловых групп валентные изменения могут происходить у двух независимых атомов углерода без всякой модификации нейтральных групп. Поэтому это самая вероятная структура в таких соединениях как бифенил -(CH)5 • C-C • (CH)5-. Для формирования азобензола -(CH)5 • CNNC • (CH)5- в комбинацию с четырехвалентными атомами углерода можно ввести аналогично сбалансированные пары атомов азота с положительной и отрицательной валентностью 3.
Альтернатива - совершение обоих валентных изменений в той же группе фенила, придавая одному атому углерода валентность (–4) и увеличивая валентность атома углерода в соседней, нейтральной группе от +1 до +4. Результат – кольцо с четырьмя нейтральными группами СН: группой СН с результирующей валентностью +3 и единичным атомом углерода с валентностью (–4). С помощью этой операции группа фенила меняется с одновалентного, положительного радикала C • (CH)5 до одновалентного, отрицательного радикала (CH)4 • CH • C. Подобно группе метила, которая может действовать либо как положительный радикал CH3 с валентностью +1, либо как отрицательный радикал CH2 • H с валентностью (–1), группа фенила способна соединяться с веществами любого вида валентности, принимая отрицательную валентность в комбинации с положительным компонентом и положительную валентность в комбинации с отрицательным атомом или группой. Она отрицательная во всех соединениях фенила металлоорганического класса и образует не только такие соединения, как фенил меди Cu-C • (CH)5- и дифенил цинка Zn(-C • (CH)5-)2, но и комбинации фенил-галоидных структур, такие как фенил олова трихлорид SnCl3-C • (CH)5-.
В комбинации с радикалом CH3 группа фенила положительная. Любой радикал может принимать любую валентность, но вероятности группы метила почти равны, а у группы фенила вероятнее положительная валентность, поскольку кроме удаления атома водорода в бензоловом кольце не совершается никакое изменение. Поэтому комбинация -(CH)5 • CCH3- является толуолом с положительным фенилом и отрицательным метилом (двухвалентным углеродом), а не фенил метаном с отрицательным фенилом и положительным метилом (четырехвалентным углеродом).
Эта разновидность недоступна в комбинации с другими углеводородными радикалами или с самим углеродом. В таких соединениях радикал фенила заменяет водород и является отрицательным. Например, дополнительные замещения фенила сводят радикал CH3 к радикалу CH2. Эта группа не может иметь результирующую валентность (–2), которая понадобилась бы для соединения с положительными радикалами фенила, и у получающегося соединения – дифенил метана - обе группы фенила принимают отрицательный статус. Аналогично, олефиновые и ацетиленовые бензолы обладают такой структурой, у которой радикал фенила отрицательный. Например, стирол – это не винилбензол -(CH)5 • C-CH2 • CH, поскольку эта комбинация содержала бы два положительных компонента и ни одного отрицательного. Это фенил этилен CH • CH2 • -C • (CH)5-, у которого СН положительна, а группа фенила отрицательна.
Интересное соединение фенила – фенил ацетилен, традиционная формула которого C6HS • C • CH. На основании нашего вывода, что водород отрицателен к углероду, атом водорода в ацетилене СН был бы отрицательным. Но это не так, поскольку его можно заменить натрием. Тогда кажется очевидным, что это фенил карбид -(CH)5 • CC2H - соединение аналогичное бутадиену, которое мы уже определили как карбид C • CH • C2H. Как уже замечалось, относительная отрицательность углерода и водорода не имеет значения в связи с радикалом карбида, обладающим результирующей, отрицательной валентностью, и не может быть никакой другой, кроме отрицательной, невзирая на то, с каким элементом или группой он соединяется. Согласно учебникам, соединение фенила определяется как ацетилен потому, что “вступает в типичные реакции ацетилена”. Но то же самое делает любой другой карбид. У первых велосипедистов ацетиленовая лампа была “карбидной лампой”.
Как и радикал фенила, циклические радикалы могут приспосабливаться либо к положительному, либо отрицательному положению в молекуле. Эти радикалы положительны в монозамещенных соединениях. Замещение метила создает гексгидротолуол, а не циклогексил метан. Но если в группе метила имеются два циклических замещения, оба они отрицательные, а результат - дициклогексил метан.
Сейчас было бы желательно исследовать влияния разных модификаций кольцевой структуры на сцепление молекулы. За основную ароматическую структуру можно принять бензоловое кольцо. Учебники и монографии по ароматическим соединениям обычно содержат главу или, по крайней мере, обширный раздел о “проблеме бензола 69”. По существу, проблема в следующем: все сообщения, основанные на наблюдении и эксперименте, указывают на то, что межатомные силы и расстояния между любыми двумя из шести групп СН в кольце идентичны. Но теория химической “связи” не способна рассматривать структуру молекулы бензола, не используя два или более вида связей. Современное решение проблемы – смести ее под ковер посредством допущения, что при переходе от одной компоновки к другой связи структуры меняются или “резонируют”.
СТОВ показывает, что силы между группами в бензоловом кольце действительно идентичны. Однако, как подчеркивалось в предшествующем обсуждении, существование и природа химических соединений не определяются силами сцепления между атомами различных элементов, а отношениями направлений, которые могут принимать вращения атомов, чтобы позволить элементам с электрическим вращением во времени устанавливать устойчивые равновесия сил в пространстве. Результаты теории согласны с тем, что влияния ориентации, позволяющие группам СН комбинироваться в бензоловое кольцо, принимают два разных вида: ближнее и дальнее. Также они раскрывают, что природа ориентирующих влияний не оказывает действия на величину межатомных сил. И это объясняет, почему разница между этими силами не может быть обнаружена экспериментально. Силы между двумя любыми нейтральными группами СН идентичны.
Поскольку факторы ориентации вынуждают атомы выравнивать вращение в конкретных особых относительных направлениях, в определенном смысле они являются силами. И чтобы отличить их от реальных сил сцепления, удерживающих вместе атомы, группы и молекулы в положениях, определенных факторами ориентации, применительно к ориентации мы будем пользоваться термином ”влияния”, а не “силы”, хотя это внесет в изложение элемент неуклюжести. Природу влияний в связи с бензоловым кольцом можно проиллюстрировать схемой ориентации, уже представленного вида.
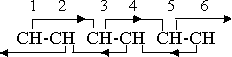
На схеме пары групп CН 1-2, 3-4 и 5-6, удерживаются в комбинированных положениях влияниями ориентации направленного характера, которые оказываются всеми магнитными группами или соединениями. Альтернативные группы 1-3, 2-4 и так далее пребывают в пределах единицы расстояния, и, следовательно, в пределах действия влияний ориентации. Например, первичное влияние группы 1 направлено к группе 2, но группа 3 тоже пребывает внутри единицы расстояния. Поэтому имеются дальнее вторичное влияние 1-3 и ближнее первичное влияние 1-2. Вследствие направленной природы влияний ориентации, первичное влияние 2-3 отсутствует, но пары 1-2 и 3-4 удерживаются в положениях, обусловленных вторичными влияниями 1-3 и 4-2.
Если заменить один из атомов водорода на какой-то отрицательный заместитель, ситуация ориентации не изменится. Новая нейтральная группа или та часть ее, которая пребывает в пределах действия сил кольца, если группа длинная, берет на себя функции неизмененной группы СН. Однако удаление атома водорода и преобразование молекулы бензола в положительный радикал фенила меняет паттерн ориентации:
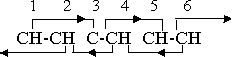
Сейчас вторичное влияние 3-5 устранено, поскольку единичный атом углерода не обладает характеристикой свободного электрического вращения магнитных групп или соединений, но оставшихся влияний ориентации еще достаточно для удержания структуры вместе. Дальнейшее изменение валентности, необходимое, если радикал фенила принимает отрицательную валентность, устраняет вторичное влияние 4-2, поскольку группа 4 больше не является магнитной. Два атома углерода и один атом водорода объединяются в радикал ССН, результирующая валентность которого составляет (–1). Этот радикал не оказывает ориентирующего влияния на соседей, но на него влияют соседние, магнитно-нейтральные группы. Паттерн ориентации принимает вид:

Как уже объяснялось, атомы углерода в комбинации ССН обладают валентностями +4 и (–4). Убирая атом водорода из этой группы, мы получаем кольцо, у которого четыре нейтральные группы СН комбинируются с двумя индивидуальными атомами углерода. Эта структура нейтральна и способна существовать как независимое соединение. В отличие от молекулы метилена она так и поступает, потому что обладает сильной тенденцией к формированию двойного кольца. Четыре группы СН, примыкающие к комбинации С-С, могут дублироваться на противоположной стороне линии действия С-С, формируя еще одно подобное кольцо, использующее ту же пару атомов углерода как часть своей кольцевой структуры. Дело в том, что влияния, возникающие в результате свободных электрических вращений, оказываются атомами углерода групп СН лишь на одной стороне. Они никоим образом не пересекаются с существованием подобных влияний на другой стороне. Отношения ориентации на второй стороне идентичны отношениям на первой стороне. Ни одно кольцо не может забрать атом водорода и стать радикалом фенила потому, что присутствие другого кольца препятствует приближению свободных атомов водорода. Следовательно, соединение с двумя кольцами обладает высокой степенью устойчивости.
Пример такого соединения – нафталин -(CH)4 • C=C • (CH)4 - уплотненный кольцевой ароматический углеводород. В этой работе в формуле соединения двойная линия между двумя атомами углерода - это символ, указывающий на структуру вида уплотненного кольца, у которой кольца связаны в двух положениях, а не в одном как у таких соединений, как бифенил. Этот символ не имеет ничего общего с “двойными связями” электронной теории.
Третье кольцо, прибавленное таким же способом, образует антрацин. Дальнейшие линейные прибавления создают такие серии соединений как нафтацин, пентацин и так далее. Но совсем не обязательно, чтобы прибавления делались линейно. Поэтому каждое соединение сопровождается другими соединениями, имеющими тот же состав, но разные структуры. Например, соединения состава нафтацена, состоящие из четырех колец (C18H12), включают хризен, нафтантрацен, 3,4-бензофенантрен и трифенилден. Пирен обладает теми же четырьмя кольцами, но более компактной структурой и составом C16H10.
Структурное поведение уплотненных колец, по существу, то же, что у единичных колец бензола. Они объединяются для формирования таких соединений как биантрил и банфтил и действуют как радикалы (нафтил, антрил, фенантрил и так далее). Посредством замещения на водород они присоединяют больше колец, создавая такие соединения как трифенил антрацен. С помощью других отрицательных заместителей, доступных ароматическим кольцам, они формируют огромное разнообразие соединений. В эту категорию входят многие интересные и важные соединения, но у них нет новых структурных характеристик. Поэтому они пребывают вне сферы настоящего обсуждения.
Для устойчивости не требуются две группы СН среднего кольца структуры антрацина, и их можно убрать. Полученное соединение – бифенилен -(CH)4 • CC=CC • (CH)4. Структура с одной группой СН в среднем кольце, промежуточная между антрацином и бифениленом, исключается низкой вероятностью непрерывного существования единичной группы СН, но подобное соединение может формироваться помещением группы CH2 в промежуточное положение, поскольку группы CH2 не ограничены пребыванием в парах. Новое соединение – флуорен. Другая группа CH2 в противоположном положении восстанавливает структуру антрацина в циклическом среднем кольце. Такое соединение называется дигидроантрацином.
Как уже упоминалось, кольцо даже с одной группой CH2 значительно отклоняется от типичного ароматического поведения, поэтому любое такое кольцо классифицируется как циклические структуры. Но этот эффект ограничивается определенным кольцом, а любые прилегающие ароматические кольца сохраняют ароматический характер. Поэтому такие соединения как флуорен дигидроантрацин должны рассматриваться как комбинация цикло-ароматических структур. Таких соединений очень много, они разнообразны, но принципы комбинирования те же, что и у чисто ароматических соединений, и не нуждаются в повторении. Поскольку циклические соединения менее устойчивы, чем соответствующие ароматические соединения, структуры комбинаций не охватывают такую большую область, как ароматические соединения. Но такая устойчивая структура как нафталин проходит через всю область замещения. Начиная с чисто ароматического соединения, последовательные пары атомов водорода могут прибавляться до образования чисто циклического соединения - декагидронафталина.
Уменьшение разнообразия комбинационных структур, за счет ослабления силы сцепления в циклическом кольце по сравнению с ароматическим кольцом, в некоторой степени препятствуют способности групп CH2 формировать кольца разных размеров. Например, 1,2,3,4-тетрадронафталин может терять одну из групп CH2 и формировать индан -(CH)4 • C=C • (CH2)3-. Из-за гибкости группы CH2, циклическое кольцо в этом соединении способно замыкаться, даже если две оставшиеся группы CH2 заменяются СН. Это создает инден -(CH)4 • C=C • (CH)2 • CH2.
Полинуклеарные циклические соединения образуются так же, как полинуклеарные и комбинационные структуры, но значительно уступают им в разнообразии. Бифенилу и его продуктам замещения соответствуют дициклопентил, дициклогексил и так далее и их производные; трипентил метан имеет циклический эквивалент трициклогексил метан; циклическим аналогом нафталина является бициклодекан и так далее.
Последнее основное подразделение кольцевых соединений – гетероциклическая группа. В нее входят все соединения, у которых любые атомы углерода в циклических или ароматических кольцах замещаются другими элементами. Основная причина выделения этих соединений в особую группу в том, что большинство замещений углерода другими элементами требует валентных изменений того или иного вида, в отличие от замещений водорода, которые обычно не включают валентных модификаций (кроме тех случаев, когда два одновалентных атома водорода заменяются двухвалентным заменителем).
Некоторые гетероциклические замещения являются замещениями двух групп; в таких случаях обычная циклическая или ароматическая структура не меняется. Например, начиная с хинона -(CH)2 • CO • (CH)2 • CO- (ароматического соединения углерода) и заменяя две группы СН нейтральными группами NH, мы получаем урацил -NH • CO • NH • CH • CH • CO-. Еще одно парное замещение убирает последние углеводородные группы и создает уразин -NH • CO • NH • NH • CO • NH-. У уже упомянутого сложного циклогексан гексона заменен весь водород, а у боразола BH • NH • BH • NH • BH • NH- убирается весь углерод. Все эти гетероциклические соединения состоят исключительно из двучленных, магнитно-нейтральных групп и, следовательно, обладают структурой бензола - шестью группами, организованными в жесткое ароматическое кольцо.
Чаще всего гетероциклический заместитель – это единичный атом или радикал. И для поддержания валентного равновесия такое замещение требует изменения валентности в какой-то другой части кольца. Поэтому замещения часто происходят в виде сбалансированных пар. Например, у пирона -(CH)2 • CO • (CH)2 • O- комбинация СО не является нейтральной группой, а радикалом с валентностью +2, балансирующим валентность (–2) атома кислорода. Радикал CH2, у которого углерод имеет обычную валентность +4, играет ту же роль у пирана -(CH)2 • CH2 • (CH)2 • O-. Замещение двух атомов азота со сбалансированными валентностями +3 и (–3) в ароматическом кольце создает диазин. Если атомы азота находятся в положениях 1,2, соединение называется пиридазин -N•N•(CH)4. Свойства соединений 1,3 и 1,4 достаточно отличаются от свойств пиридазина, поэтому им даются другие названия, соответственно пирамидин и пиразин.
Поскольку положительные и отрицательные радикалы в кольце не обладают фиксированными положениями (подобно двум концам цепей), их статус невозможно определить положениями, как мы делали это в формулах цепных соединений. Чтобы формула представляла реальную структуру настолько точно, насколько это возможно, следует разработать подходящий метод определения. В целях настоящего обсуждения это не обязательно и может подождать до дальнейшего изучения.
Нижеприведенные схемы пирана и пиридазина типичны для гетероциклических соединений с замещениями одного атома или радикала:
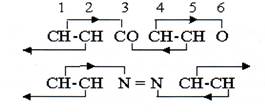
Если равновесие валентности не устанавливается с помощью пары заместителей, необходимо изменение валентности одной из нейтральных групп. Замещенный в кольце единичный атом азота где-то в структуре требует валентности +3, чтобы сбалансировать отрицательную валентность азота. Это легко выполняется посредством сдвига валентности одного из атомов углерода до +4. Тогда реконструированное кольцо состоит из атома азота с валентностью (–3), радикала СН с валентностью +3 и четырех нейтральных групп СН. Такое соединение называется пиридином -(CH)5 • N-. Гидратация может выполняться шаг за шагом, посредством промежуточных соединений, вплоть до соответствующей циклической структуры - пиперидина -(CH2)5 • NH-.
Если в ароматическое кольцо вводится кислород или другой отрицательный двухвалентный компонент, необходимое балансирование валентности может достигаться последовательным замещением одной из нейтральных групп СН на радикал CH2, как уже отмечалось в случае пирана. Или требуемого равновесия можно достичь без введения дополнительного водорода, если валентность углерода в двух группах СН повышается до уровня +2 (первичная магнитная валентность), образуя два радикала СН, каждый из которых имеет валентность +1. В кольце, состоящем из шести членов, остается нестабильное нечетное число нейтральных групп СН, но структура обладает достаточной гибкостью для замыкания кольца на базе пяти членов. Стабильность восстанавливается испусканием нейтральной группы. Возникающее соединение называется фураном -(CH)4 • O-, кольцом с пятью членами: одним атомом кислорода, двумя нейтральными группами СН и двумя одновалентными, положительными радикалами СН. Замещение на серу вместо кислорода создает тиофен -(CH)4 • S-, а помещение в то же положение отрицательного радикала MN производит пиррол -(CH)4 • NH-. Каждое соединение типа фурана существует и в циклических дигидро и тетрагидро формах. Паттерн ориентации фурана:
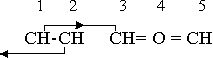
Важная характеристика всех колец класса фурана, состоящих из пяти членов, - равновесие валентности, в котором участвуют три из пяти компонентов, два оставшихся компонента являются нейтральными группами, обеспечивающими способность формирования кольца. У фурана комбинация равновесия C+-O•2-C+. Формирование подобной комбинации с азотом в положительном положении требует, чтобы какой-то элемент или радикал, положительный к азоту, занимал положительное положение, и в гетероциклическом подразделении такую роль обычно берет на себя сам азот. При таких условиях самая вероятная валентность +3, как у гидразина. Тогда две валентности азота, +3 и (–3), пребывают в равновесии, а пятый компонент кольца из пяти членов должен быть нейтральной группой. Поскольку это целостная группа, роль нейтральных групп отводится циклической группе CH2 и нейтральному трио N+3-N-3-CH2°.
Результат - соединение изопиразол -N • CH • CH • CH2 • N-. Альтернативная компоновка группы создает изоимидазол -N • CH2 • N • CH • CH-. Разновидность этой структуры сдвигает атом водорода из группы CH2 к положительному азоту, что меняет нейтральную комбинацию на NH+2-N-3-CH+1. На этой основе формируются такие соединения как пиразол -N • (CH)3 • NH- и имидазол -N • CH • NH • CH • CH-.
Посредством комбинации с другими кольцами из этих основных гетероциклических видов может образовываться огромное разнообразие уплотненных систем, таких как кумарон (бензофуран), индол (бензопиран), хинолин (бензопиридин) и так далее. И единичные кольца, и уплотненные системы открыты для дальнейшего увеличения с помощью всех обсужденных процессов прибавления и замещения. Этому классу принадлежит значительная часть известных органических соединений. Однако со структурной точки зрения основные принципы, вовлеченные в формирование всех этих соединений, те же, что и освещенные в вышеприведенном обсуждении.
На предыдущих страницах мы столкнулись с несколькими видами изомерии – существованием разных соединений с одним и тем же составом. Одни соединения (цианиды и изоцианиды) отличаются только валентностью; другие (прямая цепь и ветвящиеся парафины) отличаются положением нейтральных групп; третьи (альдегиды и кетоны) отличаются распределением атомов составляющих элементов в структурных группах. Б о льшая часть изомеров, которые мы исследовали, является отдельными устойчивыми соединениями. Имеются и другие изомерические системы, у которых две формы вещества так легко преобразовываются друг в друга, что устанавливают равновесие, меняющееся в соответствии с условиями, в которых пребывает соединение. Такая форма изомерии известна как таутомерия.
Один из известных примеров таутомерии - “кетоновые” и “энольные” формы определенных веществ. Этилацетоацетат COCH3 • CH2 • CO • (O • CH2 • CH3) - это кетоновая форма соединения, существующего и в энольной форме как этил эфир гидроксикротонной кислоты COH • CHCH3 • CO • (O • CH2 • CH3). Чтобы справиться с изменением физических и химических условий, соединение свободно переходит из одной формы в другую. Это еще один пример изменений валентности для равновесия углерода и водорода и указание на легкость, с которой могут совершаться такие изменения. У радикала COCH3 валентность углерода +4, а весь водород отрицательный. Преобразование в энольную форму включает уменьшение валентности углерода до +2, и для сохранения равновесия один атом водорода сдвигается с (–1) до +1. Тогда группа CH2 в радикале не нужна, и она сдвигается к соседней, нейтральной группе. Оставшаяся часть молекулы не меняется.
Развитие СТОВ еще не включает изучение таутомерии. Оно еще не затронуло и те виды таутомерии, которые зависят от геометрической компоновки частей-компонентов молекулы, такие как оптическая таутомерия. Поэтому эти аспекты общей темы молекулярной структуры будут отложены для последующего изучения.
Эта глава – последняя из четырех, посвященных исследованию структуры химических соединений. Заканчивая обсуждение, было бы уместно указать, как материал этих глав увязывается с общим планом работы, определенным в главе 2. Традиционное обсуждение молекулярной структуры, которое мы находим в учебниках, начинается с эмпирического наблюдения существования определенных химических соединений - хлорида натрия, бензола, воды, этилового спирта и так далее, обладающих определенными свойствами и разными молекулярными структурами. Затем теоретическая трактовка пытается изобрести правдоподобные объяснения существования наблюдаемых соединений, их структур и других свойств. Настоящая работа полностью дедуктивная. Посредством развития необходимых следствий фундаментальных постулатов СТОВ мы находим, что во Вселенной Движения должна существовать материя. Она должна существовать в форме ряда элементов. Элементы должны обладать способностью (разными способами) сочетаться друг с другом для формирования химических соединений. В этой и предшествующих главах выведены самые важные из теоретически возможных видов молекулярных структур и описаны состав и структура конкретных соединений.
Вторая цель этого труда – сравнить теоретические комбинации с наблюдаемыми химическими соединениями. Например, чисто теоретически мы выводим существование соединения в форме цепи, состоящей из трех групп атомов. Первая группа содержит три атома элемента № 1, один атом элемента № 6, результирующая валентность группы +1. Вторая группа имеет два атома элемента № 1, один атом элемента № 6 и нейтральна; то есть, результирующая валентность группы равна нулю. Третья группа состоит из одного атома элемента № 1, одного атома элемента № 8, результирующая валентность группы (–1). Теоретический состав и структура пребывают в полном согласовании с составом наблюдаемого соединения, известного как этиловый спирт, и со структурой этого соединения, полученной в результате физического и химического наблюдения и эксперимента. Следовательно, можно прийти к выводу, что этиловый спирт является химическим соединением, существующим в физической Вселенной, и соответствующим соединению, которое должно существовать в теоретической Вселенной СТОВ. Иными словами, мы определили теоретическое соединение как этиловый спирт.
На предшествующих страницах приведено огромное количество подобных согласований. Они недвусмысленны и почти самоочевидны. Это свидетельствует о корректности, как теоретического развития, так и эмпирического определения молекулярных структур. Если имеются расхождения (как в случае со структурой этилена), они легко объяснимы. Поскольку размер и сложность молекул увеличиваются, количество и разнообразие возможных модификаций теоретической структуры тоже увеличиваются, и даже в большей пропорции, а наблюдаемые расхождения уменьшаются. В случае больших молекул согласованность менее определенна, чем в случае небольших простых молекул; но это не значит, что из-за существования более сложных теоретических соединений возникает какая-то дополнительная неопределенность. Это значит, что доступная эмпирическая информация не адекватна для принятия определенного решения о том, какие из наблюдаемых соединений соответствуют определенной теоретической структуре. Поэтому можно ожидать, что дальнейшее исследование прояснит большую часть вопросов.
Обсуждение химических соединений завершает описание первичных физических сущностей - актеров в драме физической Вселенной. В томе 2 мы начнем распространение теоретических выводов на исследование сам о й драмы - деятельности, в которую вовлечены эти сущности.
Переведено специально для http://www.e-puzzle.ru и http://divinecosmos.e-puzzle.ru
* Прим. перев: Второй том - Основные свойства материи, третий том – Вселенная движения.
[1] Butterfield, Herbert, The Origins of Modern Science, Revisited Edition, The Free Press, New York, 1965, page 18.
[2] Schlegel, Richard, Completeness in Science, Appleton-Century-Crofts, New York, 1967, page 152.
[3] Burbridge and Burbridge, Quasi-Stellar Objects, W.H.Freeman & Co., San Francisco, 1967, page vii.
[4] New Scientist, Feb. 13, 1969.
[5] Dicke, R.H., American Scientist, March 1959.
[6] Woodbridge, Dean E., The Machinery of Life, McGraw-Hill Book Co., New York, 1966, page 4.
[7] Conant, James B., Modern Science and Modern Man, Columbia University Press, 1952, page 47.
[8] Feynman, Richard, The Character of Physical Law, The M.I.T. Press.1967,page 145.
[9] Bridgman, P.W., The Nature of Physical Theory, Princeton University Press, 1936, page 134.
[10] Einstein and Infeld, The Evolution of Physics, Simon & Schuster, New York, 1938, page 159.
[11] Dingle, Herbert, A Century of Science, Hutchinson’s Publications, London, 1951, page 315.
[12] Feynman, Richard, op. cit., page 156.
[13] Margenau, Henry, Quantum Theory, Vol. 1, edited by D.R. Bates, Academic Press, New York, 1961, page 6.
[14] Braithwaite, R.B., Scientific Explanation, Cambridge University Press, 1053, page 22.
[15] Feynman, Richard, op.cit., page 30.
[16] Einstein, Albert, The Structure of Scientific Thought, E.H. Madden, editor, Houghton MiMin Co., Boston, 1960, page 82.
17 Dirac, P.A.M., Scientific American, May 1963.
17. Там же.
18 Butterfield, Herbert, op.cit., page 13.
19 Hobbes, Thomas, The Metaphysical System of Hobbes, M.W. Calkins, editor, The Open Court Publishing Co., La Sane, III., 1948, page 22.
20 North, J. D., The Measure of the Universe, The Clarendon Press, Oxford, 1965, page 367.
21Einstein, Albert, Relativity, Henry Ho It & Co., New York, 1946, page 74.
22 Hocking, William E., Preface to Philosophy, The Macmillan Co, New York, 1946, page 425.
23 Tolman, Richard, The Theory of the Relativity of Motion, University of California Press, 1917, page 27.
24 Winger, Eugene P., Symmetries and Reflections, Indiana University Press, 1967, page 30.
25 Jeans, Sir James, The Universe Around Us, Cambridge University Press, 1947, page 113.
26 Heisenberg, Werner, On Modern Physics, Clarkson N. Potter, New York, 1961, page 16.
27 Heisenberg, Werner, Physics Today, March 1976.
28 Schlegel, Richard, op. sit., page 18.
15 Feynman, Richard, op. cit., page 30.
29 Gold and Hoyle, Paris Symposium on Radio Astronomy, paper 104, Stanford University Press, 1959.
30 Darrow, Karl. K., Scientific Monthly, March 1942.
31 Finlay-Freundlich, E., Monthly Notices of the Royal Fstronomical Society, 105-237.
32 Heisemberg, Werner, Philisophic Problems of Nuclear Science, Pantheon Books, New York, 1952, page 38.
33 Einstein, Albert, Albert Einstein: Philosopher-Scientist, Paul Schilpp, editor, the Library of Living Philosophers, Evanston, 111., 1949, page 67.
34 Alfven, Hannes, Worlds-Antiworlds, W. H. Freeman & Co., San Fracisco, 1966, page 92.
35 Hawkins, David, The Language of Nature, W. H. Freeman & Co., San Fracisco, 1966, page 183.
36 Lindsay, R. B., Physics Today, Dec. 1967.
5 Dicke, R. H., American Scientist, March 1959.
37 Einstein, Albert, Sidelights on Relativity, E. P. Dutton & Co., New York, 1922, page 23.
38 Einstein and Infeld, op. cit., page 185.
39 Einstein, Albert, Relativity, op. cit., page 126.
40 Heisenberg, Werner, Physics and Philosophy, Harper & Bros., New York, 1958, page 129.
41 Einstein, Albert, Foreword to Concepts of Space, by Max Jammer, Harward University Press, 1954.
42 Jeans, Sir James, op.cit., page 78.
43 Schlegel, Richard, Time and the Physical World, Michigan State University Press, 1961, page 160.
44 Whitrow, G. J., The Natural Philosophy of Time, Thomas Nelson & Sons, London, 1961, page 218.
45 Moller, C., Theory of Relativity, The Clarendon Press, Oxford, 1952, page 49.
46 Tolman, Richard C., Relativity, Thermodynamics and Cosmology, The Clarendon Press, Oxford, 1934, page 195.
47 Science, July 14, 1972.
48 Heisenberg, Werner, Philisophic Problems of Nuclear Science, op. cit., hage 12.
49 Thomson, Sir George, The Inspiration of Science, Oxford University Press, London, 1961, page 66.
50 Millikan, Robert A., Time and its Mysteries, Collier Books, New York, 1945, page 24.
51 Jeans, Sir James, Physics and Philosophy, The Macmillan Co, New York, 1945, page 190.
52 Toulmin and Goodfield, The Architecture of Matter, Harper & Row, New York, 1962, page 298.
53 Bridgeman, P. W., A Sophisticate’s Primer of Relativity, Wesleyan University Press, 1962, page 10.
54 Feyerabend, P. K., Philosophy of Science, The Delaware Seminar, Vol. 2 (1962-1963), Bernard Baumrin, editor, Interscience Publishers, New York, 1963, page 17.
55 Einstein and Infeld, op. cit., page 195.
56 Bridgman, P. W., Reflections of a Physicist, Philosophical Library, New York, 1955, page 186.
27 Heisenberg, Werner, Physics Today, March 1976.
57 Will, Clifford M., Scientific American, Nov. 1974
58 Feynman, Richard, op. cit., pages 156, 166.
59 Cohen, Crowe and Du Mond, The Fundamental Constants of Physics, Interscience Publishers, New York, 1957.
59 Cohen, Crowe and Du Mond, op. cit.
60 Alfven, Hannes, Scientific American, Apr. 1967.
61 Boorse and Motz, The World of the Atom, Vol. 2, Basic Books, New York, 1966, page 1457.
62 Hooper and Scharff, The Cosmic Radiation, John Wiley & Sons, New York, 1958, page 57.
63 Swann, W. F. G., Journal of the Franklin Institute, May 1962.
64 Davis, Leverett, Jr., Nuovo Cimento Suppl., 10th Ser., Vol. 13, No. 1, 1959.
65 Donahue, T. M., Physical Review, 2nd Ser., Vol. 84, No. 5, 1951, page 972.
66 Satz, Ronald W., Reciprocity, May 1975.
67 Weisskopf, V. F., Comments on Nuclear and Particle Physics, Jan.-Feb. 1969
68 Pauling, Linus, The Nature of the Chemical Bond, Cornell University Press, 1960, page 217.
69 См. например: Badger, G. M., The Structures and Reactions of the Aromatic Compounds, Cambridge University Press, 1954, Chapter 1.
Не нашли, что искали? Воспользуйтесь поиском: