
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Применение соединений платиновых элементов в медицине.
Многочисленные исследования показали, что цис- изомер дихлородиамминплатины(II) [Pt(NH3)4]Cl2 оказывает лечебное действие при раковых заболеваниях. Действие этого комплекса основано на том, что в нем происходит постепенное замещение хлорид-ионов хелатирующими лигандами. Такими лигандами являются аминокислотные остатки в белках. Координация идет за счет взаимодействия металла с атомами азота лиганда. После замещения хлорид-ионов создаются условия для замещения и групп NH3. В результате платина образует четыре связи с новыми лигандами. Это свойство цис-дихлородиамминплатины приводит к образованию устойчивого комплекса с молекулой ДНК. Таким образом, это вещество ингибирует синтез ДНК. Интересно отметить, что транс-изомер дихлородиамминплатины(II) токсичен, но противоопухолевым действием не обладает:

Наряду с цис-дихлордиамминплатиной(II) противоопухолевой активностью обладают и другие комплексы, содержащие в качестве лигандов амины и хлорид-ионы. Например, цис-диамминтетрахлорплатина (IV) [Pt(NH3)2Cl4] и цис-дианилиндихлорплатина (II) [Рt(NH2C6H5)2Cl2]:

Сплавы Pt — Ir и Pt — Аu применяются в ортопедической стоматологии, для изготовления шприцов; сплавы Pd — Аu, Pd — Аu — Pt, Pd — Pt — Ir — для изготовления хирургических инструментов, в ортопедической стоматологии используют сплавы Pd — Аu или Pd — Ag, Си, Ir. Вживляемые в сердце электроды для стимуляции изготовлены из сплава Pt — Ir; Ir — Pt — эталон массы (а раньше и длины). Для дезинфекции питьевой воды применяют О3, его можно получить по реакции:
 , где Ir — катализатор (порошкообразный иридий).
, где Ir — катализатор (порошкообразный иридий).
Осмий (VIII) оксид OsO4 применяется как фиксатор ткани (липидный стабилизатор) для гистологических исследований в виде 1%-ного раствора в ацетоне. OsO4 можно использовать и для электронно-микроскопического выявления ферментов. Механизм действия OsO4 может быть представлен в следующем виде:

Восстановление может идти глубже и будет образовываться Os2O3 или OsO. Все эти соединения имеют темно-коричневый или черный цвет, т.е. обеспечивается эффект контрастирования участка клетки или ткани (образуются эфиры холестерина и триглицеридов).
Комплекс [Ru(NH3)4(OH)Cl]CI — рутениевый красный также применят для анатомических и гистологических исследований. Его раствор (1:5000) окрашивает в розово-красные тона пектин.
I B-группа
Медь Сu — необходимый микроэлемент живых организмов. Серебро Ag и золото Аu — примесные микроэлементы. Их соединения применяют в медицине
Высокое сродство металлов группы 1B к сере определяет большую энергию связи М—S, а это, в свою очередь, обусловливает определенный характер их поведения в биологических системах.
Катионы этих металлов легко взаимодействуют с веществами в состав которых входят группы, содержащие серу. Например, ионы Ag+ и Сu2+ реагируют с дитиоловыми ферментами микроорганизмов по схеме:

Включение ионов металлов в состав белка инактивирует ферменты, разрушает белки.
Такой же механизм лежит и в основе действия содержащих серебро и золото лекарственных препаратов, применяемых в дерматологии.
В организме медь функционирует в степенях окисления + 1 и +2. Ионы Сu+ и Сu2+ входят в состав «голубых» белков, выделенных из бактерий. Эти белки имеют сходные свойства и называются азуринами.
Медь (I) более прочно связывается с серосодержащими лигандами, а медь (II) с карбоксильными, фенольными, аминогруппами белков.
Медь — биогенный элемент, содержится в тканях животных и растений. Общая масса меди в организме взрослого человека примерно 100 мг, что составляет около 0,0001%. Примерно 30% этого количества содержится в мышцах. Печень и мозг также богаты медью. Металлическая медь и ее соединения токсичны.

Наиболее важными с физиологической точки зрения являются медьсодержащие белки — цитохромоксидаза и супероксиддисмутаза.
Цитохромоксидаза — один из компонентов дыхательной цепи, локализованной в мембранах митохондрий. Обеспечивает клеточное дыхание, восстанавливая кислород до воды на конечном участке дыхательной цепи.
Цитохромоксидаза (Мr = 200 000) состоит из семи белковых субъединиц и четырех связанных с ними активных центров: двух молекул гема, связывающих ионы железа, и двух ионов меди, непосредственно связанных с белковыми субъединицами. Такая структура цитохромоксидазы обеспечивает передачу четырех электронов из дыхательной цепи и осуществление реакции:

При неполном восстановлении кислорода в дыхательной цепи образуется супероксид-анион радикал: 
Супероксид-анион обладает еще более высокой окислительной способностью, чем водородпероксид Н2О2. Взаимодействие О2 с органическими соединениями клетки приводит к образованию радикалов и нарушению нормального развития клетки.
Повреждающее действие супероксид-аниона предотвращается медьсодержащим ферментом супероксиддисмутазой (СОД). Этот фермент катализирует реакцию:
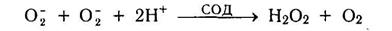
Образующийся при этом водородпероксид разлагается каталазой. В результате совместного действия содержание радикалов в клетке поддерживается на безопасном уровне.
Интересно, что переносчиком кислорода у моллюсков и членистоногих является не гемоглобин, а гемоцианин (от греч. кианос — лазурный). Кровь этих животных имеет голубой цвет.
Гемоцианин в зависимости от биологического вида имеет различную молекулярную массу (у омара Мr = 825000) и состоит из большого числа белковых субъединиц (Мr от 25000 до 35000). Каждая субъединица имеет центры связывания кислорода. Эти центры представляют собой медьпротеиновые комплексы кислорода. Эти центры представляют собой медьпротеиновые комплексы (биокластеры) с двумя ионами меди. Каждая такая пара связывает одну молекулу кислорода.
Ежедневно организму требуется 2,5—5,0 мг меди. При недостатке в организме меди может развиваться болезнь — медьдефицитная анемия. Недостаток в организме медиприводит к деструкции кровеносных сосудов, патологическому росту костей, дефектам в соединительных тканях. Кроме того, считают, что дефицит меди служит одной из причин раковых заболеваний. В некоторых случаях поражение легких раком у людей пожилого возраста врачи связывают с возрастным понижением меди в организме. Многое известно и о транспорте меди в организме. Значительная часть меди находится в форме церулоплазмина. Содержание меди в организме варьируется от 100 до 150 мг с наибольшей концентрацией в стволе мозга. Большой расход меди ведёт к дефициту и неблагоприятен для человека. Прогрессирующие заболевание мозга у детей (синдром Мениеса) связано с дефицитом меди, так как при этом заболевание не хватает медьсодержащего фермента. Некоторые улучшения в состоянии этих больных было получено при введение меди. Избыточное количество меди в организме также неблагоприятно и ведет к развитию тяжелых заболеваний. При болезни Вильсона содержание меди увеличивается практически в 100 раз по сравнению с нормой. Медь обнаруживается во многих тканях, но особенно её много в печени, почках и мозге. Её можно увидеть на роговице в виде коричневых или зелёных кругов. В настоящие время установлено, что первоначально избыточные концентрации меди возникают в печени, затем в нервной системе, проявление расстройства этих органов наступают в том же порядке. Симптомы болезни Вильсона включают цирроз печен, нарушение координации, сильный тремор, прогрессирующие разрушение зубов. Степень выраженности симптомов зависит от количества содержание меди. Уменьшение клинической симптоматики может быть достигнуто использованием хелатирующих агентов, выводящих излишки запасов меди. Сам факт исчезновение симптомов после подобной терапии означает, что разрушение мозга является больше биологическим процессом, нежели структурным.
Несмотря на генетически зависимую природу заболевания, отложение меди в тканях наблюдается не всегда. Медь откладывается в определённые медь протеины печени, при болезни Вильсона происходит нарушение в синтезе апоцерулоплазмина таким образом, что медь не может связываться с этими белками и начинает откладываться в других местах. Понятно, что это не может служить единственным объяснением, так как у ряда пациентов уровень церулоплазмина понижен незначительно. Кроме того, в больших количествах медь обнаруживается в печени новорождённых, причём 2% общего количества меди связано с белком. Через три месяца концентрация снижается до нормального уровня, с того времени печень способна синтезировать белок цирулоплазмин. Существует другая точка зрения на болезнь Вильсона: структура белка металлотеонина при болезни Вильсона нарушена, и это ведёт к повышенному связыванию ионов меди, что в свою очередь ведёт к нарушению запасов и транспорта меди в организме. У пациентов с болезнью Вильсона было продемонстрировано повышенное связывание меди металлотионеином. При лечение болезни Вильсона употребляют пищу, бедную медью, и применяют хелатирующие агенты, особенно пенисилламин. При многих других заболеваниях наблюдается увеличение меди сыворотки: так при инфекционном гепатите наблюдается увеличение сыворотки меди в 3 раза по сравнению с нормой – 350мкг/100мл. это связано с накоплением церулоплазмина. Повышение меди в крови встречается при таких заболеваниях, как лейкемия, лимфома, ревматоидный артрит, цирроз, нефрит. Высокий уровень меди может быть связан с различными явлениями, и обнаружение высоких концентраций меди сыворотки представляет диагностическую ценность только при одновременном рассмотрение с данными других исследований. Анализ концентрации ионов меди необходимо проводить для оценки эффективности лечения, так как уровень меди прямо пропорционален тяжести заболевания. Это положение верно при гепатитах и злокачественных заболеваниях. Медь необходима для усвоения железа, в частности, при синтезе цитохромоксидазы, которая содержит и железо, и медь. При дефиците меди нарушается нормальное развитие соединительных тканей и кровеносных сосудов.
Широкое применение меди и ее соединений в промышленности и сельском хозяйстве повышает риск отравления этими веществами. Отравления обычно связаны со случайной передозировкой инсектицидов, вдыханием порошка металла, заглатыванием растворов солей меди. Большую опасность представляют напитки, хранящиеся в медных сосудах без защитного покрытия стенок.
Токсическое действие соединений меди обусловлено тем,, что ионы меди взаимодействуют с тиольными —SH-rpynnaми (связывание) и аминогруппами —NH2 (блокирование) белков. При этом могут образовываться биокластеры хелатного типа:

Вследствие таких взаимодействий белки становятся нерастворимыми, теряют ферментативную активность. В результате нарушается нормальная жизнедеятельность.
В качестве наружного средства применяют 0,25%-ный водный раствор меди сульфата CuSO4 при воспалении слизистых оболочек и конъюнктивитах. Малые дозы этого препарата могут применяться во время приема пищи для усиления эритропоэза при малокровии.
Серебро и золото. В организме взрослого человека обнаруживается около 1 мг серебра, т.е. примерно 10 % (1 ч. на миллион), и до 10 мг золота, т.е. примерно 10 % (10 ч. на миллион).
Антисептические свойства растворимых солей серебра известны с древних времен. Священнослужители давно знали, что вода («святая») при хранении в серебряных сосудах долго не портится, т.е. не подвергается микробному загрязнению. В настоящее время это свойство «серебряной» воды используется моряками в дальних плаваниях. Бактерицидные свойства AgCl используются в препаратах для обработки слизистых оболочек газа. Для стерилизации и консервации пищевых продуктов применяется «серебряная вода» — обработанная кристаллами AgCl дистиллированная вода.
Сильные токсические проявления у взрослого человека наблюдаются при приеме внутрь 7 г AgNO3.
Токсическое действие соединений серебра, как и в случае меди, обусловлено главным образом тем, что ионы серебра взаимодействуют с тиольными серо- и азотсодержащими группами белков, нуклеиновых кислот и других биоорганических веществ.
В водном растворе существуют только комплексные соли золота, например, Nа3[Аu(S203)2] и различные тиоловые бионеорганические комплексы.
Механизм токсического действия соединений золота аналогичен механизму токсического действия соединений меди и серебра. В соответствии с общим правилом для тяжелых металлов одной группы токсичность возрастает с увеличением атомного номера в ряду: Сu Ag Аu.
В медицине издавна используются такие препараты, как кристаллический серебро нитрат AgNO3 (ляпис) и его водные растворы. Давно известны также препараты коллоидного металлического серебра протаргол (8 % Ag) и колларгол (70% Ag), которые представляют собой мелкодисперсные порошки с металлическим блеском. Каждая частица таких порошков представляет собой кристаллик восстановленного металлического серебра размером менее 1 мкм с белковой оболочкой из альбумина (протаргол) или коллагена (колларгол). Белковая оболочка защищает кристаллики серебра от слипания и обеспечивает их переход в водную среду (солюбилизирует).
Препараты серебра применяют как противовоспалительные, антисептические и вяжущие средства.
В качестве эффективных противовоспалительных средств применяют также препараты золота. Наиболее известны кризанол (от греч. хризос — золото), с 30%-ным содержанием благородного металла, и коллоидное золото. Главный компонент кризанола — комплекс золота с тиоловым органическим соединением Аu—S—CH2CH(OH)CH2-SO3H.
II B-группы
Цинк Zn, кадмий Cd, ртуть Hg — микроэлементы. В организме взрослого человека содержится 1,8 г (0,0024%) Zn, 50 мг (7  10 – 5%) Cd, 13 мг (2
10 – 5%) Cd, 13 мг (2  10–5%) Hg.
10–5%) Hg.
Токсичность соединений IIБ-группы увеличивается от цинка к ртути.
Водорастворимые соединения оказывают раздражающее действие на кожу. При попадании внутрь организма вызывают отравление.
Токсичны и сами металлы. При вдыхании паров цинка (воздух цинковых производств) появляется «металлическая» лихорадка. Отравление парами ртути в средние века получило название «болезнь сумасшедшего шляпочника».
Токсичность кадмия связана с его сродством к нуклеиновым кислотам. В результате его присоединения к ДНК нарушается ее функционирование.
Хроническая интоксикация кадмием и ртутью может нарушить минерализацию костей. Это связано с близостью ионных радиусов. Поэтому токсичные элементы могут замещать кальций. Это приводит к образованию апатита несовершенной структуры вследствие искажения параметров кристаллического компонента костной ткани. В результате снижается прочность костей.
Соединения Zn, Cd, Hg могут вызывать нарушение белкового обмена, что проявляется в выделении белков плазмы через почки (протеинурия).
Токсичное действие соединений группы IIБ на организм вызывается еще и тем, что ионы этих металлов вступают во взаимодействие с сульфгидрильными SH-группами белков, ферментов и аминокислот.
При взаимодействии ионов металлов с SH-группами образуются слабодиссоциирующие и, как правило, нерастворимые соединения. Поэтому блокирование сульфгидрильных групп приводит к подавлению активности ферментов и свертыванию белков. Ионы двухвалентных металлов блокируют одновременно две SH-группы:

В реакциях подобного типа ионы металлов выступают акцептором, а сера — донором электронов.
Наиболее выражено химическое сродство SH-группам у ртути. Очевидно, это связано с тем, что комплексообразующие свойства ртути выше и она образует более прочные связи с серой.
SH-группы входят в состав более 100 ферментов, активность которых может быть подавлена из-за блокирования этих групп. Поэтому очевидно, насколько важно знать механизм блокирования и методы лечения при отравлении организма металлами.
Известно, что токсические свойства элементов зависят от той химической формы, в какой они попадают в организм. Наиболее токсичны те формы, которые растворяются в липидах и легко проникают через мембрану в клетку.
В литературе описан случай массового отравления ртутью в Японии («болезнь Минамата»). Неорганические соединения ртути под действием ферментов микроорганизмов превращались в метилртуть:

Метилртуть накапливалась в рыбе, а затем с пищей попадала в организм человека. Из-за того, что CH3Hg растворяется в липидах, она накапливается в организме, в том числе и в мозге. Постепенно концентрируясь, метилртуть вызывает необратимые разрушения в организме и смерть. Токсичность ртути связана с агглютинацией (склеиванием, слипанием) эритроцитов, ингибированием ферментов.
Например, сулема HgCl2 вызывает изменение размеров, осмотическую хрупкость и снижение деформируемости эритроцитов, которая необходима для их продвижения по капиллярам.
Кадмий и ртуть — примесные элементы. Около 70% ртути сосредоточено в жировой и мышечной ткани. Кадмий локализуется на 30% в почках, остальное в печени, легких, поджелудочной железе.
Диспергированный ртуть (II) гидроксид в коллоидном состоянии служит бактерицидным средством. Антисептическим действием обладает также белый осадок ртути амидохлорида, который получается взаимодействием водного раствора аммиака с сулемой или каломелью:
HgCl2 + 2NH3 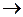 HgNH2Cl + NH4CI
HgNH2Cl + NH4CI
Hg2Cl2 + 2NH3 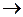 HgNH2Cl + NH4CI + Hg
HgNH2Cl + NH4CI + Hg
Обе реакции используются в химическом анализе для обнаружения ионов Hg + и Hg2+. Ртуть амидохлорид может взаимодействовать в биологической системе с сульфогидроксильными группами белков по реакции:

Этим объясняется антисептическое действие ртути амидохлорида.
Каломель в воде растворяется незначительно (2,1 г Hg2Cl2 на 1 л Н2О при 10 °С) и поэтому менее токсична, чем сулема. Сулема HgCl2 представляет собой бесцветные кристаллы, достаточно хорошо растворимые в воде, спирте, эфире, пиридине и др. Так, в 100 г воды при 0 °С растворяется 4,3 г сулемы, а при 20 °С — 7,4 г. Интересно, что в водных растворах HgCI2 почти не диссоциирует и находится в молекулярной форме. Поэтому водные растворы сулемы не проводят электрический ток.
Цинк — необходимый элемент всех растений и животных. В организме взрослого человека больше всего цинка в мышцах (65%), костях (20%). Остальное количество приходится на плазму крови, печень, эритроциты. Наибольшая концентрация цинка в предстательной железе.

Цинк не проявляет переменной валентности. Видимо поэтому его биокомплексы принимают участие во многих биохимических реакциях гидролиза, идущих без переноса электронов. Ион цинка входит в состав более 40 металлоферментов, катализирующих гидролиз эфиров и белков.
Одним из наиболее изученных является бионеорганический комплекс цинка — фермент карбоангидраза (Mr = 30 000), состоящий, примерно, из 260 аминокислотных остатков.
Ниже схематично представлено положение иона цинка в полости карбоангидразы (КА). Белковый лиганд, связанный с Zn2+, представляет активный центр фермента. Цинка в ферменте всего 0,22%. Тем не менее наличие цинка — необходимое условие каталитической активности карбоангидразы, которая обеспечивает гидратацию СО2:


Протекание этой реакции обусловливает нормальное дыхание. В отсутствие карбоангидразы нормальный газообмен был бы затруднен, так как гидратация СО2 замедлилась бы в 10 000 000 (107) раз.
Как видно из схемы, координационное число Zn2+ в карбоангидразе равно 4. Три связи заняты аминокислотными остатками (His — гистидил), а четвертая связывает гидроксил — ион ОН– или молекулу воды.
Единого мнения о действии карбоангидразы нет. Одни исследователи считают, что цинк координирует молекулу воды, гидратирующую СО2. Другие полагают, механизм «цинк — гидроксид»), что цинк координирует гидроксильную группу при гидратации СО2:

Прежде полагали, что карбоангидраза катализирует только обратимую гидратацию СО2. Однако имеются данные о каталитическом действии карбоангидразы на превращение карбонильной группы (С=О) субстрата в карбоксильную (СООН). В этом случае механизм действия карбоангидразы подобен действию другого цинксодержащего фермента – карбоксипептидазы (КОП). Одна из наиболее изученных форм КОП имеет 307 аминокислотных остатков (содержание цинка 0,19%). Схему реакции превращения карбонильной группы субстрата в карбоксильную, катализируемой КОП, можно представить следующим образом:

Механизм действия КОП окончательно не выяснен, и возможны два варианта. Механизм «цинк — карбоксил» предполагает, что субстрат вытесняет молекулу воды, координированную цинком. Затем карбонильная группа образует связь с ионом цинка. Другой механизм не предполагает образование связи через карбоксил фермента.
Цинк не входит в состав дипептидаз — ферментов, катализирующих гидролиз дипептидов — веществ, состоящих из двух аминокислот.
Цинк образует бионеорганический комплекс с инсулином — гормоном, регулирующим содержание сахара в крови.
Потребность человека в цинке полностью удовлетворяется пищевыми продуктами: мясными, молочными, яйцами.
При недостатке цинка в растениях нарушаются белковый и углеводный обмен, тормозится синтез хлорофилла и витаминов. Дефицит цинка устраняется при использовании цинксодержащих удобрений.
Использование соединений цинка и ртути в медицине основано на их вяжущем, прижигающем и антисептическом действии. В качестве глазных капель применяют 0,25%-ный водный раствор цинк сульфата ZnSO4. В стоматологии цинк хлорид ZnCl2 используют- для прижигания папиллом, для лечения воспаленных слизистых. Применяется также цинк оксид ZnO.
Ртуть(II) хлорид HgCl2 (сулема) очень ядовита и ее водные растворы при больших разбавлениях (1:1000) применяются для дезинфекции. Для лечения кожных и венерических заболеваний применяют мази, содержащие ртуть (II) оксид HgO и ртуть(II) сульфид HgS. Ртуть(I) хлорид Hg2Cl2 (каломель) плохо растворяется в воде и поэтому мало ядовита. Эту соль применяют в ветеринарии как слабительное средство.
Ртуть при обычных условиях — жидкий металл, который способен растворять другие металлы. При этом образуются твердые сплавы — амальгамы. В стоматологии для пломбирования зубов издавна применяли амальгамы серебра и кадмия. Они химически инертны, легко размягчаются при нагревании и поэтому легко формуются.
Жидкая ртуть используется в ряде приборов, применяемых в медицине. Например, для измерения артериального давления, в медицинских термометрах.
Источники ультрафиолетового света — ртутно-кварцевые лампы медицинского назначения содержат газообразную ртуть (пары). При облучении светом этих ламп больничных помещений уничтожаются микроорганизмы, содержащиеся в воздухе. С помощью ультрафиолетовых лучей лечат различные кожные заболевания.
Таким образом, по характеру функционирования и воздействия на организм металлы ПБ-группы можно разделить на жизненнонеобходимый элемент Zn и токсичные примесные элементы Cd и Hg.
Не нашли, что искали? Воспользуйтесь поиском: