
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Алканы. Циклоалканы
Алканы (парафины) – это соединения углерода с водородом, в молекулах которых атомы углерода соединены между собой одинарной связью (предельные углеводороды). Общая формула гомологического ряда алканов СnН2n+2. Радикал, получающийся при отрыве одного атома водорода от молекулы предельного углеводорода, называется алкилож, общая формула алкилов СnН2n+1.
Формулы и названия первых шести алканов (С1–С6) и отвечающих им радикалов:
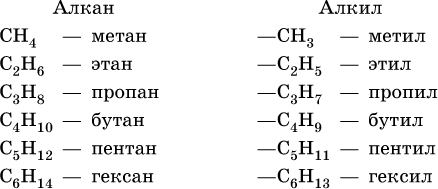
Для радикала С5Н11 использование названия амил не рекомендуется. Для составления названий алканов с разветвленной цепью, например
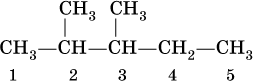
выбирают самую длинную углеродную цепь (в примере – 5 атомов) и получают основу названия (5 – пентан). Нумеруют цепь (от 1 до 5) так, чтобы заместители (–СН3) получили наименьшие номера (2 и 3). В названии арабскими цифрами указывают положение заместителей, а приставками ди – 2, три – 3, тетра – 4 и т. д. – число одинаковых заместителей. Таким образом, в нашем примере алкан должен быть назван 2,3‑диметилпентан.
При наличии разных заместителей их названия расставляют по алфавиту, т. е., например, сначала метил, а затем этил.
Для некоторых разветвленных предельных углеводородов используются, наравне с систематическими, традиционные названия, например, для алканов состава С4Н10 и С5Н12 с формулами:
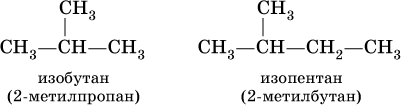
Такие же названия используются для разветвленных радикалов:
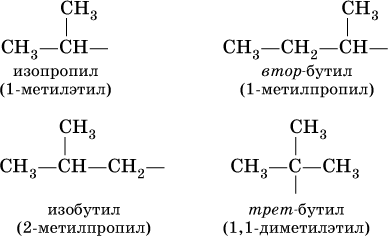
При обычных условиях первые алканы – метан, этан, пропан и бутан (С1–С4) – представляют собой газы без цвета и запаха, малорастворимые в воде. Последующие гомологи (С5–C15) – жидкости (при 20 °C), высшие гомологи (C16 и выше) – твердые вещества.
В алканах атомные орбитали углерода имеют sр3‑гибридизацию; четыре электронных облака атома углерода направлены в вершины тетраэдра под углами 109,5°. Ковалентные связи, образуемые каждым атомом углерода, в алканах малополярны.
Поэтому алканы – сравнительно инертные вещества, вступают только в реакции замещения, протекающие с симметричным (радикальным) разрывом связей С – Н. Эти реакции обычно идут в жестких условиях (высокая температура, освещение). В результате становится возможным замещение водорода на галоген (CI, Br) и нитрогруппу (NO2), например, при обработке метана хлором:
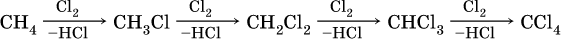
Вторая и последующие стадии реакции протекают легче, чем первая, из‑за смещения электронной плотности к атому хлора:

и увеличения подвижности остающихся атомов водорода. Названия продуктов: СН3Cl – хлорметан, СН2Cl2 – дихлорметан, СНCl3 – трихлорметан (хлороформ), СCl4 – тетрахлорметан (тетрахлорид углерода).
В тех алканах, где кроме первичных есть также вторичные и третичные атомы углерода, замещение обычно протекает с образованием смеси однозамещенных продуктов (т. е. в каждой молекуле замещается один атом водорода), например:
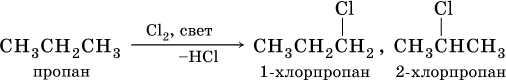
Циклоалканы – предельные углеводороды циклического строения, общая формула гомологического ряда СnH2n (п 
3), формула совпадает с таковой для алкенов. Важнейшие циклоалканы:
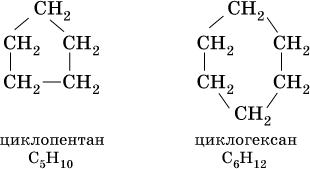
При комнатной температуре С5Н10 и С6Н12 – бесцветные жидкости, малорастворимые в воде. Химические свойства циклоалканов подобны свойствам алканов, например:

Получение: источниками алканов и циклоалканов в промышленности служат нефть, природный газ, каменный уголь. В лаборатории применяют такие способы синтеза алканов:
1) реакция Вюрца – действие натрия на галогенпроизводные углеводородов:

2) каталитическое гидрирование этиленовых углеводородов (катализаторы Pt, Pd, Ni):
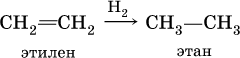
3) сплавление солей карбоновых кислот с гидроксидом натрия:

Циклоалканы синтезируют из дигалогенпроизводных алканов:
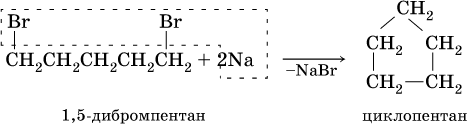
Алканы широко используются как исходное сырье в химической промышленности, моторное топливо (бензин, керосин и др.); циклоалканы применяются в органическом синтезе.
При горении метана выделяется много теплоты:
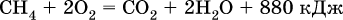
Поэтому его (в виде природного газа) применяют в качестве топлива в быту и в промышленности.
Алкены. Алкадиены
Алкены (олефины) – это углеводороды, в молекулах которых содержатся атомы углерода, соединенные между собой двойной связью (непредельные углеводороды ряда этилена). Простейший представитель – этилен С2Н4, общая формула гомологического ряда этиленовых углеводородов СnН2n (при п ≥ 2).
Систематические названия олефинов производятся от корней названий алканов с заменой суффикса – ан → – ен:

Сохраняются также традиционные названия с заменой суффикса – ан на – илен: С2Н4 – этилен, С3Н6 – пропилен, С4Н8 – бутилен; использование названия амилен для алкена С5Н10 не рекомендуется.
Положение двойной связи С=С в изомерах строения (начиная с алкена С4) указывается цифрой после названия:
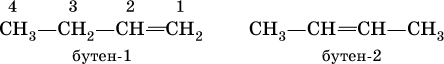
Радикал этилена – этенил СН2=СН – обычно называют винил, пропена – пропенил СН2=СН – СН2 – именуют аллил.
Другой вид изомерии в непредельных углеводородах, помимо структурной изомерии, осуществляется потому, что атомы углерода, образующие двойную связь, находятся в sр2‑гибридном состоянии; σ‑составляющая двойной связи С=С и σ‑связи С – Н лежат в одной плоскости под углом 120° друг к другу, а π‑составляющая двойной связи С=С представляет собой электронное облако, вытянутое в направлении, перпендикулярном плоскости о‑связей. Следствием такого строения алкенов является возможность геометрической изомерии (или цис‑транс‑изомерии) в зависимости от положения заместителей (атомов или радикалов):

(цис – от лат. «рядом, по одну сторону», транс – от лат. «напротив, по разные стороны»).
Алкены С2–С4 при комнатной температуре – бесцветные газы со слабым запахом нефти, малорастворимые в воде; алкены С5–C18 – жидкости, алкены C19 и выше – твердые вещества.
Важнейшие химические свойства алкенов определяются тем, что в силу меньшей прочности π‑связи (по сравнению с σ‑связью) она легко разрывается, в результате чего протекают реакции присоединения и образуются насыщенные органические соединения. Как правило, такие реакции идут в мягких условиях, часто на холоду и в растворителях, например воде, тетрахлорметане СCl4 и др.:
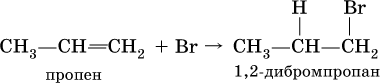
Аналогично протекает взаимодействие алкенов с бромоводородом:

Присоединение галогеноводородов к несимметричным алкенам теоретически может привести к двум продуктам:
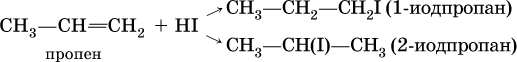
Согласно правилу Марковникова, присоединение галогеноводородов к несимметричным алкенам протекает так, что водород направляется к атому углерода, который уже содержит большее число атомов водорода. В приведенной выше реакции продуктом будет 2‑иодпропан СН3СН(I)СН3.
По правилу Марковникова протекает и реакция гидратации, т. е. реакция присоединения воды в присутствии серной кислоты. Она происходит в две стадии:
а) вначале образуется алкилсерная кислота, т. е. H2SO4 присоединяется к алкену:

б) затем происходит ее необратимый гидролиз:

Алкены обесцвечивают раствор перманганата калия на холоду в нейтральной среде, при этом образуются гликоли (двухатомные спирты):

Алкены способны вступать в реакции полимеризации:
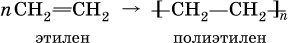
Качественные реакции на алкены – обесцвечивание бромной воды и раствора КMnO4 (уравнения реакций см. выше).
Алкадиены – непредельные углеводороды, в молекулах которых содержатся две связи С=С. Общая формула алкадиенов СnН2n‑2 (n ≥ 3), формула совпадает с таковой для алкинов.
Примеры:

Большое практическое значение имеют сопряженные диены, в молекулах которых связи С=С разделены одинарной связью С – С:

Дивинил и изопрен – традиционные названия.
Дивинил – бесцветный, легко сжижающийся (при ‑4,5 °C) газ, изопрен – низкокипящая (34,1 °C) жидкость.
Алкадиены вступают в те же реакции присоединения, что и алкены. Сопряженные диены имеют особые свойства, в частности, в реакциях присоединения; они образуют продукты 1,4‑присоединения с одной двойной связью посредине:
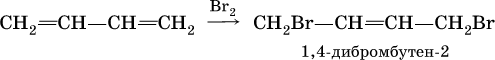
(далее возможно образование 1, 2, 3, 4‑тетрабромбутана).
Алкадиены способны полимеризоваться с образованием каучуков:

Полиметилбутадиеновый каучук – это полимер, существующий в природе (натуральный каучук), а полибутадиеновый каучук получен искусственно (С. В. Лебедев, 1932 г.) и называется синтетическим каучуком.
Получение: для алкенов в промышленности используют метод каталитического дегидрирования алканов:
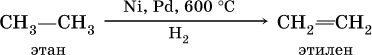
В лаборатории алкены получают:
1) дегидратацией спиртов (отщепление воды от спиртов):
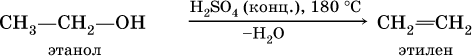
2) дегидрогалогенированиеж – отщеплением галогеноводорода от моногалогенопроизводного под действием спиртового раствора щелочи:

3) дегалогенированиеж – отщеплением галогенов от дигалогенопроизводных, в которых атомы галогена находятся у соседних атомов углерода:

Промышленное получение дивинила:
1) дегидрирование бутана:

2) способ Лебедева – одновременное отщепление воды и водорода от этанола на катализаторе (ZnO/Al2O3):

Алкены используются для органического синтеза, производства пластмасс, искусственного моторного топлива, диеновые углеводороды – исходное сырье в промышленном синтезе каучуков.
Алкины
Алкины – углеводороды с тройной связью C≡C в молекулах (непредельные углеводороды ряда ацетилена). Простейший представитель этого ряда – ацетилен С2Н2, общая формула алкинов CnH2n‑2 (при n ≥ 2).
Названия простейших алкинов:
С2Н2 – этин (традиционно: ацетилен)
С3Н4 – пропин (метилацетилен)
С4Н6 – бутин
Изомеры бутина:

Ацетилен, пропин и бутин‑1 – бесцветные газы при комнатной температуре, бутин‑2 – легкокипящая жидкость, обладает легким «эфирным» запахом.
В алкинах атомные орбитали углерода у тройной связи имеют sp‑ гибридизацию (линейное строение). Наличие двух π‑связей обусловливает их химические свойства, в частности высокую способность к реакциям ступенчатого присоединения водорода, хлора, брома, галогеноводородов, воды:
а)

б)

в)
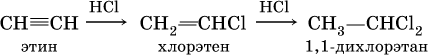
(присоединение НCl к хлорэтену происходит по правилу Марковникова; хлорэтен традиционно называют хлорвинилом или винилхлоридом);
г) реакция Кучерова (гидратация на катализаторе)
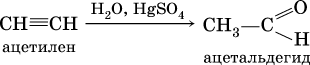
При циклизации ацетилена образуется бензол:
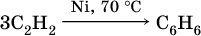
Упомянутый выше хлорвинил способен полимеризоваться:

Поливинилхлорид (ПВХ) – полимер, основа пластмассы, волокон и пленок, применяется в производстве труб, искусственной кожи, электроизоляции, пеноматериалов.
Качественные реакции:
1) на алкины любого строения – обесцвечивание раствора КMnO4, чаще всего происходит разрыв углеродной цепи по месту тройной связи (ср. с алкенами);
2) на алкины с концевой тройной связью – замещение концевого атома водорода на медь (I) с образованием ярко‑красного осадка:
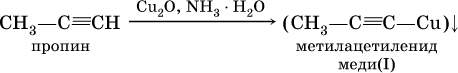
Получение: в промышленности ацетилен ранее получали гидролизом дикарбида (ацетиленида) кальция:

(неприятный «карбидный» запах газа обусловлен примесями, главным образом фосфином РН3).
Современный способ – пиролиз (термическое разложение) метана:
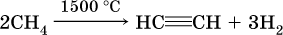
В лаборатории для получения ацетилена и его гомологов используют взаимодействие дигалогенопроизводных алканов со щелочами в спиртовом растворе при нагревании:
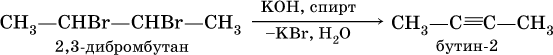
(обязательное условие – атомы галогенов должны находиться при соседних атомах углерода). Эта реакция может проходить в одну стадию (как показано выше), но чаще – в две стадии:
а)
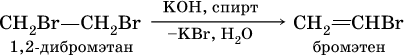
б)

Алкины, особенно ацетилен, используются как исходное сырье в химической промышленности для многих органических синтезов. Кроме того, ацетилен благодаря высокой теплотворной способности сгорания:

применяется для автогенной сварки и резки металлов.
Арены
Арены – это непредельные углеводороды, которые можно рассматривать как производные простейшего из них – бензола С6Н6. Общая формула углеводородов гомологического ряда бензола СnН2n‑6 (при n ≥ 6).
В молекуле бензола все атомы углерода находятся в sр2‑гибридизации, каждый атом углерода соединен в одной плоскости σ‑связями с двумя другими атомами углерода и одним атомом водорода. У атома углерода остается еще облако четвертого валентного электрона, расположенное перпендикулярно плоскости. Эти облака участвуют в образовании π‑связи, причем в молекуле образуются не три отдельные π‑связи (как думали раньше, см. формулу Кекуле, 1865 г.), а единая шестицентровая (С6) π‑связь (все атомы равноценны):
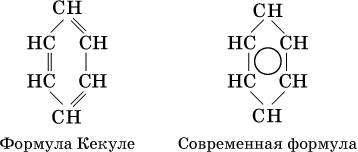
Формула Кекуле часто применяется в тех случаях, когда необходимо более наглядно представить протекание реакции с участием бензольного кольца С6; его изображение:

В обеих формулах атомы С кольца и не участвующие в реакции атомы Н опускаются (для краткости). Некоторые простейшие гомологи бензола:

Радикал бензола С6Н5 называется фенил, радикал толуола С6Н5СН2 – бензил.
Бензол и его ближайшие гомологи – жидкости без цвета, но с характерным запахом, имеют широкий интервал жидкого состояния. Практически не растворяются в воде, но хорошо смешиваются между собой и с другими органическими растворителями. Пар бензола сильно ядовит.
Несмотря на формальную непредельность, бензол отличается высокой устойчивостью к нагреванию и окислению (в гомологах бензола окисляется только боковая цепь). Характерными для бензола являются реакции замещения:
а) нитрование в присутствии концентрированной серной кислоты на холоду:
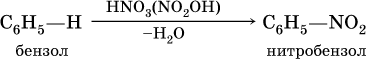
б) галогенирование в присутствии галогенидов железа (III):

в) алкилирование в присутствии хлорида алюминия:

Особый характер ненасыщенности бензола и его гомологов иллюстрируется этими химическими свойствами и называется «ароматическим» характером.
В производных бензола атом или группа, заместившие водород кольца, и само бензольное кольцо влияют друг на друга. По характеру влияния различают:
1) заместители I рода – CI, Br, I, СН3, СnН2n+1, ОН и NH2. Они облегчают реакции дальнейшего замещения и направляют второй заместитель по отношению к себе в орто‑ (о‑, или 2‑) положение и в пара‑ (п ‑, или 4‑) положение [для запоминания: о рто – о коло, п ара – п ротив], например:

2) заместители II рода – NO2, С(Н)O, СООН и CN. Они затрудняют реакции дальнейшего замещения и направляют второй заместитель в мета‑ (м ‑, или 3‑) положение, например:

Очевидно, что существуют два орто‑ положения рядом с первым заместителем X, два мета ‑положения, отделенные от первого заместителя одним углеродом кольца, и лишь одно пара ‑положение через два атома углерода бензольного кольца:
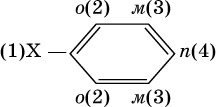
Ранее уже отмечалось, что бензол стоек к окислению даже при действии сильных окислителей. Гомологи бензола с одним боковым радикалом вступают в реакции окисления только за счет радикала; при этом, какова бы ни была его длина, отщепляется вся цепь, кроме ближайшего к кольцу атома углерода (он создает карбоксильную группу):

В жестких условиях бензол вступает в реакции присоединения:

Стирол C6H5–CH=CH2, как этилен, легко полимеризуется:

Полистирол – термопластичная пластмасса (термопласт), прозрачный материал, размягчающийся при температуре выше 80 °C. Используется для изготовления изоляции электропроводов, посуды разового употребления, упаковочной массы (пенопласт).
Получение аренов – ароматизация алифатических и алициклических углеводородов, содержащихся в нефтяных или буроугольных бензиновых фракциях:
1) дегидрирование:
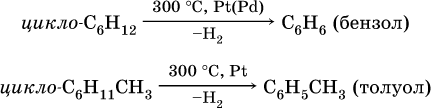
2) дегидроциклизация:

3) тримеризация ацетилена (устаревший способ):

Бензол и его гомологи используются в качестве малополярных растворителей (для каучука, лаковых смол, полимеров), сырье в органическом синтезе.
Не нашли, что искали? Воспользуйтесь поиском: