
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Это также является одной из причин, почему кислородсодержащие кислоты – более сильные окислители, чем их соли.
Деформируемость электронной оболочки влияет и на оптические свойства соединений Поглощение лучей связано с возбуждением внешних электронов. Электронные переходы отвечают тем меньшим энергиям, чем более поляризуема частица. Если частица малополяризуема, то возбуждение требует больших энергий, им отвечаеют ультрафиолетовые лучи. Если частица легко поляризуется, то возбуждение требует квантов небольшой энергии, им отвечает видимая часть спектра. В этом случае вещество окрашено. Так PbI2 имеет жёлтую окраску а CaI2 –бесцветен. Среди сульфидов металлов встречается гораздо больше окрашенных соединений, чем среди оксидов. В ряду PbCl2 - PbBr2- PbI2 окраска соли углубляется.
При образовании ионной связи электрическое поле иона обладает сферической симметрией и поэтому ионная связь не обладает направленностью и насыщаемостью.
Водородная связь
Водородная связь является особым видом химической связи. Известно, что соединения водорода с сильно электроотрицательными неметаллами, такими как F, О, N, имеют аномально высокие температуры кипения. Если в ряду Н2Тe – H2Se – H2S температура кипения закономерно уменьшается, то при переходе от H2S к Н2О наблюдается резкий скачок к увеличению этой температуры. Такая же картина наблюдается и в ряду галогеноводородных кислот. Это свидетельствует о наличии специфического взаимодействия между молекулами Н2О, молекулами HF. Такое взаимодействие должно затруднять отрыв молекул друг от друга, т.е. уменьшать их летучесть, а, следовательно, повышать температуру кипения соответствующих веществ. Вследствие большой разницы в ЭО химические связи H–F, H–O, H–N сильно поляризованы. Поэтому атом водорода имеет положительный эффективный заряд (δ+), а на атомах F, O и N находится избыток электронной плотности, и они заряжены отрицательно (δ-). Вследствие кулоновского притяжения происходит взаимодействие положительно заряженного атома водорода одной молекулы с электроотрицательным атомом другой молекулы. Из-за очень малого размера положительно поляризованного атома водорода и его способности глубоко внедряться в оболочку соседнего (ковалентно с ним не связанного отрицательно поляризованного атома) образуется водородная связь. Благодаря этому молекулы притягиваются друг к другу (жирными точками обозначены водородные связи). Водородная связь весьма распространена и играет важную роль в процессах растворения кристаллизации электролитической диссоциации и других физико-химических процессах.
Молекулы фторида водорода HF в твёрдом жидком и даже в газовом состоянии ассоциированы в зигзаобразные
цепочки (рис.15).

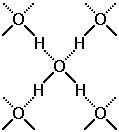
Рис. 15 Водородные связив HF Рис. 16 Водородные связи в Н2О
Молекула воды может образовывать четыре водородные связи так как имеет два атома водорода и две несвязывающие электронные пары(рис.16).
Энергия водородной связи (21–29 кДж/моль или 5–7 ккал/моль) приблизительно в 10 раз меньше энергии обычной химической связи. И тем не менее, водородная связь обусловливает существование в парах димерных молекул (Н2О)2, (HF)2 и муравьиной кислоты. В ряду сочетаний атомов НF, HO, HN, HCl, HS энергия водородной связи падает. Она также уменьшается с повышением температуры, поэтому вещества в парообразном состоянии проявляют водородную связь лишь в незначительной степени; она характерна для веществ в жидком и твердом состояниях. Такие вещества как вода, лед, жидкий аммиак, органические кислоты, спирты и фенолы, ассоциированы в димеры, тримеры и полимеры. В жидком состоянии наиболее устойчивы димеры.
Водородные связи приблизительно в 20 раз менее прочные, чем ковалентные, но именно они заставляют воду быть жидкостью или льдом (а не газом) в обычных условиях. Водородные связи разрушаются только тогда, когда жидкая вода переходит в пар. При температурах выше 0 °С (но ниже температуры кипения) вода уже не имеет такую упорядоченную межмолекулярную структуру. Поэтому в жидкой воде молекулы связаны между собой лишь в отдельные агрегаты из нескольких молекул. Эти агрегаты могут свободно двигаться рядом друг с другом, образуя подвижную жидкость. Но при понижении температуры упорядоченность становится все больше и больше, а агрегаты – все крупнее. Наконец, образуется лед, который имеет именно такую упорядоченную структуру. В кристалле льда между молекулами остаются пустоты. Объем этих пустот больше, чем размер отдельной молекулы Н2О. Поэтому лед имеет меньшую плотность, чем жидкая вода и плавает на поверхности воды. Большинство же других веществ при замерзании увеличивает свою плотность.
Энергия связи
Важное значение имеет энергетическая характеристика химической связи. При образовании химической связи общая энергия системы (молекулы) меньше энергии составных частей (атомов), т.е. Е(AB)<Е(А)+Е(B).
Энергия связи – это энергия, которая выделяется при образовании молекулы из атомов. Энергию связи обычно выражают в кДж/моль (или ккал/моль). Это одна из важнейших характеристик химической связи. Более устойчива та система, которая содержит меньше энергии. Известно, например, что атомы водорода стремятся объединиться в молекулу. Это означает, что система, состоящая из молекул Н2 содержит меньше энергии, чем система, состоящая из такого же числа атомов Н, но не объединенных в молекулы.
Для двухатомных молекул энергия связи равна энергии диссоциации. Для многоатомных молекул с одним типом связи средняя энергия связи равна 1/n части распада молекулы на атомы. Энергия распада метана на атомы равна 1649 кДж/моль. В молекуле метана имеются четыре равноценные связи С-Н поэтому средняя энергия такой связи равна Ес-н = 1649/4 = 412 кДж/моль. оль.
Таблица 3 Длина и энергия разрыва связей
Не нашли, что искали? Воспользуйтесь поиском: