
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Изотерма адсорбции Лангмюра
Фундаментальным вкладом в учение об адсорбции явилось теория мономолекулярной адсорбции Ленгмюра. Основные положения:
1) адсорбция локализована (молекулы не перемешиваются по поверхности) на отдельных адсобционных центрах, каждый из которых взаимодействует только с одной молекулой адсорбата – образуется мономолекулярный слой;
2) адсорбционные центры энергетически эквивалентны – поверхность адсорбента эквипотенциальна;
3) адсорбционные молекулы не взаимодействуют друг с другом.
Теория Лангмюра позволяет учесть наиболее сильные отклонения от закона Генри, связанные с ограниченностью адсорбционного объема или поверхности адсорбента. Ограниченность этого параметра приводит к адсорбционному насыщению поверхности адсорбента по мере увеличения концентрации распределяемого вещества. Примем, что при адсорбции происходит квазихимическая реакция между распределяемым компонентом и адсорбционными центрами поверхности:
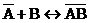 , (5.7)
, (5.7)
где  – адсорбционные центры поверхности; В – распределяемое вещество;
– адсорбционные центры поверхности; В – распределяемое вещество;  – образующийся комплекс на поверхности.
– образующийся комплекс на поверхности.
По мере увеличения концентрации вещества В реакция сдвигается в сторону образования комплекса и свободных адсорбционных центров становится меньше. Константа адсорбционного равновесия
 . (5.8)
. (5.8)
В этом соотношении

и
 , (5.9)
, (5.9)
где А – величина адсорбции;  – емкость адсорбционного монослоя;
– емкость адсорбционного монослоя;  –число оставшихся свободными адсорбционных центров, приходящихся на единицу площади поверхности или на единицу массы адсорбента.
–число оставшихся свободными адсорбционных центров, приходящихся на единицу площади поверхности или на единицу массы адсорбента.
Подставляя уравнение (5.8) в уравнение (5.9), получаем:

или
 .
.
Окончательно имеем
 . (5.10)
. (5.10)
Выражение (5.10) называется уравнением изотермы Лангмюра. Для газов и паров концентрации можно заменять парциальными давлениями.
Не нашли, что искали? Воспользуйтесь поиском: