
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Примеры решения задач.
Задача 1. Напишите электронную формулу атома меди. Сколько электронов находится на d-подуровне предпоследнего электронного слоя? К какому электронному семейству относится элемент?
Решение: атом Cu имеет порядковый номер 29. Следовательно, в его оболочке содержится 29 электронов. В электронной формуле распределяем их по подуровням согласно порядку заполнения (в соответствии с правилами Клечковского) и учитывая емкость подуровней: Cu: 1s22s22p63s23p63d94s2 При этом порядок заполнения подуровней следующий: 1s ® 2s ® 2p ® 3s ® 3p ® 4s ® 3d. Последний электрон располагается на 3d-подуровне, значит, медь относится к семейству d-элементов. Но электронная формула атома меди имеет вид: Cu 1s2 2s2 2p6 3s2 3p6 3d10 4s1, т.е. один из двух 4s-электронов “проваливается” на 3d-подуровень. На d-подуровне предпоследнего (3-го) слоя находится 10 электронов.
Ответ: 10, d.
Задача 2. Атом какого элемента имеет электронную конфигурацию 1s22s22p63s23p63d104s24p64d105s25p1?
Решение: количество электронов в оболочке нейтрального атома составляет 49. Поэтому его заряд ядра и, следовательно, порядковый номер, также равны 49. В периодической системе Д.И.Менделеева находим, что этот элемент – индий.
Ответ: In.
Задача 3. Напишите электронную формулу элемента, находящегося под № 43. К какому электронному семейству относится элемент?
Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
Решение: атом Ru (рутений) имеет порядковый номер 44. Следовательно, в его оболочке содержится 44 электрона. В электронной формуле распределяем их по подуровням согласно порядку заполнения (в соответствии с правилами Клечковского) и учитывая емкость подуровней: Ru: 1s22s22p63s23p63d104s2 4p6 4d65s2
При этом порядок заполнения подуровней следующий: 1s ® 2s ® 2p ® 3s ® 3p ® 4s ® 3d ® 4p ® 5s ® 4d.Последний электрон располагается на 4d-подуровне, значит, рутений относится к семейству d-элементов. Следовательно валентными электронами будут 4d65s2. В невозбужденном состоянии (которое называется также основным состоянием) атом рутения имеет четыре неспаренных электрона, однако для него характерны соединения, в которых он образует шесть ковалентных связей. Это оказывается возможным в результате возбуждения атома. При этом один из s-электронов последнего пятого уровня переходит на p-подуровень:
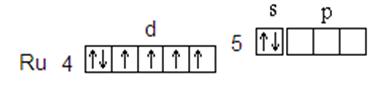
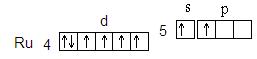
КОНТРОЛЬНЫЕ ВОПРОСЫ
61. Напишите электронные формулы атомов элементов с порядковыми номерами 9 и 28. Покажите распределение электронов этих атомов по квантовым ячейкам. К какому электронному семейству относится каждый из этих элементов?
62. Напишите электронные формулы атомов элементов с порядковыми номерами 16 и 26. Покажите распределение электронов этих атомов по квантовым ячейкам. К какому электронному семейству относится каждый из этих элементов?
63. Напишите электронные формулы атомов элементов с порядковыми номерами 25 и 34. Покажите распределение электронов этих атомов по квантовым ячейкам. К какому электронному семейству относится каждый из этих элементов?
64. Напишите электронную формулу атома цинка. Сколько электронов находится на последнем s-подуровне? К какому электронному семейству относится элемент?
65. Напишите электронную формулу элемента, у которого на 3d-подуровне находятся 3 электрона. Что это за элемент?
66. Напишите электронную формулу элемента с порядковым номером 47. Укажите, сколько электронов у него на d-подуровне. К какому электронному семейству он относится?
67. Напишите электронную формулу атома брома. Сколько электронов находится на последнем р-подуровне? К какому электронному семейству относится элемент?
68. Напишите электронную формулу атома кадмия. Сколько электронов находится на последнем d-подуровне? К какому электронному семейству относится элемент?
69. Напишите электронную формулу элемента, находящегося под № 34. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
70. Напишите электронную формулу элемента, находящегося под № 42. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
71. Напишите электронную формулу элемента, находящегося под № 24. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
72. Напишите электронную формулу элемента, находящегося под № 33. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
73. Напишите электронную формулу элемента, находящегося под № 82. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
74. Напишите электронную формулу элемента, находящегося под № 35. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
75. Напишите электронную формулу элемента, находящегося под № 53. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
76. Напишите электронную формулу элемента, находящегося под № 38. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
77. Напишите электронную формулу элемента, находящегося под № 26. Распределите валентные электроны по атомным орбиталям
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
78. Напишите электронную формулу элемента, находящегося под № 27. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
79. Напишите электронную формулу элемента, находящегося под № 43. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
80. Напишите электронную формулу элемента, находящегося под № 74. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
81. Напишите электронную формулу элемента, находящегося под № 39. Распределите валентные электроны по атомным орбиталям:
а) в нормальном состоянии атома,
б) в возбуждённом состоянии атома, если возбуждение возможно.
82. Атом какого элемента имеет электронную конфигурацию: 1s22s22p63s23p63d104s1?
83. Атом какого элемента имеет электронную конфигурацию 1s22s22p63s23p63d24s2?
84. Напишите электронную формулу элемента, у которого на 3d-подуровне находятся 3 электрона. Что это за элемент?
85. Напишите электронную формулу элемента, у которого на 4d-подуровне находятся 5 электронов. Что это за элемент?
86. Напишите электронную формулу элемента, у которого на 3d-подуровне находятся 9 электронов. Что это за элемент?
87. Напишите электронную формулу элемента, у которого на 5d-подуровне находятся 2 электрона. Что это за элемент?
88. Напишите электронные формулы атомов элементов с порядковыми номерами 15 и 28. Покажите распределение электронов этих атомов по квантовым ячейкам. Чему равен максимальный спин р -электронов у атомов первого и d – электронов у атомов второго элемента?
89. Напишите электронные формулы атомов элементов с порядковыми номерами 21 и 23. Покажите распределение электронов этих атомов по квантовым ячейкам. Сколько свободных d – орбиталей в атомах этих элементов?
90. Напишите электронные формулы атомов элементов с порядковыми номерами 14 и 40. Покажите распределение электронов этих атомов по квантовым ячейкам. Сколько свободных d – орбиталей у атомов последнего элемента?
Не нашли, что искали? Воспользуйтесь поиском: