
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Зависимость скорости реакции от природы реагирующих веществ
Влияние природы реагирующих веществ определяется их атомным составом, пространственным строением и свойствами молекул. Скорость реакции определяется скоростью разрыва одних химических связей и образования других. При этом изменяется потенциальная энергия реагирующих частиц и всей системы.
Для того, чтобы произошла реакция, необходимо преодолеть отталкивание электронных оболочек молекул, разорвать связи между атомами в молекулах исходных веществ. На это нужно затратить определенную энергию. Если сталкивающиеся молекулы не обладают такой энергией, то столкновение будет неэффективным и новые молекулы не образуются. Если молекулы обладают достаточной энергией, при их столкновении происходит перестройка атомов и образуются молекулы нового вещества. Такой запас энергии называется энергией активации данной реакции (Еа) измеряется в кДж/моль. Молекулы, обладающие такой энергией, называются активными молекулами.
Для различных реакций энергия активации различна. Именно этим и определяется влияние на скорость реакции природы реагирующих веществ. Если энергия активации очень мала, то большая часть столкновений будут эффективными и скорость такой реакции велика. Например, ионные реакции протекают практически мгновенно, так как обладают очень низкой Еа.
Реакции с очень большой энергией активации протекают очень медленно. Например, реакция синтеза аммиака при обычных температурах:
3 H2(г) + N2(г) = 2 NH3(г)
Реакции начинаются с того, что разрываются старые связи между атомами в молекулах исходных веществ. При этом вещества переходят в неустойчивое промежуточное состояние, характеризующееся большим запасом энергии. Это состояние называется активированным комплексом. Именно для его образования необходима энергия активация. Активированный комплекс неустойчив, существует очень короткое время. Он распадается с образованием исходных веществ или продуктов реакции, при этом выделяется энергия.
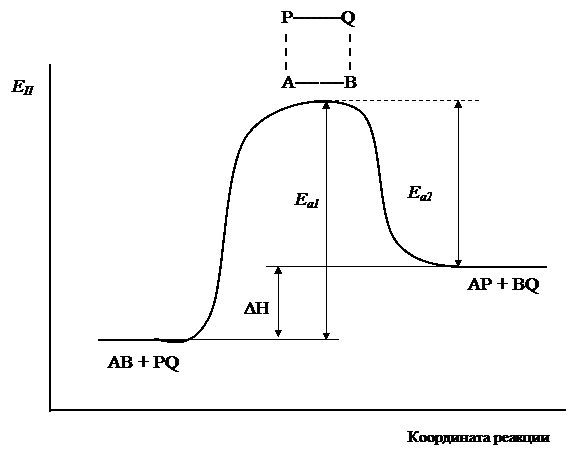 На рис.7 показано изменение потенциальной энергии системы при взаимодействии исходных веществ АВ и PQ. В ходе реакции образуется промежуточный активированный комплекс АВPQ. Энергия активации прямой реакции Еа1 определяется как разность между энергией активированного комплекса и потенциальной энергией исходных веществ. Энергия активации обратной реакции Еа2 равна разности энергии активированного комплекса и потенциальной энергией продуктов реакции. Очевидно, что тепловой эффект реакции ΔH определяется как разность энергий активации прямой и обратной реакций, или разность значений потенциальной энергии системы в начальном и конечном состоянии.
На рис.7 показано изменение потенциальной энергии системы при взаимодействии исходных веществ АВ и PQ. В ходе реакции образуется промежуточный активированный комплекс АВPQ. Энергия активации прямой реакции Еа1 определяется как разность между энергией активированного комплекса и потенциальной энергией исходных веществ. Энергия активации обратной реакции Еа2 равна разности энергии активированного комплекса и потенциальной энергией продуктов реакции. Очевидно, что тепловой эффект реакции ΔH определяется как разность энергий активации прямой и обратной реакций, или разность значений потенциальной энергии системы в начальном и конечном состоянии.
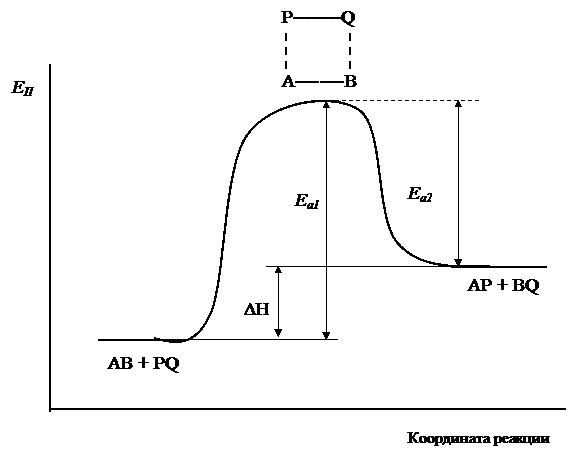 |
Рис.7. Изменение потенциальной энергии системы при взаимодействии веществ АВ и PQ
Пример №1: По энергетической диаграмме реакции А + Б = АБ определите тепловой эффект реакции Δ H и энергию активации Еа ..
 Решение. Потенциальная энергия исходных веществ (А + В) 100 кДж, продуктов реакции 200 кДж, энергия активированного комплекса 250 кДж. Энергия активации прямой реакции
Решение. Потенциальная энергия исходных веществ (А + В) 100 кДж, продуктов реакции 200 кДж, энергия активированного комплекса 250 кДж. Энергия активации прямой реакции
Еа .=(250-100)кДж=50 кДж.
Тепловой эффект реакции равен разности значений потенциальной энергии продуктов и исходных веществ: ΔH = (200 – 100) = 100кДж
Не нашли, что искали? Воспользуйтесь поиском: