
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Решение типовых задач
Задача 1. В 80 г воды растворено 4 г соли. Определить процентную концентрацию раствора и растворимость этой соли.
Решение. Находим массу раствора: 80+4=84г.
1. Определение массовой доли:
| в 84 г содержится 4 г соли в 100 «х « | 
|
2. Определение растворимости соли:
| 80 г воды растворяют 4 г соли 100 «х « | 
|
Задача 2. Вычислить молярность и моляльную долю водного раствора H2SO4, плотность которого при 20 оС равна 1,303 г/см3.
Решение. По справочной таблице (прил.1) находим, что такой раствор содержит 40 % H2SO4; литр этого раствора весит 1303 г (1,303·1000). Для вычисления содержания H2SO4 составляем пропорцию и находим х:
| 100 г раствора содержат 40 г H2SO4 1303 «х H2SO4 |  г/л. г/л.
|
Для вычисления моляльной доли раствора нужно вычислить число граммов H2SO4 в 1000 г воды (растворителя). Поскольку дан 40 %-ный раствор, 40 г H2SO4 содержится в 60 г воды. Отсюда составляем пропорцию и находим х:
| 60 г воды содержат 40 г H2SO4 1000 «х H2SO4 |  г/кг. г/кг.
|
Так как 1 моль H2SO4 равен 98 г и в 1000 г (1 кг) раствора содержится 666,7 г H2SO4, то моляльная доля раствора равна: 666,7/98=6,8 моль/кг.
Задача 3. В 250 мл раствора гидроксида кальция содержится 3,705 г Са(ОН)2. Вычислить молярность этого раствора.
Решение. Сначала вычислим, сколько граммов содержится
1 л раствора:
| 3,075 г Са(ОН)2 содержится в 250 мл х Са(ОН)2 «1000 « | 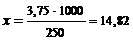 г/л г/л
|
Молярность определяем из следующего соотношения:
| 74,10 г/л – 1 моль 14,82 г/л – х |  М. М.
|
Задача 4. Вычислите молярную долю HCl в растворе соляной кислоты, содержащем 36% HCl.
Решение. Допустим, что имеет 100 г раствора. Тогда в растворе должно содержаться 36 г HCl и 64 г Н2О.
| 1М раствора содержит 36,5 г HCl х М«36 г HCl | 
|
| 1М раствора содержит 18 г H2О х М«64 г H2О | 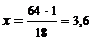 М Н2О М Н2О
|
Молярная доля вычисляется по формуле (3.5)
Х НС1= 
Не нашли, что искали? Воспользуйтесь поиском: