
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Теоретические пояснения. Химическим эквивалентом (Э) называется реальная или условная частица вещества, которая может замещать
Химическим эквивалентом (Э) называется реальная или условная частица вещества, которая может замещать, присоединять, высвобождать или быть каким-либо другим способом эквивалентна (равноценна) одному иону водорода в кислотно-основных и обменных реакциях, либо одному электрону в окислительно-восстановительных реакциях.
Реальные частицы - это атомы, ионы, молекулы и т.д., а условные частицы - это, например, 1/2 (H2SO4), 1/4(С), 1/3(Fe3+).
В общем случае эквивалент любого вещества X может быть записан в виде ЭХ =1/z(X), где z - число эквивалентности, или эквивалентное число, которое всегда > 1. Оно показывает, сколько эквивалентов содержится в одной формульной единице вещества.
Для данного вещества z находится по конкретной реакции. В окислительно-восстановительных процессах z определяется числом электронов, принятых или отданных одной формульной единицей вещества, например, в реакции:
Mg + 2HCl → MgCl2 + H2
Z(Mg)=2, т.к. магний в ходе окислительно-восстановительной реакции отдает 2 электрона, а ЭMg =½ (Mg). В обменных процессах Z определяется стехиометрией и равно знаменателю правильной дроби, которая получается при делении коэффициента перед веществом на самый большой коэффициент в реакции:
АI2O3 + 6HCI =2AICI3 +3H2O
Z (АI2O3) = 6, т.к. при делении коэффициента перед АI2O3 на самый большой коэффициент в реакции - 6, получается правильная дробь  , знаменатель которой равен 6; Z(HCI) = 1, т.к. при делении коэффициента перед HCI на самый большой коэффициент в реакции - 6, получается 1.
, знаменатель которой равен 6; Z(HCI) = 1, т.к. при делении коэффициента перед HCI на самый большой коэффициент в реакции - 6, получается 1.
Когда речь не идет о конкретной реакции, при определении z для сложных веществ можно воспользоваться следующими правилами:
1) для оксидов z равно числу атомов элемента, умноженному на степень окисления элемента;
2) для кислот z равно основности кислоты;
3) для оснований z равно кислотности основания;
4) для солей z равно числу катионов металла, умноженному на заряд катиона.
Количество вещества эквивалента обозначается vЭ,единица измерения - моль. Один моль эквивалента вещества содержит 6,022-1023 эквивалентов.
Молярная масса эквивалента MЭ - это масса 1 моль эквивалентов вещества, измеряется в г/моль.
Связь между молярной массой эквивалента, количеством вещества эквивалента, массой и молярной массой вещества выражается соотношениями:
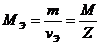
 (4.1)
(4.1)
Экспериментальное определение молярной массы химического эквивалента цинка в данной работе основано на законе эквивалентов:
Вещества реагируют друг с другом в равных количествах эквивалентов 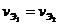 . (4.2)
. (4.2)
Из закона эквивалентов следует, что массы реагирующих друг с другом веществ, а также массы продуктов реакции относятся друг к другу как молярные массы их эквивалентов:
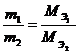 (4.3)
(4.3)
Если вещество находится в газообразном состоянии то для него справедливы соотношения: 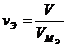 ;
; 
 ; где
; где  – количество вещества эквивалента; V – объем газообразного вещества в данных условиях;
– количество вещества эквивалента; V – объем газообразного вещества в данных условиях; 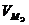 – молярный объем эквивалента вещества в тех же условиях; VM – молярный объем вещества; Z – число эквивалентности.
– молярный объем эквивалента вещества в тех же условиях; VM – молярный объем вещества; Z – число эквивалентности.
На основе закона эквивалентов можно вывести следующие формулы для вычисления молярных масс эквивалентов сложных веществ:
Моксида
M1/z оксида = _______________________________________, (4.4)
Число атомов элемента · Валентность элемента
Mкислоты
М1/z кислоты = _____________________, (4.5)
Основность кислоты
Моснования
М1/z основания = ____________________, (4.6)
Кислотность основания
Мсоли
М1/z соли = ______________________________________. (4.7)
Число атомов металла · Валентность металла
Не нашли, что искали? Воспользуйтесь поиском: