
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Теоретические пояснения. Концентрация раствора- это относительное содержание растворенного вещества в растворе
Концентрация раствора- это относительное содержание растворенного вещества в растворе. Для выражения концентрации растворов существует два способа.
I. долевой способ:
а) массовая доля вещества ω, безразмерная величина или выражается в процентах, вычисляют по формуле
 % (7.1)
% (7.1)
где m(в-ва), масса вещества, г;
m(р-ра), масса раствора, г.
б) мольная доля χ, величина безразмерная или выражается в процентах, вычисляют по формуле
 % (7.2)
% (7.2)
где ν(в-ва), количество вещества, моль;
ν1 + ν2 +…, сумма количеств всех веществ в растворе, моль.
в) объемная доля φ, величина безразмерная или выражается в процентах, вычисляют по формуле
 % (7.3)
% (7.3)
где V(в-ва), объем вещества, л;
V(смеси), объем смеси, л.
II. концентрационный способ:
а) молярная концентрация CM, моль/л, вычисляют по формуле
 (7.4)
(7.4)
где ν(в-ва), количество вещества, моль;
V(р-ра), объем раствора, л.
б) нормальная концентрация СН, моль/л, вычисляют по формуле
 (7.5) или
(7.5) или 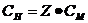 (7.6)
(7.6)
где ν(экв), количество вещества эквивалента, моль;
V(р-ра), объем раствора, л;
Z, фактор эквивалентности.
в) моляльная концентрация Сb, моль/кг, вычисляют по формуле
 (7.7)
(7.7)
где ν(в-ва), количество вещества, моль;
m(р-ля), масса растворителя, кг.
г) титр Т, г/мл, вычисляют по формуле
 (7.8)
(7.8)
где m(в-ва), масса вещества, г;
V(р-ра), объем раствора, мл.
Обычно вызывает затруднение изучение свойств растворов (осмос и осмотическое давление, понижение давления насыщенного пара, понижение температуры кристаллизации и повышение температуры кипения растворов), а также свойств растворенных веществ — растворимости и произведения растворимости.
Осмос- это односторонняя диффузия веществ из растворов через полупроницаемую мембрану, разделяющую раствор и чистый растворитель или два раствора различной концентрации.
В системе растворитель-раствор молекулы растворителя могут перемещаться через перегородку в обоих направлениях. Но число молекул растворителя, переходящих в раствор в единицу времени, больше числа молекул, перемещающихся из раствора в растворитель.
Давление, которое надо приложить, чтобы скорости обоих процессов были равными, называют осмотическим.
Растворы, характеризующиеся одинаковым осмотическим давлением, называются изотоническими.
Осмотическое давление определяют согласно закону Вант-Гоффа
 , (7.9)
, (7.9)
где ν, количество вещества, моль;
R, газовая постоянная, равная 8,314 Дж/(моль·К);
Т, абсолютная температура, К;
V, объем раствора, м3
Относительное понижение давления пара растворителя над раствором согласно закону Рауля выражается соотношением
 , (7.10)
, (7.10)
где P0, давление пара над чистым растворителем;
P, давление пара растворителя над раствором;
n, количество растворенного вещества, моль;
N, количество растворителя, моль.
Повышение температуры кипения и понижение температуры замерзания растворов по сравнению с чистым растворителем, согласно закону Рауля, пропорциональны моляльной концентрации растворенного вещества неэлектролита
∆Т= КСb (7.11)
где Сb, моляльная концентрация, моль/кг;
К, коэффициент пропорциональности.
В случае повышения температуры кипения раствора К называется эбулиоскопической константой, в случае понижения температуры замерзания- криоскопической константой. Эти константы, численно различные для одного и того же растворителя, характеризуют повышение температуры кипения и понижение температуры замерзания одномоляльного раствора, т.е. при растворении 1 моль нелетучего неэлектролита в 1000 г растворителя.
Растворимость S показывает, сколько граммов вещества может раствориться в 100 г воды при данной температуре. Растворимость твердых веществ с ростом температуры, как правило, возрастает, а для газообразных веществ – уменьшается.
Для перехода от массы раствора к его объему и наоборот нужно знать величину плотности. Плотность выражается в г/см3 (г/мл), кг/м3, г/л, и др. Для приближенного и быстрого определения плотности служит ареометр или денсиметр (см. рис. 7.1).
 Ареометр представляет собой поплавок с дробью и узкой трубкой. На трубке имеется шкала, проградуированная в единицах плотности. Ареометр погружается в различные жидкости или растворы различной концентрации на разную глубину. При этом вытесняются различные объемы жидкостей, но массы их всегда одинаковы, они равны массе ареометра.
Ареометр представляет собой поплавок с дробью и узкой трубкой. На трубке имеется шкала, проградуированная в единицах плотности. Ареометр погружается в различные жидкости или растворы различной концентрации на разную глубину. При этом вытесняются различные объемы жидкостей, но массы их всегда одинаковы, они равны массе ареометра.
В состоянии равновесия выталкивающая сила, действующая на ареометр, уравновешивается силой тяжести: Fвыт.= mg или рж·V·g = mg, отсюда V = m/рж,. Итак, объем вытесненной жидкости (или глубина погружения) обратно пропорционален плотности жидкости рж. На этом и основано измерение плотности ареометром.
Жидкость наливают в чистый цилиндр. Из набора выбирают ареометр, который погружается на такую глубину, чтобы уровень жидкости в цилиндре находился в пределах шкалы ареометра. Ареометр не должен касаться дна и стенок цилиндра. Показания следует снимать по нижнему краю мениска в случае прозрачной жидкости, и по верхнему - в случае непрозрачной. Зная плотность раствора, по специальным таблицам (см. табл. 7.1) можно определить массовую долю раствора, и наоборот, зная концентрацию раствора, определить его плотность.
Рис.7.1 Определение плотности жидкости при помощи ареометра
Таблица 7.1- Массовая доля (ω%) и плотность (р) растворов солей при 20°C
| ω% | р, г/см3 | |||||
| СаСI2 | NaCI | CuSO4 | KCI | Na2СO3 | ВаСI2 | |
| 1,0070 | 1,0053 | 1,009 | 1,0046 | 1,009 | - | |
| 1,0148 | 1,0125 | 1,019 | 1,0110 | 1,019 | 1,016 | |
| 1,0316 | 1,0226 | 1,040 | 1,0239 | 1,040 | 1,034 | |
| 1,0486 | 1,0413 | 1,062 | 1,0369 | 1,061 | 1,053 | |
| 1,0659 | 1,0559 | 1,084 | 1,0500 | 1,082 | 1,072 | |
| 1,0835 | 1,0707 | 1,107 | 1,0633 | 1,103 | 1,092 | |
| 1,1015 | 1,0857 | 1,131 | 1,0768 | 1,085 | 1,113 | |
| 1,1198 | 1,1009 | 1,155 | 1,0905 | 1,101 | 1,134 |
Если в таблице отсутствует необходимое значение величины, то применяют метод интерполяции (нахождение промежуточного значения величины по известным крайним значениям). В данном случае применяется линейная интерполяция: считается, что в узких интервалах зависимость между плотностью и концентрацией линейна. Это является, в некоторой степени, приближением. В действительности возможны и отклонения от линейности.
Допустим, нужно определить плотность 2,3% раствора хлорида натрия. Такой концентрации в таблице нет. Ближайшие значения массовой доли - 2% и 4%, им соответствуют плотности растворов 1,0125 г/см3 и 1,0226 г/см3. Следовательно, при изменении концентрации на 2%, плотность раствора изменится на 1,0226-1,0125=0,0101 г/см3. Составив пропорцию, найдем, как изменится плотность при изменении концентрации на 0,3%:
2% — 0,0101 г/см3
0,3% — х г/см3
Из пропорции х=0,0015 г/см3. Прибавив эту величину к значению плотности 2%- ного раствора, получим плотность 2,3%- ного раствора: 1,0125+0,0015=1,0140 г/см3.
Не нашли, что искали? Воспользуйтесь поиском: