
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
ЭНТРОПИЯ. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ. УСЛОВИЯ ПРОТЕКАНИЯ ХИМИЧЕСКИ ПРОЦЕССОВ. УСЛОВИЯ РАВНОВЕСИЯ
126. Подсчитав ∆S0 реакций, определите, какая из двух реакций термодинамически возможна:
FeO + CO = Fe + CO2; FeO + H2 = Fe + H2O(г).
127. По известным значениям стандартной энтропии для приведенных ниже реакций определите, какие из этих реакций являются термодинамически возможными в изолированой системе:
а) CS2(ж) + 3O2(г) = CO2(г) + 2SO2(г);
б) А12(SO4)3(к) = А12О3(к) + 3SO3(г).
128. Энтропия реакции зависит не столько от химической индивидуальности реагентов и продуктов, сколько от агрегатного состояния веществ и их количеств, участвующих в реакции. Укажите, какое значение (>0,<0) имеет стандартная энтропия реакций:
а) 2О3(г) = 2О2(г);
б) SO2(г) + 2H2S(г) = 2S(т) + 2Н2О(ж);
в) J2(г) = 2J(г).
Подтвердите Ваш ответ расчетом с использованием справочных данных.
129. В изолированной системе протекают следующие процессы:
3Fe(т) + 4Н2О(г) = 4Н2(г) + Fe3O4.
На основании определенного значения ∆S укажите направление реакции.
130. Вычислите значение ∆Н  , ∆G
, ∆G  , ∆S
, ∆S  для процесса МеСО3(к)
для процесса МеСО3(к)  МеО(к) + СО2(г) и составьте ряд термической стабильности карбонатов MgCO3, BaCO3, CaCO3. Как влияет на течение этих процессов температура?
МеО(к) + СО2(г) и составьте ряд термической стабильности карбонатов MgCO3, BaCO3, CaCO3. Как влияет на течение этих процессов температура?
131. В каком направлении будет протекать реакция:
Fe2O3(k) + 3H2(г) = 3H2O(г) + Fe(k).
132. Как ведет себя магний в атмосфере кислорода, углекислого газа, паров воды? Ответ подтвердите расчетами.
133. Вычислите ∆Н0, ∆S0, ∆G  реакции, протекающей по уравнению
реакции, протекающей по уравнению
TiO2(k) + 2C(k) = Ti(k) + 2CO(г).
Возможна ли реакция восстановления TiО2 углеродом при температурах 1000 и 3000 К?
134. Определите, при какой температуре начинается реакция восстановления Fe3O4, протекающая по уравнению: Fe3O4(k) + 4CO(г) = 3Fe(k) + 4CO2(г);
∆Н = +34,55 кДж.
135. Тепловой эффект и изменение энергии Гиббса при 250С для реакции
СО2(г) + 4Н2(г) = СН4(г) + 2Н2О(ж)
соответственно равны –253,02 кДж 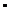 моль–1; –130,1 кДж
моль–1; –130,1 кДж 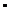 моль–1. Определите ∆S0 для этой реакции.
моль–1. Определите ∆S0 для этой реакции.
136. Установите возможность или невозможность самопроизвольного протекания реакции при температуре 298 К: СО2(г)  СО(г) + 1/2O2(г).
СО(г) + 1/2O2(г).
137. Установите возможность самопроизвольного протекания реакции ВаО + СO2 = BaСO3 при температуре 298 К.
138. Установите возможность самопроизвольной реакции разложения сульфатных соединений CaSO4 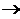 CaO + SO3; CaSO4
CaO + SO3; CaSO4  CaO + SO2 + 1/2O2.
CaO + SO2 + 1/2O2.
139. Образование какого оксида СО или СО2 - наиболее вероятно при сгорании угля. При ответе используйте данные ∆Н0, ∆S0, ∆G0.
140. Вычислите ∆G  окисления аммиака кислородом с образованием NO или N2. Какой из этих процессов наиболее вероятен при сжигании аммиака?
окисления аммиака кислородом с образованием NO или N2. Какой из этих процессов наиболее вероятен при сжигании аммиака?
141. Определите S0,  в следующих реакциях:
в следующих реакциях:
2С(ГРАФИТ) + Н2 (Г)  С2Н2 (Г),
С2Н2 (Г),
А1 (К) + Сr2O3 (К)  Cr + A12O3 (К),
Cr + A12O3 (К),
2С(ГРАФИТ) + СО2 (Г)  2СО2 (Г).
2СО2 (Г).
Возможны ли реакции при стандартных условиях?
142. Подсчитав ∆S0, ∆G0 реакций, определите, какая из двух реакций термодинамически возможна:
FeO + CO = Fe + CO2, FeO + H2 = Fe + H2O (Г).
143. В ракетных двигателях можно использовать реакции
Н2 (Г) + F2 = 2HF(Г); Н2 (Г) + O2 = 2H2O(Г).
Рассчитать изменение энтропии и ∆G0 при стандартных условиях для каждой из реакций и сравнить такие смеси по их эффективности. С учетом полученных данных и свойств начальных и конечных продуктов оценить перспективность использования каждой смеси.
144. По уравнению реакции 4FeO (Т) + O2 (Г) = 2Fe2O3 (Т); ∆S = –259 Дж/К, рассчитайте стандартную энтропию оксида железа (III).
145. Рассчитайте стандартную энтропию реакции образования оксида железа (III) из простых веществ по следующим данным:
(I) 2Fe (Т) + O2 (Г) = 2FeO (Т), ∆S 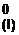 = –145 Дж/К;
= –145 Дж/К;
(II) 4FeO (Т) + O2 (Г) = 2Fe2O3 (Т), ∆S  = –259 Дж/К.
= –259 Дж/К.
Определить ∆G0 при стандартных условиях.
146. Определите расчетом, какие из реакций, уравнения которых:
a) 2ZnS (Т) + 3O2 (Г) = 2ZnO (Т) + 2SO2 (Г);
б) Аl2(SO4)3 (Т) = Al2O3 (Т) + 3SO3 (Г);
в) 2AgNO3 (Т) = 2Ag (Т) + 2NO2 (Г) + O2 (Г);
будут протекать самопроизвольно в изолированной системе при стандартных условиях.
147. Определите расчетом, какие из реакций, уравнения которых:
а) 4H2O(Г) + 3Fe(Т) = 4H2 (Г) + Fe3O4(Т);
б) 3Fe2O3(Т) + CO(Г) = 2Fe3O4 (Т) + CO2 (Г);
г) 3Fe2O3(Т) + Н2(Г) = 2Fe3O4(Т) + H2O(Г); будут протекать самопроизвольно в изолированной системе при стандартных условиях. Сделайте вывод о возможности протекания реакции.
148. Определите расчетом, какие из реакций, уравнения которых:
а) 2PbS (Т) + 3O2 (Г) = 2PbO (Т) + 2SO2 (Г);
б) CuCl2 (Т) + H2O (Г) = CuO (Т) + 2HСl (Г)
будут протекать самопроизвольно в изолированной системе при стандартных условиях.
149. Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите ∆G0 реакции, протекающей по уравнению NH3 (Г) + HСl (Г) = NH4Cl (К). Может ли эта реакция при стандартных условиях идти самопроизвольно?
150. При какой температуре наступит равновесие системы СО(Г) + 2Н2(Г) 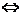 СН3ОН(Г); ∆H = –128,05 кДж?
СН3ОН(Г); ∆H = –128,05 кДж?
Не нашли, что искали? Воспользуйтесь поиском: