
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Текстура и свойства поверхности. Структура оксида алюминия зависит от типа исходного гидроксида, условий термической обработки, остаточного содержания воды и присутствия оксидов щелочных и
Структура оксида алюминия зависит от типа исходного гидроксида, условий термической обработки, остаточного содержания воды и присутствия оксидов щелочных и щелочно-земельных металлов.
Особенностью оксида алюминия является многообразие его модификаций и наличие фазовых переходов между ними в очень широком интервале температур. Эти фазы характеризуются шпинельной структурой и отличаются друг от друга наличием дефектов в кристаллической решетке. На рис. 19 приведены плотно и рыхлоупакованные решетки
α-Al2O3 (а) и γ-Al2O3 (б) [23].

Рис. 19. Плотно- и рыхлоупакованные решетки соответственно α-Al2O3 (а) и γ-Al2O3 (б)
Хотя образование плотноупакованной решетки α-Al2O3термодинамически возможно при низкой температуре, реально оно происходит только после некоторой перестройки кристаллических решеток переходных фаз оксида алюминия, что требует высокой температуры.
В ходе прокаливания гидроксида алюминия образующиеся частицы оксида обычно сохраняют форму исходных частиц или агрегатов частиц гидроксида.
В процессе превращения решетка оксида строится по простым законам на основе решетки гидроксида. Например, грань (001) байерита превращается в грань (111) шпинельной решетки  -оксида алюминия с образованием специфической структуры пор. Имеется два основных типа текстуры гидроксидов: кристаллический тригидроксид и микрокрис-таллический бемит. Непористый кристаллический тригидроксид характеризуется низкой удельной поверхностью, при термическом разложении его удаляются три молекулы воды и развивается высокая пористость с объемом пор 0,2−0,3 см3/г. При низкой температуре прокаливания система микропор оксида алюминия состоит из плоских параллельных пор, соответствующих расщеплению по грани (001) тригидроксида. Размер этих пор не превышает 2 нм, что приводит к значению Sуд порядка 500 м2/г. При дальнейшем нагревании эта система пор постепенно исчезает, уступая место цилиндрической системе пор с той же ориентацией, параллельно грани (001). Во всех случаях пористость образуется вследствие упаковки возникающих кристаллитов оксида алюминия. Сложность механизма разложения объясняется не столько структурными, сколько текстурными причинами.
-оксида алюминия с образованием специфической структуры пор. Имеется два основных типа текстуры гидроксидов: кристаллический тригидроксид и микрокрис-таллический бемит. Непористый кристаллический тригидроксид характеризуется низкой удельной поверхностью, при термическом разложении его удаляются три молекулы воды и развивается высокая пористость с объемом пор 0,2−0,3 см3/г. При низкой температуре прокаливания система микропор оксида алюминия состоит из плоских параллельных пор, соответствующих расщеплению по грани (001) тригидроксида. Размер этих пор не превышает 2 нм, что приводит к значению Sуд порядка 500 м2/г. При дальнейшем нагревании эта система пор постепенно исчезает, уступая место цилиндрической системе пор с той же ориентацией, параллельно грани (001). Во всех случаях пористость образуется вследствие упаковки возникающих кристаллитов оксида алюминия. Сложность механизма разложения объясняется не столько структурными, сколько текстурными причинами.
Мезо- и макропористость создаются соответственно упаковкой кристаллитов и агломератов оксидов. Регулирование пористости осуществляется за счет управления размерами кристаллитов и их агломератов, а также характером упаковки обоих. Термическое разложение крупных кристаллитов тригидроксида приводит к образованию пористых агрегатов мелких кристаллитов оксида алюминия.
Алюмогели и активный оксид алюминия относятся к адсорбентам с развитым объемом мезопор. Крупнопористый оксид алюминия имеет средний радиус пор 6−10 нм и удельную поверхность до 200 м2/г, мелкопористый – 3−4 нм и Sуд ~ 350-400 м2/г.
Свежепрокаленный оксид алюминия в присутствии влаги воздуха вновь гидратируется и гидроксилируется при обычной температуре. Это явление соответствует диссоциативной адсорбции воды, ведущей к образованию ОН-групп по схеме, представленной на рис. 20.
|
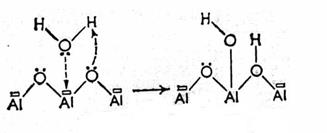
Образующиеся гидроксильные группы на поверхности оксида алюминия придают ей положительный заряд. 
Поверхность оксида алюминия представляет собой комбинацию ионов алюминия и кислорода, каждый из которых может иметь меньшее координационное число, чем в объеме. Эти поверхностные ионы являются вакантными центрами, которые при комнатной температуре всегда заняты либо гидроксильными группами, либо координационно-связанными молекулами воды. При этом восстанавливается нормальное координационное состояние поверхностных ионов: октаэдрическое или тетраэдрическое для ионов алюминия и октаэдрическое для ионов кислорода. Дегидрирование и дегидроксилирование поверхности оксида алюминия приводят к появлению координационно-ненасыщенных атомов кислорода (основные центры Льюиса) и алюминия (кислотные центры Льюиса), в результате чего оксид алюминия приобретает каталитические свойства в некоторых реакциях.
Характеристики некоторых отечественных и зарубежных марок активного оксида алюминия представлены в табл. 5.
Не нашли, что искали? Воспользуйтесь поиском:
 – кислота Льюиса, Ö – основание Льюиса
– кислота Льюиса, Ö – основание Льюиса