
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Применение I закона термодинамики к термохимии.
1) 1780 Лавуазье, Лаплас установили:
Кол-во теплоты, поглощаемое при разложении соединения должно быть равно количеству теплоты, которое выделяется при образовании этого соединения при этех же условиях. |qразл|=|qIобр| 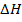 разл=
разл=  обр. Т.е. при написании обратной реакции надо изменить знак
обр. Т.е. при написании обратной реакции надо изменить знак 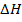 .
.
2) 1840 Гесс:
Суммарный тепловой эффект химической реакции при постоянном P не зависит от промежуточных стадий реакций.
Оба принципа вытекают из I закона термодинамики и являются следствиями того факта, что H – функция состояния.
P=const: 
Это позволит рассчитать изменение Н для реакций, которые нельзя изучить непосредственно.
3С(тв.)+ 2О2(газ)=2СО(газ)+CО2(газ)
Нецелесообразно измерять теплоту сгорания углерода до окиси углерода в ограниченном количестве О2, т.к. в продуктах реакции всегда есть смесь СО+ CО2 неопределенного состава.
Однако,
- можно измерить теплоту сгорания С до CО2 в избытке О2: для графита при 250С
С(тв.)+ О2(газ)=CО2(газ) 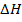 0=-94,0518ккал.
0=-94,0518ккал.
- можно измерить теплоту сгорания СО до CО2
СО(газ)+ 1/2О2(газ)=CО2(газ) 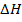 0=-67,6361ккал
0=-67,6361ккал
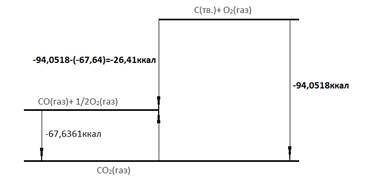
Нужную реакцию можно сконструировать из этих двух:
С(тв.)+ О2(газ)=CО2(газ) 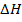 0= - 94,0518ккал.
0= - 94,0518ккал.
+
CО2(газ)=СО(газ)+ 1/2О2(газ) 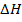 0=+67,6361ккал
0=+67,6361ккал
_______________________________________
С(тв.)+ 1/2О2(газ)= СО(газ)) 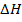 0= - 26,4157ккал
0= - 26,4157ккал
Допущения:
Пусть энтальпия элемента равна нулю при любой температуре.
Действительно, для нас представляет интерес разность энтальпий продуктов и исходных веществ в том случае, когда речь идет о простых элементах типа (O;H;N), то ясно, что они не из чего не образуются, нет перехода, нет изменения энтальпии.
Значит произвольно положим энтальпию простого элемента равной нулю при любой температуре, и это будет нашей точкой отсчета.
Простыми считаются элементарные вещества, находящиеся в том агрегатном состоянии, которое для них устойчиво при атмосферном давлении P=1атм и рассматриваемой температуре Т.
Например, при комнатной температуре Т=298К (250С) простыми веществами являются газы H2, O2, N2, жидкости Hg, Br и твердые вещества, такие как C, Si, Fe и др.
Теплота образования простых веществ принимается равной нулю.
Не нашли, что искали? Воспользуйтесь поиском: