
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
ИССЛЕДОВАНИЕ ВЛИЯНИЯ РАЗЛИЧНЫХ ФАКТОРОВ НА РАСТВОРИМОСТЬ МЕДИ В ШЛАКАХ
(2 часа)
1. ЦЕЛЬ РАБОТЫ
Определение с помощью ЭВМ доли оксидных и сульфидных потерь меди со шлаками
2. ТЕОРЕТИЧЕСКОЕ ВВЕДЕНИЕ
Плавка сульфидного сырья цветных металлов характеризуется получением трех фаз штейна, шлака и газа. Эти фазы частично растворимы друг в друге. Растворимость штейна в шлаке приводит к тому, что часть меди в растворенном виде находится в шлаке, что снижает ее извлечение в штейн. Кроме этого, часть меди присутствует а виде взвешенных частиц, не успевших осесть и слиться с донной фазой. Эту часть меди называют механическими потерями. Рассмотрим основные факторы, влияющие на растворенные и механические потери
Количество растворенной меди в шлаке зависит от условий плавки. Для правильного ведения процесса необходимо знать закономерности, определяющие растворимость меди в шлаке. Так, растворимые потери меди со шлаком представлены двумя формами • сульфидной (CuS0,5,) и оксидной (СиО0.5).

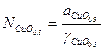
где: 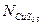 - мольная доля CuS0,5,
- мольная доля CuS0,5,  - активность CuS0,5,
- активность CuS0,5, 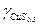 - коэффициент активности CuS0,5,
- коэффициент активности CuS0,5,  - мольная доля CuO0,5,
- мольная доля CuO0,5,  - активность CuO0,5,
- активность CuO0,5,  - коэффициент активностиCuO0,5 Активность этих соединений зависит от температуры, состава газовой фазы и состава шлака
- коэффициент активностиCuO0,5 Активность этих соединений зависит от температуры, состава газовой фазы и состава шлака


Общие потери растворенной меди со шлаками равны

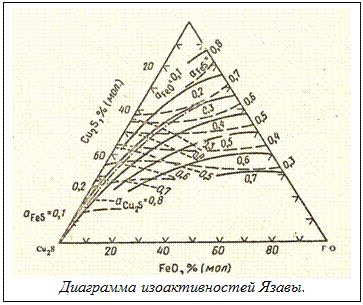
Для того чтобы определить активности сульфидной и оксидной меди в шлаковом расплаве используется диаграмма изоактивностей компонентов штейна (см рисунок) и система уравнений рассматриваемых ниже реакций.
На диаграмме вместо линий фазовых равновесий нанесены активности веществ Линии изоактивностей этой диаграммы описываются следующими уравнениями
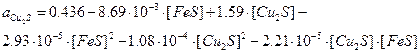 ,
,
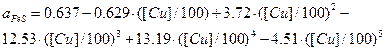 ,
,
аFeO = 0.35,
 где:
где:  - активность Cu2S в штейне,
- активность Cu2S в штейне, 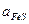 - активность FeS в штейне,
- активность FeS в штейне, 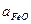 - активность FeO в штейне, [Сu] - содержание Сu в штейне, %, [Cu2S] - содержание Cu2S в штейне, %; [FeS] - содержание FeS в штейне, %
- активность FeO в штейне, [Сu] - содержание Сu в штейне, %, [Cu2S] - содержание Cu2S в штейне, %; [FeS] - содержание FeS в штейне, %
Тогда, зная активности компонентов штейна и давление SO2, можно определить активность магнетита, исходя из уравнения
3(Fe304) + [FeS] = 10(FeO) + SO2,
G = -171340-9,41T, ккал/моль,

Парциальное давление кислорода 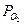 , определяем из следующей реакции:
, определяем из следующей реакции:
3 FeO + l/2О2 =Fe3О4
G = - 96200 + 40.59T, ккал/моль
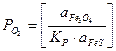
Парциальное давление серы  определяем из реакции
определяем из реакции
О2 + 1/2 S2 = SО2
G = - 88379 + 17.35Т, ккал/моль

Активность меди определяем из реакции
2Сu + 1/2 S2 = Cu2S,
G = - 35160 + 10.05Т, ккал/моль
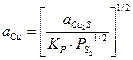
Тогда активность CuS 0,5 будет равна

Активность CuO0,5 определяем из реакции:
Сu + 1/4 O2 = CuO0,5

Полученные зависимости позволяют рассчитать активность CuO0,5 и активность CuS0,5. Кроме того, в ходе расчета определяются давления кислорода и серы.
Для расчета коэффициентов активности CuSo.5 и CuO0,5 используют регрессионные уравнения:
 ,
,

где: N - мольная доля компонента в шлаке.
Таким образом, полученных данных достаточно для определения количества растворенной меди со шлаками. Приведенный расчет показывает, что, зная состав штейна, шлака, температуру процесса и содержание сернистого ангидрида в газах, можно расчетным путем определить растворимость меди в шлаке.
Кроме абсолютных значений потерь металла со шлаком, можно определить и их доли.
Доля оксидных потерь меди, растворенной в шлаке, определяется по уравнению
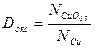
Доля сульфидных потерь определяется аналогично.
Размер механических потерь зависит от физических свойств штейна и шлака, а кроме того, от конкретных условий перемешивания, существующих в агрегате. Поэтому не представляется возможным не только точный расчет механических потерь меди, но и точное экспериментальное моделирование условий плавки.
3. АППАРАТУРА
Работа проводится на ЭВМ IBM-PC/АТ-386 по специально составленной программе, моделирующей процесс растворения штейна в шлаке. Программа составлена на языке Паскаль и работает в диалоговом режиме.
4. ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
1. Определить номер задания в соответствии с номером по АСУ (см. приложение)
2. Ввести исходные данные в ЭВМ и после расчета в таблицу записать результаты смоделированной опытной плавки.
Исходные и расчетные данные
| Исходные данные | Результаты расчета | |||||||||||
| N | Т.К | Cuшт | O2 | FeO | SiO2 | CaО | Al203 | Cuсул | Cuокс | Cuо6щ | PO2*103 | PS2*103 |
| … | ||||||||||||
5. ОБРАБОТКА РЕЗУЛЬТАТОВ
По полученным данным построить графики в соответствии с заданием. Сделать выводы о влиянии различных факторов на растворимость меди в шлаках.
6. ТРЕБОВАНИЯ К ОТЧЕТУ
Отчет должен содержать:
1. Краткое теоретическое введение.
2. Таблицу результатов.
3. Графики зависимости растворимости.
4. Письменные выводы о влиянии различных факторов на растворимость меди и описание продуктов плавки.
7. ЛИТЕРАТУРА
Ванюков А.В., Зайцев В.Л. Теория пирометаллургических процессов. - М.: Металлургия, 1993. С. 229-243.
8. КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Механические и растворенные (электрохимические) потери меди со шлаками.
2. Почему в процессе плавки важно получать шлаки определенного состава?
3. Каков механизм образования физических (сульфидных) и химических (оксидных) потерь меди со шлаками?
4. Что такое гетерогенизация шлака? К чему приводит гетерогенизация шлака по кремнезему и магнетиту?
5. Каково влияние температуры на величину механических и растворенных потерь?
6. Каково влияние состава штейна на размер сульфидных и оксидных потерь? Что означает максимума на кривой зависимости сульфидных потерь от состава штейна?
7. Чем объяснить, что большие добавки оксида кальция приводят к резкому падению растворенных потерь меди?
8. Как изменяется окислительный РO2, и сульфидирующий РS2 потенциалы системы при обогащении штейна? Как изменяются эти параметры при увеличении SO2 в газе?
Приложение
ЗАДАНИЯ К ЛАБОРАТОРНОЙ РАБОТЕ 5
| N | Т, К | Сuшт, % | SO2, % | FeO, % | SiO2, % | СаО, % | А12O3, % | Строящиеся зависимости |
| 0-80 | 20 и 50 | (Cu)сул – [Cu] (Cu)окс – [Cu] (Cu)общ – [Cu] | ||||||
| 0-80 | 20 и 50 | (Cu)сул – [Cu] (Cu)окс – [Cu] (Cu)общ – [Cu] | ||||||
| 0-80 | 20 и 50 | (Cu)сул – [Cu] (Cu)окс – [Cu] (Cu)общ – [Cu] | ||||||
| 0-80 | 30 и 70 | (Cu)сул – [Cu] (Cu)окс – [Cu] (Cu)общ – [Cu] | ||||||
| 0-80 | 30, 70 | (Cu)сул – [Cu] (Cu)окс – [Cu] (Cu)общ – [Cu] | ||||||
| б | 0-80 | 30, 70 | (Cu)сул – [Cu] (Cu)окс – [Cu] (Cu)общ – [Cu] | |||||
| 0-80 | 20, 50 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | ||||||
| 0-80 | 20, 50 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | ||||||
| 0-80 | 20, 50 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | ||||||
| 0-80 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | |||||||
| 0-80 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | |||||||
| 0-80 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | |||||||
| 0-80 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | |||||||
| 0-80 | (Cu)сул – [Cu] lgPO2 – [Cu] lgPS2 – [Cu] | |||||||
| (Cu)сул – T Dокс – T Dсул – T | ||||||||
| (Cu)сул – T Dокс – T Dсул – T | ||||||||
| (Cu)сул – T Dокс – T Dсул – T | ||||||||
| (Cu)сул – T Dокс – T Dсул – T | ||||||||
| (Cu)сул – T Dокс – T Dсул – T | ||||||||
| (Cu)сул – T Dокс – T Dсул – T | ||||||||
| 0-80 | 5, 20 | (Cu)сул – [Cu] Dокс – [Cu] Dсул – [Cu] | ||||||
| 0-80 | 5, 20 | (Cu)сул – [Cu] Dокс – [Cu] Dсул – [Cu] | ||||||
| 0-80 | 3, 30 | (Cu)сул – [Cu] Dокс – [Cu] Dсул – [Cu] | ||||||
| 0-80 | 3, 30 | (Cu)сул – [Cu] Dокс – [Cu] Dсул – [Cu] | ||||||
| 0-80 | 3, 30 | (Cu)сул – [Cu] Dокс – [Cu] Dсул – [Cu] |
П ример выполнения задания
Исходные данные
Т = 1220°С
М2 = 1% и 60%
Сишт = 0 - 80%
FеОшл = 55%
SiO2 = 35%
Al2O3 = 7%
СаОшл = 3%
Построить зависимости: %Сишя - %Сишт,
lgP(O2)- %Сишт
Dоkc - % Cuшт
Пример исходных и расчетных данных
| Исходные данные | |||||||
| N | Т,К | Cuшт | S02 | FeO | Si02 | СaО | А1203 |
| Результаты расчёта | |||||||
| N | Cuсул | Cuокс | Cuобщ | PO2∙109 | PS2∙103 | ||
| 2,9 | |||||||
| 0,020 | 0,062 | 0,082 | 2,7 | ||||
| 0,028 | 0,089 | 0,117 | 2,6 | ||||
| 0,033 | 0,111 | 0,147 | 2,3 | ||||
| 0,037 | 0,141 | 0,178 | 1,9 | ||||
| 0,038 | 0,178 | 0,217 | 1,4 | ||||
| 0,037 | 0,233 | 0,276 | 0,8 | ||||
| 0,033 | 0,362 | 0,396 | 0,3 | ||||
| 0,021 | 0,968 | 0,989 | 2,4 | 0,03 | |||
| 3,9 | |||||||
| 0,418 | 0,066 | 0,485 | 4,0 | ||||
| 0,584 | 0,096 | 0,680 | 4,1 | ||||
| 0,700 | 0,121 | 0,821 | 4,3 | ||||
| 0,775 | 0,151 | 0,926 | 4,8 | ||||
| 0,808 | 0,191 | 0,998 | 5,5 | ||||
| 0,790 | 0,255 | 1,046 | 7,3 | ||||
| 0,705 | 0,388 | 1,093 | 5,3 | ||||
| 0,448 | 1,038 | 1,486 | 0,4 |
Не нашли, что искали? Воспользуйтесь поиском: