
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Определение знака заряда мицеллы коллоидного раствора
Метод капиллярного поднятия. При погружении фильтроваль-ной бумаги в раствор по ее капиллярам поднимается вода, увлекая частицы дисперсной фазы. Поверхность стенок капилляров бумаги, смоченной водой, имеет отрицательный заряд.
Если частицы золя заряжены положительно, то они, электростатически адсорбируясь на стенках капилляров, не будут подниматься по бумаге выше уровня раствора. Отрицательно заряженные мицеллы вместе с дисперсионной средой распространяются по бумаге, окрашивая ее.
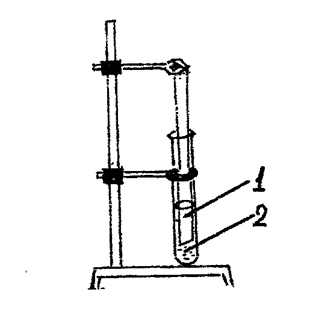
Рис. 5.3. Фиксированное погружение фильтровальной бумаги (1) в раствор (2)
Таким образом, погружая конец полоски фильтровальной бума-ги (шириной около 1 см, рис.5.3) в коллоидный раствор на 20–
30 мин., можно установить знак заряда поверхности мицелл золя.
Выполнение опыта
В чистую коническую колбу (на 250 мл) возьмите 50 мл 0,1н KMnO4 и, тщательно перемешивая стеклянной палочкой, приливайте по каплям 1 % раствор Н2О2 до полного израсходования перманга-ната калия. Конец реакции определите по исчезновению розовой окраски капли раствора, нанесенного стеклянной палочкой на фильтровальную бумагу.
Полученный раствор разбавьте в три раза (добавив двукратный объем воды). Определите знак заряда золя методом капиллярного поднятия. Испытайте устойчивость золя оксида марганца (IV) в присутствии электролитов. С этой целью в три пробирки налейте поровну (около 3 мл) полученного гидрозоля. В одну пробирку из бюретки прилейте по каплям 1н NaCl, отмечая объем раствора, вызывающего коагуляцию золя. В двух других пробирках определите коагулирующие действия 1н MgCl2 и 1н AlCl3.
В отчете приведите структуру мицеллы оксида марганца (IV) и график распределения заряда в двойном электрическом слое мицеллы, укажите и объясните знак заряда золя, его характерные свойства и устойчивость в присутствии электролитов.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Что называется раствором?
2. Каковы способы выражения концентраций растворов?
3. Какое количество растворяемого вещества CuSO4 необходи-мо взять для приготовления 3 литров: а) 2 N, б) 6 %, в) 1,5 М раствора?
4. Какое количество концентрированной серной кислоты (96 %), плотность которой 1,84 г/см3, необходимо взять для приготовления раствора: а) 100 мл 0,2 N; б) 300 мл 0,5 М; в) 450 мл 2,5 N?
5. Почему при растворении КОН, H2SO4, HNO3 выделяется тепло, а при растворении KCl тепло поглощается?
6. Почему зимой посыпают снег солью, что такое антифризы, какова их роль?
7. Рассчитайте концентрацию Н+ в растворах: а) 0,3 М HCl; б) 0,2 N H2SO4; в) 0,02 М СН3СООН.
8. Вычислите рН растворов: а) 0,01 М HCl; б) 0,2 М NaOH; в) 0,03 М СН3СООН.
9. Вычислите активности Н+ и ОН  в растворах, если рН равен: а) 11,2; б) 4,5; в) 2,3.
в растворах, если рН равен: а) 11,2; б) 4,5; в) 2,3.
10. Какие значения рН имеют растворы солей при гидролизе: а) FeSO4, Na2CO3; б) Na2S, CuSO4; в) CH3COONa, Ca(NO3)2?
11. Могут ли существовать в растворах соли: а) СаСО3; б) Fe2S3;
в) Al2(CO3)3?
12. Как отличить коллоидные растворы от истинных?
13. Что обусловливает устойчивость коллоидных растворов?
14. Нарисуйте строение мицеллы золя AgI в избытке йодида калия.
15. Какие системы называют эмульсиями?
16. Что такое эмульгаторы?
Не нашли, что искали? Воспользуйтесь поиском: