
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Период расплавления и окислительный период
Плавку ведем с применением железной руды и технического кислорода. В период расплавления и окислительный период окисляются следующие элементы:
1. Для получения в конце окислительного периода содержание углерода 0,18 % необходимо окислить:
ΔС = ΔСмш - ΔСКО.П. =1,356 – 0,18=1,176 %
2. Кремний окисляется полностью – 0,504 кг
3. Марганец по практическим данным окисляется на 55%.

4. Сера полностью переходит в металл.
5. Фосфора в готовом металле должно быть 0,02 %. Следовательно, нужно окислить ΔP = 0,073 – 0,02 = 0,053 % от веса металла, или
GP =  =
=  = 0,051 кг
= 0,051 кг
6 Железо окисляется на 2 – 4 %. Принимаем 3 %, или
GFe =  = 2,94 кг.
= 2,94 кг.
По практическим данным около 90 % железа окисляется до Fe2O3 и испаряется в зоне электрических дуг, около 10 % окисляется до FeO и Fe2O3 и переходит в шлак, причем задаемся соотношением FeO/Fe2O3 = 3, т.е. 75 % окислившегося железа в шлак окисляется до FeO, а 25,0 % железа – до Fe2O3.
Следовательно, в шлак переходит железа
 = 0,294 кг
= 0,294 кг
Из этого количества окисляется до FeO  = 0,22 кг
= 0,22 кг
До Fe2O3 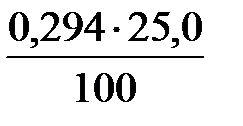 = 0,074 кг.
= 0,074 кг.
В зоне электрических дуг испаряется железа  = 2,646 кг Fe до Fe2O3.
= 2,646 кг Fe до Fe2O3.
В таблице 7 приводится необходимое количество закиси железа для окисления указанных элементов и количество образовавшихся оксидов.
Таблица 7 – Количество закиси железа (FeO) и образовавшихся оксидов
| Реакция окисления | Количество окислившегося элемента, кг | Потребное количество FeO, кг | Количество образовавшегося оксида, кг | Количество восстановленного в металл железа, кг |
| [Mn]+(FeO)= =(Mn)+[Fe] | 0,322 | 0,322  = 0,42 = 0,42
| GMnO = 0,322  =
=0,416 =
=0,416
| Fe = 0,322 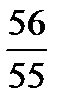 =
= 0,328 =
= 0,328
|
| [Si]+2(FeO)= =(SiO2)+2[Fe] | 0,504 | 0,504 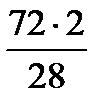 = 2,6 = 2,6
| GSiO2 = 0,504  =
=1,08 =
=1,08
| Fe = 0,504  = 2,0 = 2,0
|
| 2[P]+5FeO= =(P2O5)+5[Fe] | 0,051 | 0,051  = 0,29 = 0,29
| GP2O5=0,051  =0,11 =0,11
| Fe = 0,051 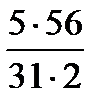 = =0,23 = =0,23
|
| Итого | ΣFeO = 3,31 кг | ΣFe = 2,5 кг |
В таблице 8 необходимое количество кислорода для окисления углерода и железа шихты и количество образовавшихся оксидов
Таблица 8 – Количество кислорода и образовавшихся оксидов
| Реакция окисления | Количество окислившегося элемента, кг | Необходимое количество кислорода, кг | Количество образовавшегося оксида, кг |
| [C]+(FeO) = {CO}+[Fe] | 1,176 | 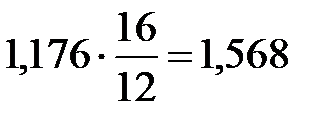
| 
|
| Fe+1/2O2 = FeO | 0,147 | 
| 
|
| 2Fe+3/2O2 = Fe2O3 | 0,049 | 
| 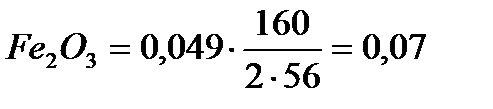
|
| 1,768 | 
| 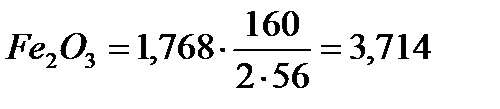
| |
| Итого: S O2 = 2,4 кг |
Определение количества шлака окислительного периода и периода расплавления.
Одной из задач окислительного периода является удаление фосфора из металла. По существующей технологии около 80 % фосфора удаляется из металла в период расплавления, а остальное количество – в начале окислительного периода.
Коэффициент распределения фосфора между шлаком и металлом выражается следующим соотношением
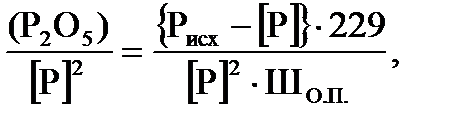 (9)
(9)
где (P2O5) / [Р]2 – коэффициент распределения фосфора между металлом и
шлаком;
Рисх – содержание фосфора в шихте, %;
[Р] – содержание фосфора в готовом металле, %;
Ш О.П. – количество шлака окислительного периода, % (от веса металла).
Принимаем CaO/SiO2 = 2,4; FeO = 16 %; t = 1580 0С.
Согласно данным [1] получаем  = 15850.
= 15850.
Из выражения определяем количество шлака. Принимаем Pисх = 0,03 %;
[P] = 0,01 %, имеем
ШО.П. =  = 9,1 %
= 9,1 %
Или GШо.п = 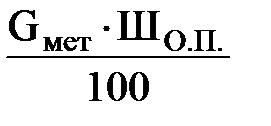 =
=  = 8,8 кг.
= 8,8 кг.
Шлак окислительного периода наводится из извести и кварцита, для хорошей дефосфорации принимаем, что FeO = 16 %, а основность шлака CaO/SiO2 = 2,4.
По практическим данным около 10 % MgO из подины перейдет в шлак, т.е.
GШ.о.п. = GMnО + GP2O5 + GFe2O3 + GMgO + GFeO + GSiO2 + GCaO. (10)
Количество (MnO), (P2O5), (Fe2O3) приведено в таблицах 7 и 8. Количество (FeO), (MgO), содержащееся в шлаке, равно
GFeO =  =
=  = 1,5 кг.
= 1,5 кг.
GMgO =  =
= 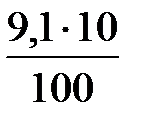 = 0,91 кг.
= 0,91 кг.
Так как основность шлака CaO/SiO2=2,4, содержание CaO=2,4SiO2.
Таким образом, получаем из уравнения
9,1 = 0,416+0,11+0,11+0,91+1,456+GSiO2+2,4GSiO2
GSiO2 = 1,8 кг; GCaO = 4,3 кг.
Данные о приближенном весовом количестве и химическом составе шлака окислительного периода приведены в таблице 9.
Таблица 9 – Вес и состав шлака окислительного периода
Не нашли, что искали? Воспользуйтесь поиском: