
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Электролитическая диссоциация
Растворение любого вещества в воде сопровождается образованием гидратов. Если при этом в растворе не происходит формульных изменений у частиц растворенного вещества, то такие вещества относят к неэлектролитам. Ими являются, например, газ азот N2, жидкость хлороформ СНCl3, твердое вещество сахароза C12Н22О11, которые в водном растворе существуют в виде гидратов их молекул.
Известно много веществ (в общем виде МА), которые после растворения в воде и образования гидратов молекул MA nН2O претерпевают существенные формульные изменения. В результате в растворе появляются гидратированные ионы – катионы М+ • nН2O и анионы А • nН2O:

Такие вещества относят к электролитам.
Процесс появления гидратированных ионов в водном растворе называется электролитической диссоциацией (С. Аррениус, 1887).
Электролитическая диссоциация ионных кристаллических веществ (М+)(А‑) в воде является необратимой реакцией:

Такие вещества относятся к сильным электролитам, ими являются многие основания и соли, например:

Электролитическая диссоциация веществ MA, состоящих из полярных ковалентных молекул, является обратимой реакцией:
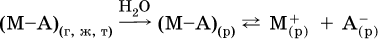
Такие вещества относят к слабым электролитам, ими являются многие кислоты и некоторые основания, например:
а)

б)

в)

г)

В разбавленных водных растворах слабых электролитов мы всегда обнаружим как исходные молекулы, так и продукты их диссоциации – гидратированные ионы.
Количественная характеристика диссоциации электролитов называется степенью диссоциации и обозначается α[1], всегда α > 0.
Для сильных электролитов α = 1 по определению (диссоциация таких электролитов полная).
Для слабых электролитов степень диссоциации – отношение молярной концентрации продиссоциировавшего вещества (сд) к общей концентрации вещества в растворе (с):

Степень диссоциации – это доля от единицы или от 100 %. Для слабых электролитов α «С 1 (100 %).
Для слабых кислот НnА степень диссоциации по каждой следующей ступени резко уменьшается по сравнению с предыдущей:
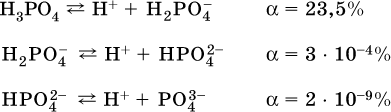
Степень диссоциации зависит от природы и концентрации электролита, а также от температуры раствора; она растет при уменьшении концентрации вещества в растворе (т. е. при разбавлении раствора) и при нагревании.
В разбавленных растворах сильных кислот НnА их гидроанионы Нn‑1А не существуют, например:

B концентрированных растворах содержание гидроанионов (и даже исходных молекул) становится заметным:

(суммировать уравнения стадий обратимой диссоциации нельзя!). При нагревании значения α1 и α2 возрастают, что способствует протеканию реакций с участием концентрированных кислот.
Кислоты – это электролиты, которые при диссоциации поставляют в водный раствор катионы водорода и никаких других положительных ионов не образуют:

Распространенные сильные кислоты:

В разбавленном водном растворе (условно до 10 %‑ного или 0,1‑молярного) эти кислоты диссоциируют полностью. Для сильных кислот НnА в список вошли их гидроанионы (анионы кислых солей), также диссоциирующие полностью в этих условиях.
Распространенные слабые кислоты:

Основания – это электролиты, которые при диссоциации поставляют в водный раствор гидроксид‑ионы и никаких других отрицательных ионов не образуют:

Диссоциация малорастворимых оснований Mg(OH)2, Cu(OH)2, Mn(OH)2, Fe(OH)2 и других практического значения не имеет.
К сильным основаниям (щелочам) относятся NaOH, КОН, Ва(ОН)2 и некоторые другие. Самым известным слабым основанием является гидрат аммиака NH3 Н2O.
Средние соли – это электролиты, которые при диссоциации поставляют в водный раствор любые катионы, кроме Н+, и любые анионы, кроме ОН‑:

Речь идет только о хорошо растворимых солях. Диссоциация малорастворимых и практически нерастворимых солей значения не имеет.
Аналогично диссоциируют двойные соли:

Кислые соли (большинство из них растворимы в воде) диссоциируют полностью по типу средних солей:

Образующиеся гидроанионы подвергаются, в свою очередь, воздействию воды:
а) если гидроанион принадлежит сильной кислоте, то он сам диссоциирует также полностью:

и полное уравнение диссоциации запишется в виде:

(растворы таких солей обязательно будут кислыми, как и растворы соответствующих кислот);
б) если гидроанион принадлежит слабой кислоте, то его поведение в воде двойственно – либо неполная диссоциация по типу слабой кислоты:

либо взаимодействие с водой (называемое обратимым гидролизом):

При α1 > α2 преобладает диссоциация (и раствор соли будет кислым), а при α1 > α2 – гидролиз (и раствор соли будет щелочным). Так, кислыми будут растворы солей с анионами HSO3‑, H2PO4‑, H2AsO4‑ и HSeO3‑, растворы солей с другими анионами (их большинство) будут щелочными. Другими словами, название «кислые» для солей с большинством гидроанионов не предполагает, что эти анионы будут вести себя в растворе как кислоты (гидролиз гидроанионов и расчет отношения между α1 и а2 изучаются только в высшей школе).
Оснóвные соли MgCl(OH), Cu2CO3(OH)2 и другие в своем большинстве практически нерастворимы в воде, и обсуждать их поведение в водном растворе невозможно.
Не нашли, что искали? Воспользуйтесь поиском: