
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Разнообразие архей способных использовать энергию света. Особенности механизма и экологическое значение.
Солеустойчивые археи — галоархеи (лат. Haloarchaea) — используют в качестве источника энергии солнечный свет,
Галобактерии (лат. Halobacteriaceae) — семейство архей. Включает около двадцати родов, в том числе Halobacterium, Halococcus, Haloarcula, Natrococcus, Natrobacterium.
Представители семейства живут в средах с высоким содержанием солей, в том числе в Мёртвом море, где концентрация соли достигает 26—27 %, а в некоторые годы повышается до 31 % (при 36 % NaCl выпадает в осадок), на кристаллах соли в прибрежной полосе, в солончаках, на солёной рыбе, на засолённых шкурах животных, на рассольных сырах, в капустных и огуречных рассолах.
Галобактерии — кокковидные или палочковидные, подвижные или неподвижные аспорогенные микроорганизмы. Большинство из них окрашиваются грамположительно. У некоторых имеются газовые вакуоли для контроля плавучести.
Преимущественно аэробы, но могут переносить и очень низкое содержание кислорода в среде, свободноживущие сапрофиты. По типу источника энергии это фототрофы, по донору электронов — органотрофы и по источнику углерода — гетеротрофы. При наличии кислорода и органических соединений, которые можно использовать в качестве источника энергии, галобактерии способны развиваться и в темноте (то есть в зависимости от условий фотоорганогетеротрофы либо хемоорганогетеротрофы). Однако при недостатке или даже при полном отсутствии кислорода и ярком освещении в оболочке клеток синтезируется бактериородопсин, позволяющий использовать энергию Солнца. Из-за большого содержания каротиноидов галобактерии окрашены в красные, оранжевые и жёлтые тона. Наиболее распространённый каротиноид это бактериоруберин.
Их мембранный бислой построен из изопрениловых диэфиров фосфоглицерина, с небольшим содержанием неполярных липидов-с30-изопреноидов и с очень большим содержанием белков. В мембране различают участки пурпурного и красно-оранжевого цветов. В пурпурной мембране 75 % массы приходится на одно единственное вещество — бактериородопсин. В мембране также содержится два так называемых сенсорных родопсина, которые обеспечивают положительный и отрицательный фототаксис. Различные длины волн считываются ими, что вызывает каскад сигналов, управляющих жгутиковым двигателем бактерий. Кроме того, в мембране имеется галородопсин, представляющий собой светозависимый насос ионов хлора. Его основная функция — транспорт в клетку Cl−, которые постоянно теряются бактерией под действием электрического поля, создаваемого бактериородопсином. Жизнь в гипоксическом рассоле привела к выработке у галобактерий мощной системы активного транспорта, благодаря которой концентрация Na+ в цитоплазме поддерживается на низком уровне, несмотря на колоссальный концентрационный градиент Na+ на клеточной мембране.
Следует отметить, что чем выше концентрация натрия в среде, тем выше содержание К+ внутри клеток. Известно, что калий необходим для работы большинства внутриклеточных ферментов, тогда как натрий подавляет активность многих из них. При существенном снижении концентрации соли в среде, клетки бактерий разрушаются. Посредником синтеза АТФ служит концентрационный градиент Н+ на мембране галобактерий. Он создаётся и поддерживается системой активного транспорта, переносящей их из среды в цитоплазму. За счёт этого pH в цитоплазме стабилен, очень низок — около 3 и мало зависит от щелочности водоёма, где pH может достигать 12.
Экология:
Судя по их строению, галобактерии — одни из древнейших обитателей нашей планеты. Человечеству они известны довольно давно по красноватому налёту на продуктах, консервируемых с использованием больших количеств поваренной соли. Впервые галобактерии были выделены в начале прошлого столетия из микрофлоры лиманной грязи, однако их систематическое изучение началось только в конце второго десятилетия двадцатого века. У них практически нет врагов или конкурентов, способных жить в таких же условиях, и поэтому галобактерии свободно эволюционировали на протяжении всей истории жизни на Земле. Галобактерии не наносят никакого существенного вреда народному хозяйству. Очевидно, что внутренняя среда человека непригодна для жизнедеятельности галобактерий, поэтому среди них нет ни одного патогена.
36)Разнообразие прокариот, осуществляющих процессы брожения. Общая характеристика энергетическая сторона, пути осуществления. Обобщающая схема важнейших брожений.
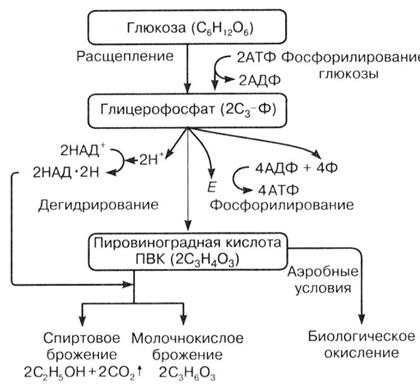
"Брожение" — это сугубо микробиологический термин. Он характеризует энергетическую сторону способа существования нескольких групп эубактерий, при котором они осуществляют в анаэробных условиях окислительно-восстановительные превращения органических соединений, сопровождающиеся выходом энергии, которую эти организмы используют. Поскольку брожение протекает без участия молекулярного кислорода, все окислительно-восстановительные превращения субстрата происходят за счет его "внутренних" возможностей. Процесс брожения связан с такими перестройками органических молекул субстрата, в результате которых на окислительных этапах процесса высвобождается часть свободной энергии, заключенной в молекуле субстрата, и происходит ее запасание в молекулах АТФ. В процессе брожения, как правило, происходит расщепление углеродного скелета молекулы субстрата.
Круг органических соединений, которые могут сбраживаться, довольно широк. Это углеводы, спирты, органические кислоты, аминокислоты, пурины, пиримидины. Химическое вещество может быть подвергнуто сбраживанию, если оно содержит неполностью окисленные (или восстановленные) углеродные атомы. В этом случае есть возможность для окислительно-восстановительных преобразований между молекулами (или внутри одного вида молекул), возникающими из субстрата. В результате одна часть продуктов брожения будет более восстановленной, другая — более окисленной по сравнению с субстратом. Продуктами брожений являются различные органические кислоты (молочная, масляная, уксусная, муравьиная), спирты (этиловый, бутиловый, пропиловый), ацетон, а также CO2 и H2. Обычно в процессе брожения образуется несколько продуктов. В зависимости от того, какой основной продукт накапливается в среде, различают молочнокислое, спиртовое, маслянокислое, пропионовокислое и другие виды брожений.
Следовательно, в каждом виде брожения можно выделить две стороны: окислительную и восстановительную. Процессы окисления сводятся к отрыву электронов от определенных метаболитов с помощью специфических ферментов (дегидрогеназ) и акцептированию их другими молекулами, образующимися из сбраживаемого субстрата, т. е. в процессе брожения происходит окисление анаэробного типа.
Энергетическая сторона
Собственно энергетической стороной процессов брожения является их окислительная часть, поскольку реакции, ведущие к выделению энергии, — это реакции окисления. Существует несколько исключений из этого правила: некоторые анаэробы часть энергии при сбраживании субстрата получают также в результате его расщепления.
При брожении некоторые реакции на пути анаэробного преобразования субстрата связаны с наиболее примитивным типом фосфорилирования — субстратным фосфорилированием. К синтезу АТФ по механизму субстратного фосфорилирования ведут катаболические реакции, которые в зависимости от своей химической природы могут быть разделены на два типа. Большинство относится к окислительно-восстановительным реакциям. Богатые энергией соединения возникают в процессе брожения на этапах анаэробного окисления.
Второй тип реакций связан с расщеплением субстратов или промежуточных продуктов, образующихся из них. Катализируются эти реакции ферментами, относящимися к классу лиаз.
Из других высокоэнергетических соединений важное место в энергетике процессов брожения принадлежит фосфоенолпировиноградной кислоте (ФЕП). Эти соединения характеризуются тем, что свободная энергия, освобождающаяся при их гидролизе, находится в области значений от -35 до -88 кДж/моль и с помощью соответствующих ферментов может быть перенесена на молекулы АДФ.
Несмотря на большое число углеродных субстратов, доступных для сбраживания, количество реакций, приводящих непосредственно к синтезу АТФ при брожениях, сравнительно невелико. Наиболее распространены следующие из них:
1) ацетилфосфат + АДФ ® ацетат + АТФ;
2) 1,3-фосфоглицериновая кислота + АДФ ® 3-фосфоглицеринновая кислота + АТФ;
3) фосфоенолпировиноградная кислота + АДФ ® пировиноградная кислота + АТФ.
37) Разнообразие молочнокислых бактерий и их практическое значение. Пути сбраживания углеводов.
Молочнокислое брожение осуществляют филогенетически не родственные микроорганизмы, объединяемые по признаку образования молочной кислоты (представители порядков Lactobacillales и BaciHales класса Bacilli и сем. Bifidobacteriaceae класса Actino- bacteria). Они различны по морфологии, но все грамположительны, не образуют спор (кроме представителей сем. Sporolacto- bacillaceae), неподвижны. Живут только за счет брожения (АТФ получают исключительно путем субстратного фосфорилирования), аэротолерантны, каталазоотрицательны, не содержат гемопротеинов (цитохромов), растут только на богатых средах с добавлением большого количества факторов роста (витаминов), могут использовать лактозу, чем схожи с бактериями кишечной группы.
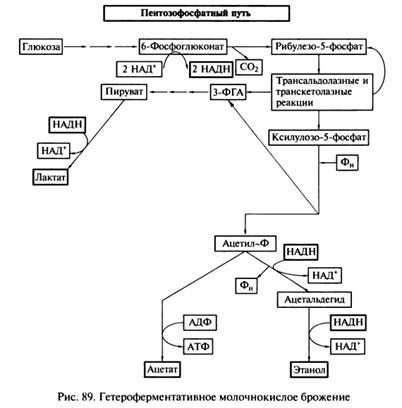
Схема сбраживания сахаров через гликолиз характерна для гомоферментативного молочнокислого брожения (рис. 88), когда лактата образуется -90% и только 10 % приходится на другие продукты (ацетат, ацетоин, этанол). При гетероферментативном молочнокислом брожении (рис. 89) сахара сбраживаются через пентозофосфатный путь и лактата образуется ~50 %.
Некоторые гетероферментативные молочнокислые бактерии очень чувствительны к изменению условий. Так, L. mesenteroides при соприкосновении с кислородом образует значительное количество полисахарида (происходит ослизнение продукта).
Гетероферментативные молочнокислые бактерии рода Bifidobacterium образуют при делении V-подобные структуры.

38) Разнообразие азотфиксирующих микроорганизмов. Особенности фиксации молекулярного азота как метаболического процесса.
Азотфиксация -это уникальный процесс, присущий только прокариотическим микроорганизмам. Под азотфиксацией понимается способность некоторых групп бактерий и архей к энзиматическому восстановлению атмосферного N2 до аммония (с образованием водорода), который затем включается в клеточное вещество.
Большое число микроорганизмов- представители 80 родов из 27 семейств бактерий и по крайней мере три термофильных рода архей- обладают способностью к азотфиксации.
Такие микроорганизмы подразделяют на свободноживущие и ассоциативные.
Процесс фиксации молекулярного азота
Несмотря на разнообразие микроорганизмов, осуществляющих азотфиксацию, ферментный комплекс нитрогеназы одинаков и у анаэробов, и у аэробов. Один из ее отличительных признаков — чрезвычайная чувствительность к наличию кислорода. Поэтому у аэробных микроорганизмов существует проблема защиты нитрогеназы от кислорода. Разные микроорганизмы решают ее разными путями. У цианобактерий имеются специализированные клетки- гетероцисты, в которых нет ФС II и поэтому при фотосинтезе не образуется кислород, а толстая клеточная стенка препятствует его диффузии снаружи. Активная оксидазная система тут же восстанавливает проникший кислород. У азотобактера сильно развита слизистая капсула, препятствующая проникновению кислорода, и уникальная оксидазная система с очень высоким сродством к 02 (/lm = 10-7— 10_6, т.е. в 10— 100 раз выше обычной), не допускающая метаболический кислород к нитрогеназе. Обнаружено, что некоторые свободноживущие аэробы обладают нитрогеназой, белковая часть которой имеет особую конформацию, менее чувствительную к 02. Некоторые аэробные азотфиксаторы выбирают микроаэрофильные местообитания или сосуществуют в экосистемах с организмами, активно потребляющими кислород. Факультативные анаэробы фиксируют азот только в анаэробных условиях. Наиболее изощренная защита нитрогеназы обнаружена у клубеньковых бактерий, которые снабжают растение связанным азотом. Растение же защищает бактероиды и дает им продукты фотосинтеза — органические вещества. Для защиты нитрогеназы в клубеньках синтезируется леггемоглобин — самый высокочувствительный к кислороду белок-оксидаза. Леггемоглобин реагирует с наномолярными количествами кислорода. Интересно, что синтез этого соединения происходит совместно — белковую часть образует растение, а гем синтезирует бактероид.
Фиксация азота жестко регулируется наличием его связанных форм. Нитрогеназа репрессируется, если в среде есть NH|.
Итак, газ азот — это химически инертное и очень стабильное вещество. Чтобы разорвать тройную связь в его молекуле, необходимо много энергии. Реакция ЗН2 + N2 -> 2NH3 — эндотермическая. Для ее осуществления требуется по крайней мере 8 электронов и 16 молекул АТФ. На самом деле АТФ затрачивается больше, поскольку часть ее нужна для поддержания анаэробных условий.
Нитрогеназный ферментный комплекс состоит из двух компонентов: Mo-Fe-белок с молекулярной массой 220 кДа и Fe- белок — 64 кДа. Mo-Fe-белок содержит два атома молибдена и 28 — 32 атомов железа, в Fe-белке — 4 атома железа. Для проявления нитрогеназной активности необходимы оба компонента, они взаимозаменяемы у разных микроорганизмов. Mo-Fe-белок состоит из четырех субъединиц: 2а (кодируются nifD-геном) и 2р (nifK-ген). Fe-белок состоит из двух субъединиц. Ферредоксин восстанавливается либо в реакциях фотосинтеза у фототрофов, либо при дыхании у аэробных диазотрофов, или при брожении у анаэробов. При фиксации азота всегда выделяется молекулярный водород:
N2+ 8ё + 8Н++ 16АТФ - Mg2+ -> 21МН3 + Н2Т + 16АДФ - Mg2+
Реакция проходит в несколько стадий: N = N———»Н1М=
= NH |2Н| >H2N—NH2 |2H| >2NH3. Первым свободным
продуктом является аммиак, все промежуточные продукты связаны с ферментным комплексом. В отсутствие N2 нитрогеназа интенсивно выделяет Н2, так как электроны восстановителей необходимо сбросить. Несмотря на высокое сродство нитрогеназы к N2, она не очень специфична и может восстанавливать и другие соединения: С2Н2 -» С2Н4, HCN -» СН4 + NH3.

39) Разнообразие метанобразующих архей. Пути образования метана.
Метанобразующие бактерии(метаногены)-морфологически разнообразная группа, объединяемая двумя общими для всех ее представителей признаками: облигатным анаэробиозом и способностью образовывать метан. Для создания таксономической структуры был использован филогенетический подход, основанный на сравнительном анализе нуклеотидных последовательностей 16S рРНК.3 порядка- Methanobacteriales, Methanococcales, Methanomicrobiales, 6 семейств, более 40 видов.
В состав группы входят бактерии с разной морфологией: прямые или изогнутые палочки разной длинны; клетки неправильной формы, близкие к коккам; извитые формы. Клетки неподвижные или передвигающиеся с помощью перитрихально или полярно расположенных жгутиков. КС 3х типов: из псевдомуреина, построенные из белковых глобул и гетерополисахаридной природы. 20-30% мембранных липидов метаногенов представленны нейтральными и 70-80% - полярными липидами. Метагены- чистые анаэробы. Большинство имеет температурный оптимум дл роста в области 30-40 С, т.е являются мезофилами. Нейтрофилы с оптимальным рН 6.5-7.5. Среди метаногенов есть галофилы. Источник углерода и энергии - газовая смесь Н2 и СО2. Источник азота- аммонийный азот или некоторые аминокислоты. Источник серы- сульфаты, сульфид или серосодержащие аминокислоты.
БОльшинство известных метаногенов способны расти хемолитоатотрофно на смеси СО2+Н2 в качестве единственного источника углерода и энергии. Энергию получают, осуществляя следующую реакцию: 4Н2+СО2→СН4+2Н2О
Фиксация СО2 у автотрофных метаногенов происходит по нециклическому ацетил-КоА-пути, функционирующему и у ацетоногенных эубактерий. Ключевым промежуточным соединением этого пути является ацетил-КоА, синтезируемый из двух молекул CO2. Метильная и карбоксильная группы молекулы образуются разными путями. Метильная группа возникает при восстановлении молекулы CO2 до уровня метанола, оставаясь при этом всегда связанной с переносчиком. Карбоксильная группа появляется в результате восстановления второй молекулы CO2 до CO, катализируемого CO-дегидрогеназой. Метальные и карбоксильные группы связываются в реакциях трансметилирования и транскарбоксилирования с образованием активированной уксусной кислоты. Процесс осуществляется при участии уникальных ферментов. Из ацетил-КоА, в результате восстановительного карбоксилирования образуется пируват и далее фосфоенолпировиноградная и щавелевоуксусная кислоты, которые служат предшественниками аминокислот и сахаров. Пути фиксации CO2ацетогенными эубактериями и метаногенными архебактериями различаются коферментами и некоторыми частными реакциями.

Рис. 107. Схема начальных этапов метаболизма CO2 у Мethanobaircteus thermoautotrophicum: X1-COOH — карбоксипроизводное; X1-CHO — формилпроизводное; X2-CH2 — метиленпроизводное; X2-CH3 — метилпроизводное; Ф1 — метилредуктазная система; Ф2 — CO-дегидрогеназа; ФЕП — фосфоенолпировиноградная кислота; ФГК — фосфоглицериновая кислота; ФГА — фосфоглицериновый альдегид; Ф-6-Ф — фруктозо-6-фосфат; ЩУК — щавелевоуксусная кислота; КоМ-S-CH3 — метилкофермент М
Биосинтез метана. Восстановление CO2 до CH4 требует переноса 8 электронов. Образующиеся на этом пути промежуточные продукты находятся не в свободном состоянии, а остаются связанными с переносчиками. Согласно предложенной модели на первом этапе CO2 связывается с переносчиком углерода, образуя карбоксипроизводное (X1-COOH), которое восстанавливается до формилпроизводного (X1-CHO). Второй этап метаногенеза включает перенос формильной группы на другой переносчик (Х2), который проводит C1-группу через две последовательные восстановительные реакции, приводящие к образованию метилпроизводного (X2-CH3). На уровне образования метиленпроизводного (X2-CH2) в процесс метаногенеза включается экзогенный формальдегид. Соединения, содержащие метильные группы (CH3OH, CH3COOH, CH3NH2 и другие метиламины), подключаются на уровне метилпроизводного. В этой же точке происходит разветвление анаболических и катаболических путей. Функция X2 у метаногенов напоминает функцию тетрагидрофолата у ацетогенных эубактерий.
На третьем конечном этапе метаногенеза, наиболее изученном, метильные группы с переносчика поступают на кофермент М (КоМ-SH). Образуется метил-КоМ. Далее следует его восстановление, сопровождающееся распадом комплекса и выделением CH4. Обе реакции катализируются метилредуктазной системой, представляющей сложный мультиферментный комплекс, в состав которого помимо фермента входят кофермент М, фактор F430. Для активности системы необходимы АТФ, ионы Mg2+ и еще не идентифицированные кофакторы.
Экология и роль в природе. Метаболические свойства метанобразующих бактерий (строгий анаэробиоз, зависимость от ограниченного набора ростовых субстратов, и в первую очередь от молекулярного водорода) определяют их распространение в природе. Обычными местами обитания этих бактерий является анаэробная зона разных водоемов, богатых органическими соединениями. Они обнаруживаются в иловых отложениях озер и рек, в болотах и заболоченных почвах, в осадочных слоях морей и океанов. Метанобразующие бактерии — обитатели пищеварительного тракта животных и человека, а также важный компонент микрофлоры рубца жвачных животных.
Не нашли, что искали? Воспользуйтесь поиском: