
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Неформальная кинетика цепных реакций термолиза (пиролиза) этана
Существующие в настоящее время методы составления кинетических зависимостей (моделей) химических процессов можно подразделить на 2 группы: методы, лишенные теоретического обоснования и показывающие лишь, чему количественно равна скорость реакции при тех или иных условиях (эмпирическая или формальная зависимость), и методы, базирующиеся на теоретическом и экспериментальном обосновании механизма протекания реакций (неформальные детерминированные кинетические зависимости). Очевидно, более целесообразны детерминированные методы. Однако они требуют установления действительного механизма протекания реакций. В настоящее время более или менее однозначно установлен механизм лишь для немногих преимущественно простых химических реакций. В большинстве случаев известны лишь общие закономерности по химизму и механизму реакций, как, например, в процессах термолиза или катализа нефтяного сырья. Для таковых процессов можно составить детерминированные кинетические уравнения, включающие сотни и более дифференциальных или алгебраических уравнений. Однако их решение даже с применением ЭВМ представляется чрезмерно сложной и практически неразрешимой задачей.
В ряде случаев в кинетических исследованиях вынужденно пользуются полудетерминированными методами, когда из общих закономерностей механизма устанавливаются наиболее значимые или лимитирующие в данных условиях стадии суммарного процесса химических превращений.
12*
Рассмотрим неформальную кинетику радикально-цепных реакций термолиза нефтяного сырья на примере этана (предложенную Р.З.Магарилом). При пиролизе этана протекают следующие элементарные реакции:
Инициирование цепи
к,. 1С2Н6-»2СН3.
Передача цепи
2. СН3 + С2Н6 % СН4 + С2Н5.
Звено цепи
З.СДчОД+Н-.
4. Н+С2Нв 4 Н2 +C2HS.
Обрыв цепи
S.CjHs+ff-X^+Hj.
Чередование элементарных реакций (3) и (4) дает реакцию распада этана по стехиометрическому уравнению
С2Н6 = С2Н4+Н2.
В продуктах пиролиза будет присутствовать и метан, образующийся по реакции (2). Для простоты в предложенном механизме пиролиза этана не учтено образование ацетилена и более высокомолекулярных газообразных и жидких ароматизированных продуктов. Для облегчения решения системы кинетических уравнений примем допущение, что $г=0.
Для этана и каждого из трех радикалов можно записать следующую систему уравнений скорости:
"хн4 iCCjHe+k2CCjH6 сн3+к4СС2Н(,Сн., v'-o)
"chj^kjCc^—k2Cc Hj^-cHjj ('•')
"^с2н5 =k2CCju6C ch3— kjC c2H5+k4CC2HsCH.-kJCH.Cc2Hs» ('««»)
™№=ЩРс2ия~ ^С^н^Сн.—k5CH.CCiHj, ('•9)
При установившемся стационарном режиме скорости образования и расходования промежуточных веществ - радикалов будут равны нулю, то есть \Уён = О» W£ н = 0 и WH. = 0.
Тогда
2kiCC2He= kjCc^CcH^. (7.10)
к2СС2н6Ссн3+к4ССгНбСн.=к3Сс2И5 + ksCij.CcjjHj. (7.11)
кз^с^^к^с^Сн.+ЦСн.С,^]!^ (7.12)
Суммируя (7.10), (7.11) и (7.12), получим
kiC-c2H6 = I^Ch.C- С2н5. (7.13)
Из уравнения (7.13) следует, что скорость реакций инициирования цепей принудительно равна скорости реакций (реакции) их обрыва.
В уравнении (7.12) членом kjC,,. C£ H как произведением двух малых концентраций радикалов можно пренебречь по сравнению с к«С-с.н, Сн.:
кзСС;гн5—*t4^--c2H6CH.
(7.14)
Из (7.13) и (7.10) следует, что к, Сс н и к2 Сс н С^ являются малыми величинами порядка kjC,,. Сс н и ими в уравнении (7.6) также можно пренебречь.
Тогда уравнение расходования этана примет более простой вид
| W, |
| с2н6"к4Сс2Н(.Сн. |
(7.15)
Решая совместно уравнения (7.13) и (7.14) относительно Сн. получим
1/2
Сн =
чк4к5
(7.16)
Подставляя (7.16) в (7.15), получим
| CcjH, |
Л=К"СсЛ=
.1/2
(7.17)
Таким образом, находим, что цепной процесс распада этана описывается кинетическим уравнением первого порядка. Оно отличается от уравнения формальной кинетики для мономолекулярной необратимой реакции тем, что кажущаяся константа скорости (К") пиролиза этана является функцией констант отдельных элементарных реакций этого процесса.
7.2.5. Химизм газофазного термолиза нефтяного сырья
Термолиз алканов приводит преимущественно к образованию более термостойких низкомолекулярных алкенов и алканов. Из алканов наибольшей термостабильностью обладает метан. Его термическая деструкция термодинамически возможна при температуре выше 560 °С. С заметной скоростью распад метана протекает при температуре выше 1000°С. Высокая термостабильность метана объясняется тем, что в его молекуле отсутствуют связи С-С, энергия разрыва которых меньше, чем для связей С-Н. При высокотемпературном пиролизе метана, кроме водорода (и пироуглерода), образуются этилен, этан, ацетилен и арены. Синтез этих продуктов можно выразить следующей схемой:
2 СН, —> HL+2CH, —> 2Н.+ 2СН, —»• ЗН+2СН —> 4Н2+2С
U U U
с2н, с2н4 с,н,
Ароматические углеводороды образуются в результате вторичных реакций синтеза из ацетилена и этилена.
Этан менее устойчив, чем метан: его деструкция начинается при температуре = 500°С. При пиролизе этана образуются, как показано в § 7.3.4, преимущественно этилен и водород, а также метан и жидкие продукты, богатые аренами и алкенами.
Пропан и бутан термически менее устойчивы, чем этан. Пропан начинает разлагаться при 460 °С, а я-бутан и изобутан - около 435°С. Основные направления пиролиза пропана:
с,н,
с3н,+ н2
-> С2Н4+СН4
-»• 1/2 СН4+ 1/2 С,Н,+ 1/2 С,Н,
Все другие продукты пиролиза пропана (бутадиен, ацетилен, ароматика и др.) являются, несомненно, продуктами вторичного происхождения.
Начиная с бутана, при термолизе алканов преобладающим становится распад по связи С-С. Относительная скорость их термолиза возрастает с увеличением молекулярной массы, что обусловливается уменьшением энергии разрыва С-С-связей по мере приближения к середине цепи и увеличения степени разветвленности молекул.
В процессе пиролиза /r-бутана преобладают следующие 2 реакции его распада:
с4н„
с,н4+с2н,
СН.+ СН,.
Характерно, что чем выше температура пиролиза бутана, тем больше отодвигается место его распада по С-С-связи к краю молекулы. На это указывает непрерывное возрастание содержания метана в газообразных продуктах реакции вплоть до 900°С. Аналогичные реакции распада характерны для термолиза более высокомолекулярных алканов. Для них при умеренных температурах (400 - 500 °С) наблюдается симметричный разрыв молекулы с образованием оле-фина и парафина приблизительно одинаковой молекулярной массы. При более высоких температурах в продуктах их термолиза обнаруживаются низшие алканы и высокомолекулярные алкены и арены, вероятно, как результат вторичных реакций.
Алкены характеризуются ввиду наличия двойной связи высокой реакционной способностью в реакциях присоединения, но повышенной, по сравнению с алканами, термостойкостью в отношении реакций распада. Этилен из алкенов наиболее устойчивый. Он всегда содержится в продуктах термолиза нефтяного сырья как первичный и вторичный продукт их превращений. По термической стабильности он занимает промежуточное положение между метаном и этаном. Термический распад этилена заметно начинается при температуре 660 °С. При 400 - 600°С в основном протекает его полимеризация;
2С2Н4 — > С4Н8.
В тех же условиях в продуктах пиролиза этилена содержатся высокомолекулярные олефины - продукт сополимеризации бутиле-нов с этиленом. При температурах 600 °С и выше в продуктах термолиза этилена появляются бутадиен и водород в результате дегидрирования бутена-1.
Оптимальная температура образования диенов при пиролизе этилена - 750 °С. При температурах выше 900°С бутадиен в продуктах пиролиза исчезает, вероятно, превращаясь по диеновому синтезу в арены:
Пропилен по термической стабильности уступает этилену и при термолизе образует метан и этилен:
сн3-сн=сн2 — > сн3 + сн2=сн — > сн4+ сн2=сн,.
Термолиз бутиленов приводит к образованию метана, пропилена и бутадиена по реакциям:
С4Н8— > СН2=СН-СН=СН2+Н2;
C4Hg+H2 ---- ^ СН4+СзНв.
При этом одновременно начинается интенсивное образование ароматизированных жидких продуктов.
В процессе термолиза высших алкенов при умеренных температурах основной реакцией является полимеризация. При повышении температуры развивается реакция распада по С- С-связи (то есть обратная реакции полимеризации). С малой скоростью происходит также изомеризация алкенов с образованием более стабильных симметричных олефинов.
С увеличением молекулярной массы алкенов возрастает тенденция к разрыву С - С-связи. Для высокомолекулярных алкенов наличие двойной связи практически не влияет на термостойкость алкенов, и по устойчивости они становятся близкими алканам с тем же углеродным атомом.
Нафтены при термолизе более стабильны, чем соответствующие алканы. Наиболее устойчивыми среди нафтенов являются циклопен-тан и циклогексан. Реакции термолиза незамещенных циклоалка-нов протекают по нецепному механизму посредством разрыва одной из С-С-связей и образования бирадикала, который далее распадается на стабильные молекулы:
 Q __,. сн2-(сн,)ге:на
Q __,. сн2-(сн,)ге:на
зс,н4
-*с2н4+с4н,
С,Н.
Дегидрирование незамещенных цикланов по цепному механизму не происходит, так как по сравнению с ним распад с образованием бирадикала протекает со значительно большей (на несколько порядков) скоростью. Алкилнафтены при термолизе ведут себя, как алканы: преимущественно распадаются боковые цепи по радикально-цепному механизму.
Бициклические нафтены при 600 °С и выше подвергаются деци-клизации, деалкилированию и дегидрированию:
ОЗ-*0С+с>н'+2Н'!
Термолиз ароматических углеводородов. Термостойкость аренов зависит от наличия алкильных цепей в их молекуле. Арены, имеющие С-С-связь, сопряженную с кольцом, распадаются легче алканов преимущественно по (3-правилу. Основным направлением их превращения является крекинг алкильных цепей и деалкилирование по радикально-цепному механизму с участием алкильных радикалов.
Незамещенные (голоядерные) и метилзамещенные арены значительно более термоустойчивы, чем алканы. При термолизе они преимущественно подвергаются дегидроконденсации.
Бензол конденсируется по цепному механизму по следующей схеме:
свнв —>c„hs+ н-
свн4 + с,нв->с,н5-свнв
с.н.-с.н.-^с.н^-с.н.+ н-
Н-+С.Н, ->Ha + CHs
2 С.Н, -> С„Н1в + Н2
Аналогично происходит дегидроконденсация нафталина:
2 С10Н8 — > С10Н7-С10Н7+Н1.
В результате конденсации бензола и нафталина образуются ди-фенил, динафтил, а также более высококонденсированные арены:
| fY*\ | -н, |
| kXJ^ | |
| нафталин ч |

динафтил перилен
Ароматические углеводороды накапливаются в жидких продуктах термолиза тем в больших количествах, чем выше температура процесса. При пиролизе они являются главной составной частью так называемой смолы пиролиза.
Термолиз смеси углеводородов. Цепные реакции, протекающие при термолизе углеводородов.всегда взаимозаменяемы. Инициирование в радикально-цепных процессах термолиза является самой энергоемкой и, следовательно, лимитирующей стадией. Дальнейшие превращения радикалов происходят значительно меньшими энергиями активации. Термолиз смеси углеводородов, по сравнению с индивидуальными углеводородами, во многих случаях протекает с большей скоростью вследствие увеличения скорости инициирования активными радикалами, которые не всегда могут образоваться при распаде отдельных классов углеводородов. Отдельные углеводороды, например нафтены, распадающиеся в чистом виде по нецепному пути из-за малой скорости инициирования, в смесях могут превращаться по цепному механизму. В качестве инициаторов цепных реакций могут участвовать и отдельные продукты, образующиеся при термолизе углеводородных смесей.
Основные выводы по химизму газофазного термолиза различных классов углеводородов сводятся к следующему.
1. Алканы подвергаются реакциям распада на предельные и непредельные углеводороды. Молекулярная масса полученных углеводородов постоянно снижается за счет последовательного крекинга.
2. Алкены полимеризуются и вступают в реакцию деструктивной полимеризации. В меньшей степени выражена реакция деполимеризации. Возможна также реакция циклизации.
3. Цикланы и арены претерпевают реакции деалкилирования алкильных цепей, образуя алканы, алкены и цикланы с короткой боковой цепью. Шестичленные цикланы дегидрируются в арены, а последние подвергаются поликонденсации, образуя высокомолекулярные жидкие продукты.
Из вышеизложенного следует, что при термолизе нефтяного сырья протекает множество консекутивных реакций и получаются продукты чрезвычайно сложного состава. Исследовать ход превращений и конечную судьбу каждого компонента смеси не представляется возможным. Несмотря на это, зная средний состав сырья, можно приблизительно прогнозировать групповой (не индивидуальный) состав конечных продуктов термолиза.
7.2.6. Краткая характеристика сырья термодеструктивных процессов
В качестве сырья термодеструктивных процессов нефтепереработки, кроме пиролиза, используются остатки прямой перегонки (мазуты, полугудроны, гудроны), термического крекинга, пиролиза (смолы), деасфальтизации (деасфальтизат или асфальтит) и высо-кокипящие ароматизированные концентраты и газойли, получаемые на основе дистиллятных продуктов (экстракты масляного производства, тяжелые газойли каталитического крекинга, коксования, дис-тиллятные крекинг-остатки и др.). В процессах пиролиза наилучшим видом сырья являются парафиновые углеводороды, дающие максимальный выход олефинов: газообразные (этан, пропан, бутан и их смеси) и жидкие (низкооктановые бензины и керосино-газойлевые фракции). Тяжелые нефтяные остатки (ТНО) представляют собой исключительно сложную многокомпонентную и полидисперсную по молекулярной массе смесь высокомолекулярных углеводородов и гетеросоединений, включающих, кроме углерода и водорода, серу, азот, кислород и металлы, такие, как ванадий, никель, железо, молибден и др. Основными компонентами первичных (нативных) ТНО являются масла, смолы (мальтены) и асфальтены. Во вторичных ТНО, подвергнутых термодеструктивному воздействию, могут присутствовать, кроме перечисленных компонентов, карбены и карбоиды.
Качество ТНО как сырья термодеструктивных (а также каталитических) процессов, кроме группового их состава, определяется в значительной степени и содержанием в них гетеросоединений. Как правило, с утяжелением нативных ТНО практически все основные гетероатомные элементы концентрируются в высокомолекулярной их части. Содержание гетеросоединений в ТНО колеблется в широких пределах в зависимости от качества исходной нефти, глубины отбора и технологии получения остатков.
Основными типами сернистых соединений в ТНО являются высокомолекулярные сульфиды с углеводородной частью парафинового, нафтенового, ароматического и смешанного строения, а также гомологи тиофанов и тиофенов. Молекулярная масса сернистых соединений составляет 250 -10000. Основная часть сернистых соединений в ТНО связана с ароматическими и смолис-то-асфальтеновыми структурами, в состав которых могут входить и другие гетероатомы. Проявляется следующая закономерность в распределении гетеросоединений: в нативных ТНО с высоким содержанием смол и асфальтенов (то есть с высокой коксуемостью) содержится больше сернистых, азотистых, кислородных и металлоорганических (преимущественно ванадия и никеля)соединений.
Содержание азота в ТНО составляет 0,2 - 0,6 % масс. Установлено, что азотсодержащие соединения в ТНО относятся преимущественно к структурам с третичным атомом азота. Среди них преобладают алкил- и циклоалкилпроизводные пиридинов, хинолинов, акридинов и нейтральные соединения типа пиррола, индола и кар-базола. В остатках высокосернистых нефтей распределение основных азотистых соединений примерно следующее (в % от общего их содержания):
Хинолины и их нафтеновые гомологи 50-70
Бензхинолины и их нафтеновые гомологи 25—40
Бензтиозолы и их нафтеновые гомологи 7-15
'■'■■■■''*■■' Кислородные соединения в ТНО входят в основном в состав смол и асфальтенов.
Основная часть металлоорганических соединений концентрируется также в смолисто-асфальтеновых компонентах ТНО. В масляной части ванадий практически полностью отсутствует, а часть ни-
(. 364
Таблица 7 Л
Характеристика остатков некоторых нефтей России
| Показатель | Мазуты (> 350°С) | Гудроны (> 500 °С) | ТКГ | ЭМФ-4 | ||||
| Плотность, г/см3 | ||||||||
| Коксуемость, % масс. | 6,04 | 12,8 | 9,9 | 26,05 | 18,52 | 2,3 | ||
| Содержание, % масс. | ||||||||
| углерода | 85,08 | 84,04 | 85,38 | 85,7 | 85,66 | - | - | |
| водорода | 11,44 | 11,15 | 11,53 | 10,86 | 10,38 | 10,8 | - | - |
| серы | 2,05 | 4,11 | 3,12 | 2,86 | 4,35 | 2,98 | 1,48 | 3,08 |
| азота | 0,25 | 0,41 | 0,36 | 0,4 | 0,63 | 0,44 | - | - |
| Содержание | ||||||||
| металлов, мг/г | ||||||||
| ванадия | 485, | -, | - | |||||
| никеля | . - | - | ||||||
| Групповой | ||||||||
| химический состав, | ||||||||
| % масс. | ||||||||
| Масла, в т.ч. | 85,1 | 74,6 | 70,4 | 48,4 | 93,7 | 95,2 | ||
| парафино- нафтеновые | - | 16,3 | - | - | - | - | ||
| легкие ароматические | 18,4 | - | - | 15,9 | - | - | ||
| средние ароматические | 9,3 | - | - | 7,6 | - | - | >57Д | >74,6 |
| тяжелые ароматические | 26,1 | - | - | 30,6 | - | - | J | J |
| Смолы | 13,2 | 18,1 | 25,1 | 34,4 | 26,3 | 5,9 | 4,8 | |
| Асфальтены | 1,7 | 7,3 | 4,5 | 17,2 | 14,7 | 0,4 | нет | |
| Выход на нефть, % | - | 22+23 | - | - | - |
Примечание: ТКГ - тяжелый газойль каталитического крекинга; ЭМФ-4 -экстракт фенольной очистки четвертой масляной фракции; 1, 2, 3 и 4 - остатки соответственно западно-сибирской, арланской, ромашкинсхой и смеси туймазинской и шкаповской нефтей.
келя присутствует и в дистиллятах. Содержание ванадия в ТНО тем больше, чем выше содержание серы, а никеля - чем выше содержание азота. В ТНО малосернистых нефтей содержание никеля выше, чем ванадия. Установлено, что основное количество ванадия и
никеля представлено в нефтяных остатках в виде металлоорганичес-ких соединений непорфиринового характера (например, 62 и 60 % соответственно в мазуте ромашкинской нефти), а меньшая их часть -в виде металлопорфириновых комплексов (27 и 33 % соответственно).
В табл.7.4 приведены данные, характеризующие качество натив-ных и вторичных остатков некоторых нефтей России.
На практике для оценки качества сырья термодеструктивных процессов, кроме перечисленных в табл.7.4 (плотность, коксуемость, элементный состав, групповой химический состав), пользуются так же такими показателями, как вязкость, температура размягчения, индекс корреляции и др.
7.2.7. Основные закономерности жидкофазного термолиза нефтяных остатков
Жидкофазный термолиз имеет место в таких термодеструктивных процессах нефтепереработки, как термический крекинг, висб-рекинг, пекование и коксование тяжелых нефтяных остатков.
Основной отличительной кинетической особенностью жидко-фазных химических реакций является высокая, превышающая на 2-3 порядка, чем в газофазных, концентрация реагирующих веществ в единице объема реактора. В силу этого проведение реакций в жидкофазном состоянии при атмосферном давлении равносильно проведению их в газовой фазе под давлением порядка 10-100 МПа. Это означает, что в жидкофазных процессах будет значительно выше вероятность столкновения реагирующих молекул, в результате преимущественно ускоряются вторичные бимолекулярные реакции. При этом, однако, низкомолекулярные продукты первичного распада высокомолекулярного сырья и алкильные радикалы в зависимости от условий проведения процесса могут «разлетаться» в газовую фазу и не участвовать во вторичных жидкофазных реакциях. В этих условиях цепной процесс жидкофазного термолиза нефтяного сырья будет осуществляться с участием более высокомолекулярных, так называемых долгоживущих бен-зильных и фенильных радикалов. В результате при равных температурах жидкофазный термолиз углеводородов дает значительно больший выход продуктов конденсации и меньший выход продуктов распада.
На суммарный результат жидкофазного термолиза нефтяного сырья существенное влияние оказывает «клеточный эффект». При газофазном распаде молекулы углеводорода образующиеся радикалы мгновенно разлетаются. В жидкой же фазе радикалы окружены «клеткой» из соседних молекул. Для удаления радикалов на расстояние, при котором они становятся кинетически независимыми частицами, необходимо преодолеть дополнительный активационный барьер, равный энергии активации диффузии радикала из клетки. Тем самым клеточный эффект приводит к изменению энергии активации жидкофазной реакции относительно газофазной, а также стационарной концентрации радикалов.
Из результатов многочисленных исследований зарубежных и отечественных ученых отметим следующие общепризнанные закономерности жидкофазного термолиза нефтяного сырья.
1. Термолиз нефтяного сырья в жидкой фазе протекает через последовательные или параллельно-последовательные стадии образования и расходования промежуточных продуктов уплотнения по схеме: легкие масла — > полициклические ароматические углеводороды — > смйлы — > асфальтены —^ карбены — > карбо-иды —> кокс. При этом на каждой стадии образуются газы и менее низкомолекулярные жидкие продукты по сравнению с образовавшимися промежуточными продуктами уплотнения. Так, при термолизе смол образуются, кроме асфальтенов, масла и газы. Это обстоятельство позволяет процесс термолиза рассматривать как обратимый процесс, хотя вторичные продукты уплотнения по молекулярной структуре не вполне идентичны исходным нативным компонентам сырья.
2. При термолизе ТНО имеют место фазовые превращения групповых компонентов. Так, при осуществлении процессов термодеструкции с образованием кокса в коксующейся системе происходит несколько фазовых переходов: первый связан с образованием и выделением из раствора фазы асфальтенов, а следующий - с зарождением и осаждением не растворимых в ароматических растворителях фазы карбенов, которые затем превращаются в карбоиды и конечный твердый продукт - кокс.
Проведенными за последние два десятилетия специальными (спектральными, микроскопическими и др.) исследованиями (Брукса, Тейлора, Уайта, Хонда, З.И.Сюняева и Р.Н.Гимаева) в продуктах карбонизации органических полимеров, нефтяных и каменноу-
гольных пеков, ароматизированных дистиллятных нефтяных остатков были обнаружены анизотропные микросферические/структуры размером 0,1—20 мкм, обладающие специфическими рвойствами жидких кристаллов и получившие название мезофазы, Это открытие имеет исключительно важное научное и практическое значение и позволяет более точно установить механизм жидкофазного термолиза нефтяного сырья. Мезофаза представляет собой слоистый жидкий кристалл, состоящий преимущественно из конденсированных ароматических структур с числом бензольных (или нафталиновых) колец от 10 до 15, соединенных посредством алкильных или гетеро-алкильных групп (метиленовых, диариловых, аминных, амидных и т.д.), имеет примерно на порядок выше парамагнитность. По мнению З.И. Сюняева, мезофаза - это ассоциаты асфальтенов, образованные за счет межмолекулярных физических сил. С ростом температуры физические силы переходят в химические, и формируется углеродный кристаллит анизатропнои структуры. Нерастворимость части мезофазы обусловливается появлением поперечных связей между плоскоконденсированными структурами. В условиях термолиза (пекования или коксования ТНО) микросферы мезофазы растут за счет подвода молекул из карбонизируемой среды и коалес-ценции мелких сфер с последующим осаждением их за счет разности плотностей анизотропной и изотропной фаз.
3. На интенсивность (скорость) термодеструктивных превращений ТНО существенное влияние оказывает растворяющая способность дисперсионной среды, которая определяет значение так называемой «пороговой» концентрации асфальтенов. Если дисперсионная среда представлена парафино-нафтеновыми углеводородами, обладающими слабой растворяющей способностью (то есть являющимися «плохим» растворителем), асфальтены выпадают из раствора при низких их концентрациях. Наоборот, в среде «хорошего» растворителя, например, полициклических ароматических углеводородов или смол, выпадение асфальтенов происходит только при превыше-' нии значения их пороговой концентрации (с показателем растворяющей способности тесно связано и такое понятие, как «агрегатив-ная устойчивость» сырья или реакционной среды, широко применяемое при объяснении причин и разработке способов защиты против расслоения и закоксовывания змеевиков печей и новых сортов высоковязких топлив, вяжущих, связующих материалов и др.).
4. При Термолизе ТНО растворитель служит не только дисперсионной средой, но и является реагирующим компонентом. К тому же сами асфальтены полидисперсны не только по молекулярной массе, но и по растворимости в данном растворителе. В связи с этим в ходе жидкофазного термолиза непрерывно изменяются химический состав и растворяющая способность дисперсионной среды. По мере уплотнения и насыщения раствора асфальтенами в первую очередь будут выделяться наиболее высокомолекулярные плохо растворимые асфальтены, а затем - асфальтены с более совершенной структурой, мезофаза и кокс.
Останавливая процесс термолиза на любой стадии, то есть регулируя глубину превращения ТНО, можно получить продукты требуемой степени ароматизации или уплотнения, например, крекинг-остаток с определенным содержанием смол и асфальтенов и умеренным количеством карбенов, кокс с требуемой структурой и анизотропией.
Таким образом, можно заключить, что термодеструктивные процессы переработки ТНО, особенно коксования, представляют собой исключительно сложные многофакторные нестационарные гетерогенные и гетерофазные диффузионные процессы со специфическим гидродинамическим, массообменным и тепловым режимом.
7.2.8. Влияние качества сырья и технологических параметров на процесс термолиза нефтяных остатков
Качество сырья. На качество продуктов термолиза наиболее существенное влияние оказывает групповой углеводородный состав сырья, прежде всего содержание полициклических ароматических углеводородов. Групповой состав ТНО определяет свойства как дисперсионной среды, так и дисперсной фазы, а также агрегативную устойчивость сырья в условиях термолиза. При термолизе ароматизированного сырья образовавшиеся асфальтены более длительное время находятся в объеме без осаждения в отдельную фазу и претерпевают более глубокие химические превращения (обрыв боковых цепочек, образование крупных блоков поликонденсированных ароматических структур и т.д.). В результате образуются более упорядоченные карбоиды и кокс с лучшей кристаллической структурой.
Нефтяные коксы с высокой упорядоченностью, в частности игольчатые, получаются только из ароматизированных дистиллятных ви-
дов сырья с низким содержанием гетеросоединений (дистиллятные крекинг-остатки, смолы пиролиза, тяжелые газойли каталитического крекинга, экстракты масляного производства и др.). Ц связи с этим в последние годы значительное внимание уделяется как в России, так и за рубежом проблеме предварительной подготовки сырья для процесса коксования и термополиконденсации.
Временную зависимость процесса термолиза при заданных температуре и давлении можно представить следующим образом (рис.7.2). При термолизе ТНО в начале процесса в результате ра-
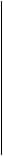 |
| .iv ^ |
100^
| 40 36 | \СЛ' | . | |||
| J32 | См | . | |||
| §28 | ' \ / \ | а | ^~* | ||
| ;*И | V D | СА1У^ | ^W | ||
| %20 Tis | N. " | ||||
| э | |||||
| 0/2 | - | ||||
| !саК | 3^ | ||||
| ^^^^ | |||||
| СА6 |
10 20 30 40 50 60 70 80 90 100 Время, мин
| см | - | too. и 90% | ||
| Cat | < 70 к | |||
| Раз sfi | ~| " | |||
| у» / 1 | »■ | . | во** | |
| М\м | Са | 50 40 | ||
| VwA/ | - | |||
| 1\ ^>_Д ° | -%о_ | 20 10 | ||
| tO 20 30 40 | 50 60 70 | 90 W0 | ||
| Время, мии | ||||
| б |
Рис. 7.2. Изменение концентрации групповых компонентов дистиллятного крекинг-остатка Красноводского НПЗ от продолжительности термолиза при давлении 0,1 МПа и температурах 420 (а) и 490 °С (б): CAi - легкие масла; СА2 -полициклические ароматические углеводороды; Сдз - смолы; Сд4 - асфальтены; Сд5 - карбены; Сдв - карбоиды; СА7 - летучие (данные Г.Г.Валявина)
дикально-цепных реакции распада и поликонденсации происходит накопление в жидкой фазе полициклических ароматических углеводородов, смол и асфальтенов (то есть происходит как бы последовательно химическая «эволюция» групповых компонентов). Признаком последовательности протекания сложных реакций в химической кинетике общепринято считать наличие экстремума на кинетических кривых для концентрации промежуточных продуктов. Как видно из рис.7.2, при термолизе ТНО таковые экстремумы имеются для полициклических ароматических углеводородов, асфальтенов и карбенов. Отсутствие экстремума для смол объясняется высоким их содержанием в исходном сырье. В дальнейшем по мере накопления
в системе уромежуточных продуктов уплотнения происходят два фазовых перехода в жидкой среде. Сначала из карбонизирующегося раствора при достижении пороговой концентрации выделяется фаза асфальтенов, затем в этой среде зарождается фаза анизотропной кристаллической жидкости - мезофаза. Последующая длительная термообработка асфальтенов в растворе в молекулярно-диспер-гированном состоянии способствует более полному отщеплению боковых заместителей и повышению доли ароматического углеводорода в структуре молекул асфальтенов. Это создает предпосылки к формированию мезофазы с более совершенной структурой, что, в свою очередь, приводит при дальнейшей термообработке к улучшению кристаллической структуры конечного продукта - кокса.
Влияние температуры. Поскольку энергии активации отдельных реакций термолиза различаются между собой весьма существенно, то температура как параметр управления процессом позволяет обеспечить не только требуемую скорость термолиза, а прежде всего регулировать соотношение между скоростями распада и уплотнения и, что особенно важно, между скоростями реакций поликонденсации, тем самым свойства фаз и условия кристаллизации мезофазы. При этом регулированием продолжительности термолиза представляется возможным обрывать на требуемой стадии «химическую эволюцию» в зависимости от целевого назначения процесса. С позиций получения кокса с лучшей упорядоченностью структуры коксование сырья целесообразно проводить при оптимальной температуре. При пониженных температурах ввиду малой скорости реакций деструкции в продуктах термолиза будут преобладать нафтено-арома-тические структуры с короткими алкильными цепями, которые будут препятствовать дальнейшим реакциям уплотнения и формированию мезофазы. При температурах выше оптимальной скорости реакций деструкции и поликонденсации резко возрастают. Вследствие мгновенного образования большого числа центров кристаллизации коксующийся слой быстро теряет пластичность, в результате чего образуется дисперсная система с преобладанием мелких кристаллов. Возникающие при этом сшивки и связи между соседними кристаллами затрудняют перемещение и рост ароматических структур. Более упорядоченная структура кокса получается при средних (оптимальных) температурах коксования (= 480 °С), когда скорости реакций деструкции и уплотнения соизмеримы с кинетикой роста мезофазы. Коксующий слой при этом более длительное время оста-
ется пластичным, что способствует формированию крупных сфер мезофазы и более совершенных кристаллитов кокса.,
Влияние давления. Давление в термодеструктивны/х процессах следует рассматривать как параметр, оказывающий значительное влияние на скорость газофазных реакций, на фракционный и групповой углеводородный состав как газовой, так и жидкой фаз реакционной смеси, тем самым и дисперсионной среды. Последнее обстоятельство обусловливает, в свою очередь, соответствующее изменение скоростей образования и расходования, а также молекулярной структуры асфальтенов, карбенов и карбоидов. Анализ большого количества экспериментальных данных свидетельствует, что в процессе термолиза нефтяных остатков с повышением давления:
-почти пропорционально возрастают скорости радикально-цепных газофазных реакций распада с преимущественным образованием низкомолекулярных газов, в результате возрастает выход Н2 и газов С,-С4, а выход суммы летучих продуктов снижается;
-за счет повышения роли физической конденсации низкомолекулярной части продуктов термолиза в дисперсионной среде увеличивается содержание парафино-нафтеновых углеводородов - выса-дителей асфальтенов. При этом пороговая (соответственно и равновесная) концентрация асфальтенов снижается, они раньше выпадают во вторую фазу. В результате выход карбоидов возрастает почти пропорционально давлению. Увеличение выхода карбоидов возможно также за счет образования их, минуя стадию образования асфальтенов, например, адсорбцией полициклических ароматических углеводородов на поверхности мезофазы;
- концентрации полициклических ароматических углеводородов, смол и асфальтенов с ростом давления термолиза изменяются незначительно;
- при термолизе нефтяных остатков с высоким содержанием полициклических ароматических углеводородов с ростом давления несколько улучшается кристаллическая структура карбоидов.
Коэффициент рециркуляции. Газойлевая фракция коксования содержит в своем составе около 30-40 % полициклических ароматических углеводородов. Поэтому рециркуляция этой фракции позволяет ароматизировать и повысить агрегативную устойчивость вторичного сырья и улучшить условия формирования надмолекулярных образований и структуру кокса. Однако чрезмерное повышение коэффициента рециркуляции приводит к снижению произ-
водительности установок по первичному сырью и по коксу и возрастанию эксплуатационных затрат. Повышенный коэффициент рециркуляции (1,4—1,8) оправдан лишь в случае производства высококачественного, например, игольчатого кокса. Процессы коксования прямогонных остаточных видов сырья рекомендуется проводить с низким коэффициентом или без рециркуляции газойлевой фракции.
Не нашли, что искали? Воспользуйтесь поиском: