
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
ИДЕАЛЬНЫЕ ГАЗЫ И ОСНОВНЫЕ ГАЗОВЫЕ ЗАКОНЫ
Под идеальным газом понимают воображаемый газ, в котором отсутствуют силы притяжения между молекулами, а собственный объем молекул исчезающе мал по сравнению с объемом междумолекулярного пространства. Таким образом, молекулы идеального газа принимаются за материальные точки. В действительно существующих газах при высоких температурах и малых давлениях можно пренебречь силами притяжения и объемом самих молекул. Поэтому такие газы можно также называть идеальными.
Основные зависимости, характеризующие соотношения между параметрами идеального газа при некоторых определенных условиях изменения его состояния:
1) если температура газа не изменяется (Т = const), то давление газа и его удельный объем связаны следующей зависимостью (закон Бойля-Мариотта):
 ; (2.1)
; (2.1)
2) если давление газа остается постоянным (р = const), то соотношение между удельным объемом газа и его абсолютной температурой подчиняется закону Гей-Люссака:
 ; (2.2)
; (2.2)
3) при V = const по закону Шарля
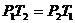 . (2.3)
. (2.3)
Характеристическое уравнение идеального газа или уравнение состояния связывает между собой основные параметры состояния -давление, объем и температуру - и может быть представлено следующими уравнениями:
 ; (2.4)
; (2.4)
 ; (2.5)
; (2.5)
 . (2.6)
. (2.6)
В уравнениях (2.4 - 2.6) приняты следующие обозначения:
р - давление газа, Н/м2;
V - объем газа, м3;
G - вес газа, кг;
v - удельный объем газа, м3/кг;
Vm - объем одного моля газа, м3/моль;
R - газовая постоянная для 1 кг газа, Дж/кг К.
Каждое из этих уравнений отличается от другого лишь тем, что относится к различным весовым количествам газа. Первое - к G кг, второе - к 1 кг; третье - к 1 молю газа.
Газовая постоянная, отнесенная к 1 кг газа, определяется из уравнения

 . (2.7)
. (2.7)
Не нашли, что искали? Воспользуйтесь поиском: