
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
II.1. Классификация теплоемкостей по единицам количества вещества и видам процессов.
Однородными называются системы, у которых в различных их частях свойства одинаковые.
Теплоёмкостью называется количество теплоты, необходимое для изменения температуры единицы количества вещества на 1°.
В зависимости от того, что является единицей измерения количества вещества, различают:
1) массовую (удельную) теплоёмкость  ;
;
2) мольную (молярную) теплоёмкость  ;
;
Примечание:
1 Кмоль – это количество вещества в килограммах, численно равное его молекулярной массе. Например, у сухого воздуха  =28,96 и соответственно его 1 Кмоль имеет массу 28,96 кг.
=28,96 и соответственно его 1 Кмоль имеет массу 28,96 кг.
3) объёмную теплоёмкость 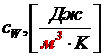 .
.
Так как объём вещества зависит от давления и температуры, то объёмные теплоёмкости в справочной литературе, как правило, даются для нормальных физических условий:
рнорм = 101325 Па
Тнорм = 273,15 К
Перечисленные выше теплоемкости, связаны между собой следующими соотношениями
 (70)
(70)
 (71)
(71)
Из уравнения состояния идеального газа
rнорм = 
Как следует из определения теплоёмкости  , ее величина зависит от вида процессов. Как было показано ранее, теплота
, ее величина зависит от вида процессов. Как было показано ранее, теплота  является функцией процесса, поэтому и теплоемкости также подразделяются по видам термодинамических процессов на изохорную, изобарную, изотермическую, адиабатную теплоемкости и теплоемкость в политропном процессе.
является функцией процесса, поэтому и теплоемкости также подразделяются по видам термодинамических процессов на изохорную, изобарную, изотермическую, адиабатную теплоемкости и теплоемкость в политропном процессе.
Теплоемкости изопроцессов являются теплофизическими характеристиками вещества и их значения содержатся в справочниках, но значения изотермических теплоемкостей и адиабатных не приводятся, потому что из определения теплоемкости  следует:
следует:
cT = сmT = cWT =  ;
;
cs = сms = cWs = 0.
Таким образом для изохорного процесса (V=const) используются:
cv – массовая изохорная теплоёмкость (теплоемкость в изохорном процессе).
сmv – молярная (мольная) изохорная теплоёмкость;
cWv – объёмная изохорная теплоёмкость.
Для изобарного процесса (p=const) используются:
cp – массовая изобарная теплоёмкость.
сmp – молярная (мольная) изобарная теплоёмкость;
cWp – объёмная изобарная теплоёмкость.
Теплоемкость политропного процесса рассматривается далее в разделе IV.
Не нашли, что искали? Воспользуйтесь поиском: