
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Сформулировать законы Авогадро и Дальтона.
Закон Авогадро звучит так: в равных объемах различных газов при постоянных температуре и давлении содержится одинаковое число молекул.
Из Закона Авогадро выводится 2 следствия: 1) Один моль любого газа при одинаковых условиях занимает одинаковый объем; 2) Отношение масс одинаковых объемов двух газов есть величина постоянная для данных газов
Закон Дальтона звучит так: давление смеси газов, не взаимодействующих друг с другом химически, равно сумме парциальных давлений этих газов.
3. Сформулировать законы идеального газа для изопроцессов. Описать уравнения Клапейрона и Клапейрона–Менделеева.
Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным.
1. Изохорический процесс. Закон Шарля. V=const.
Изохорическим процессом называется процесс, протекающий при постоянном объёме. Поведение газа при этом изохорическом процессе подчиняется закону Шарля: при постоянном объёме и неизменных значениях массы газа и его молярной массы, отношение давления газа к его абсолютной температуре остаётся постоянным: P/Т=const.
График изохорического процесса на РV-диаграмме называется изохорой.

Уравнение изохоры:  .
.
2. Изобарический процесс. Закон Гей-Люссака. Р=const.
Изобарическим процессом называется процесс, протекающий при постоянном давлении. Поведение газа при изобарическом процессе подчиняется закону Гей-Люссака: при постоянном давлении и неизменных значениях массы и газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T=const.
График изобарического процесса на VT-диаграмме называется изобарой.

Рис. 1.8
Уравнение изобары: 
3. Изотермический процесс. Закон Бойля – Мариотта. T=const.
Изотермическим процессом называется процесс, протекающий при постоянной температуре.
Поведение идеального газа при изотермическом процессе подчиняется закону Бойля – Мариотта: при постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV=const.
График изотермического процесса на РV-диаграмме называется изотермой.

Уравнение изотермы:  .
.
Уравнение Клапейрона имеет вид:  .
.
Уравнение Клапейрона-Менделеева - связь между числом молей газа, его температурой, объемом и давлением:  .
.
Задача 6
В баллоне объемом 10 л находится гелий под давлением 1 МПа и при температуре 300 K. После того как из баллона было взято 10 г гелия, температура в баллоне понизилась до 290 K. Определить давление гелия, оставшегося в баллоне.
Дано:




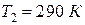
|

|
Решение. По уравнению Менделеева-Клапейрона для газа в начальный момент (до выпускания газа) и в конечный момент (после выпускания газа) имеем:  ,
,  ,
,
где  - молярная масса гелия.
- молярная масса гелия.
Тогда, начальная и конечная массы газа в баллоне равны:
 ,
,  .
.
Так как масса выпущенного газа  , то имеем:
, то имеем:  .
.
Тогда, конечное давление равно:  .
.
Получаем, 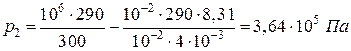 .
.
Ответ. 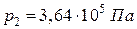 .
.
Ответить на теоретические вопросы:
Не нашли, что искали? Воспользуйтесь поиском: