
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Газдардың молекула – кинетикалық теориясы туралы не айта аласыз? Қандай макроскопиялық шамаларды білесіз? Изопроцестер деген не?
Изопроцестер деп үш параметрдің (Р - қысым, V - көлем, Т - температура) біреуі тұрақты болғандағы басқа екі параметр өзгеретін процесті айтады.
Изопроцестер үшеу: изотермалық, изобаралық, изохоралық.
1. Тұрақты температурада термодинамикалық жүйе күйінің өзгеру процесі Изотермалық процесс (көне грекше: ἴσος - бірдей және көне грекше: θέρμη - жылу) деп атайды.
2. Тұрақты қысымда термодинамикалық жүйе күйінің өзгеру процесі Изобаралық процесс (грек. көне грекше: ἴσος - бірдей, көне грекше: βάρος - ауырлық салмақ) деп аталады.
3. Көлем тұрақты болғанда, температураның өзгеруінен туындайтын газ қысымының өзгеру процесін Изохоралық процесс (грек. көне грекше: ἴσος - бірдей жәнекөне грекше: χώρος - көлем) деп атайды.
Барлық газ заңдары Менделеев-Клайперон теңдеуінен жеңіл алынады.
Изотермалық процесс, изотермиялық процесс – физикалық жүйеде тұрақты температурада жүретін процесс; термодинамикалық күй диаграммасында изотермамен кескінделеді.
Изотермалық процессті жүзеге асыру үшін жүйе, әдетте, термостатқа орналастырылады. Бұл жағдайда термостаттың жылу өткізгіштігі өте үлкен болып келеді де, жүйе температурасының іс жүзінде термостат темп-расынан айырмашылығы болмайды. Изотермалық процесстің мысалына тұрақты температурадағы сұйықтықтың қайнауы не қатты дененің балқуы жатады. Изотермалық процесс кезіндегі идеал газда қысым мен көлемнің көбейтіндісі тұрақты болады. Изотермалық процесс кезінде жүйеге белгілі бір жылу мөлшері беріледі (не одан белгілі бір жылу мөлшері алынады) және оның есебінен сыртқы жұмыс жасалады. Идеал газ үшін ол жұмыстың шамасы мынаған тең:
 , мұндағы
, мұндағы 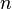 –газдағы бөлшектер саны,
–газдағы бөлшектер саны,  – абсолют температура,
– абсолют температура, 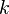 – Больцман тұрақтысы,
– Больцман тұрақтысы, 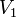 және
және  – газдың бастапқы және соңғы көлемдері.
– газдың бастапқы және соңғы көлемдері.
Егер фазалық ауысу болмаса, онда изотермалық процесс кезінде қатты дененің және көптеген сұйықтықтардың көлемі өте аз өзгереді.
Идеал газ күйінің теңдеуі немесе Менделеев-Клайперон теңдеуі[өңдеу]
Газдың қандай күйде тұрғанын білу үшін оның термодинамикалық параметрлерін, яғни қысымды, температураны, көлемді білу қажет. Термопараметрлердің біреуінің өзгерісі оның басқа параметрлерінің өзгеруіне әкеп соғады. Бұл параметрлерді байланыстыратын теңдеу газ күйінің теңдеуі деп аталады. Осы теңдеуді молекулалы-кинетикалық теорияның негізгі теңдеуін пайдалана отырып, шығарып көрейік. Бізге p = nkТ екені белгілі. Газ молекулаларының концентрациясын n = N/V ескеріп, p = NkT/ V аламыз. Осыдан pV = NkT шығады. Газ молекулаларының санын газдың зат мөлшері арқылы табамыз: N = 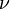 NA = mNA / M. Осыны ескерсек,
NA = mNA / M. Осыны ескерсек,
 .
.
Екі тұрақты санның - Авагадро санының және Больцман тұрақтысының көбейтіндісіне тең шаманың өзі де тұрақты шама. Оны универсал газ тұрақтысы деп атайды:

Универсал газ тұрақтысы дегеніміз - заттың 1 молінің температурасын 1К-ге арттыру үшін оған қанша жылу мөлшерін беру қажет екенін көрсететін физикалық шама. Бұл универсал газ тұрақтысының физикалық мағынасы. Осы айтылғандарды ескерсек, онда идеал газ үшін мына теңдеу орындалады:

Бұл идеал газ күйінің теңдеуі деп аталады. Осы түрде бұл теңдеуді тұңғыш рет ұлы орыс ғалымы Д.И. Менделеев алған, сондықтын ол Менделеев-Клайперон теңдеуі деп аталады. 10 жылдай Ресейде қызмет еткен, атақты француз физигі, Б.П.Клайперон идеал газ күйінің теңдеуін Менделеевтен бұрын (1834 ж.) алды. Идеал газ күйінің теңдеуі физикадағы алғашқы тамаша жалпылау теңдеуі. Ол тәжірибеде тағайындалған бірқатар газ заңдарын жалпылайды. Қандай затты алғанымызға тәуелсіз болатын жалпыланған заңдарды ашу - физика ғылымының мақсаты.
| p | Газдың қысымы (Па) |
| V | Газдың көлемі (м3) |
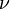
| Зат мөлшері (моль) |
| R | Универсал газ тұрақтысы (Дж/ K ˑ моль) |
| T | Абсолют температура (К) |
| N | Молекулалар саны |
| NA | Авогадро саны (1/ моль) |
| m | Заттың массасы (кг) |
| M | Мольдік масса (кг/ моль) |
Егер күй теңдеуін қалыпты жағдайда идеал газдың бір молі үшін жазатын болсақ, онда ол p = 101325 Па, Т = 273 K, кезінде V = 22.4 л/моль көлем қабылдайды. Сонда
 8,31 Дж/К ˑ моль.
8,31 Дж/К ˑ моль.
Универсал газ тұрақтысы шықты.
Изопроцестер[өңдеу]
Газдарда өтіп жататын көптеген процестердің ішінен газдың берілген массасы үшін қандай да бір термопараметрдің тұрақты болып қалатын кезіндегі процестер изопроцестер деп аталады. Оның 3 түрі бар:
Изотермалық (грек. isos - бірдей және therme - жылу) процесс - тұрақты температура кезінде өтетін процесс. Изопроцестердің ішінен бірінші болып осы изотермалық процесс зерттелді. Ағылшын физигі Р. Бойль 1662 ж. және оған тәуелсіз француз физигі Э. Мариотт тәжірибе жүзінде тұрақты температура кезінде газдың берілген массасы үшін оның қысымының газ алып тұрған көлемге көбейтіндісі тұрақты шамаға тең болатынын тағайындады, яғни pV = const Ірі жазу. Бұл заң Бойль - Мариотт заңы деп аталады.
 .
.
Изобаралық (грек. isos - бірдей және baros - ауырлық салмақ) процесс - тұрақты қысым кезінде өтетін процесс. Француз физигі Гей - Люссак 1802 ж. тәжірибе жүзінде тұрақты қысымда газдың берілген массасы көлемінің температураға сызықты тәуелді болатынын тағайындады, яғни
 .
.
Бұл заң Гей - Люссак заңы деп аталады.
Изохоралық (грек. isos - бірдей және chosa - көлем) процесс - тұрақты көлем кезінде өтетін процесс. бұл процессті француз физигі Ж. Шарль зерттеген. 1787 ж. ол тәжірибе жүзінде тұрақты көлемде берілген газ массасынәң қысымы оның температурасына тура пропорционал болатынын тағайындады, яғни
 .
.
Бұл - Шарль заңы. Шарль өзінің заңын Гей - Люссактан ерте ашты, бірақ кеш жариялады.
Изобаралық процесс – сыртқы тұрақты қысымда физикалық жүйеде өтетін процесс.
Ол термодинамикалық диаграммада изобарамен кескінделеді. Изобаралық процесстің қарапайым мысалына ашық ыдыстағы суды қыздыру, еркін қозғалатын поршені бар цилиндрдегі газдың ұлғаюы жатады. Бұл екі жағдайда да қысым атмосфералық қысымға тең. Изобаралық процесс кезінде идеал газдың көлемі температураға пропорционал болады (қ. Гей – Люссак заңы). Изобаралық процессте, жүйенің жылу сыйымдылығы изохоралық процеске (тұрақты көлемде) қарағанда көбірек болады. Мысалы, идеал газ үшін:
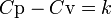 , мұндағы
, мұндағы  және
және  – изобаралық және изохоралық процестердегі бір бөлшекке келетін жылу сыйымдылықтары.
– изобаралық және изохоралық процестердегі бір бөлшекке келетін жылу сыйымдылықтары.
Изобаралық процессте идеал газдың жасайтын жұмысы  -ге тең, мұндағы
-ге тең, мұндағы  – қысым,
– қысым,  – газ көлемінің өзгерісі.
– газ көлемінің өзгерісі.
Изохоралық процесс – физикалық жүйеде тұрақты көлемде жүретін процесс. Ол термодинамикалық күй диаграммасында изохорамен кескінделеді.
Изохоралық процессті көлемі өзгермейтін герметикалық (тұмшаланған) ыдыстағы газдар мен сұйықтықтарда жүзеге асыруға болады. Дене көлемінің өзгеруіне ішкі энергиясының өзгеруі жылудың жұтылуы не шығуы есебінен атқарылады. Температураның өзгеруіне байланысты газдың (сұйықтықтың) қысымы да өзгереді. Изохоралық процесс кезінде идеал газдың қысымы температураға пропорционал (Шарль заңы) болады. Нақты (идеал емес) газда Шарль заңы орындалмайды. Өйткені газға берілген жылудың белгілі бір бөлігі бөлшектердің өзара әсерлесу энергиясын арттыруға жұмсалады. Ал қатты денедегі изохоралық процессті атқару техникалық жағынан едәуір күрделі болып келеді. Сығылғыштығы өте аз қатты денедегі кез келген изотермалық процесті, бірнеше ондаған килобар қысымға дейін, изохоралық процесс деп есептеуге болады.
Термодинамиканың бірінші бастамасы — термодинамикалық жүйелер үшін керек энергияның сақталу заңы; бұл заң бойынша жүйеге берілетін жылу оның ішкі энергиясын өзгертуге және жүйенің сыртқы күштерге қарсы жұмысына жұмсалады.[1]
Дене күйінің барлық энергиясы - микроскопиялық қозғалысының толық түріндегі сыртқы кинетикалық энергиясы Ек және салмақ күші өрісі, электрлі немесе магнит өрісі жағдайындағы потенциалды энергия Еn, сонымен қатар, дене бөлшектерінің құрамдық әрекеттері мен қозғалу энергиясын жасаушы ішкі энергия U қосындыларынан тұрады:
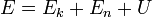
Қаралып отырған жылу динамикалық жүйе шамаланса, онда дененің орталық салмақтық алмасу жылдамдығы өте аз (С=0), яғни қозғалыссыз жұмыстық дене көлемінің өзгеруі туралы сөз болады, сондықтан Ек=0. Айталық, Ер=0 сонымен, бұл жерде толық энергия ішкімен бірдей (E=U), ал жүйе энергиясының өзгеруі - жұмыстық дененің, ішкі энергиясының өзгеруіне келтіреді.
Жылу динамикасының бірінші заңына сәйкес, жұмыстық дененің энергиясы кезінде, қабылданған жағдайға тиісті кезіндегі жүйенің өтуі 1 бастапқы күйінен 2 соңғы мәндеріне артуы, денеге берілген жылулық dQ және мәніне келуі dL істелінген жүйе жұмысына тең: dU=dQ-dL немесе әдетте былай жазу қабылданған -

Сыртқы ортамен әрекеттестігі жоқ болғандағы кезінде (dQ=0 және dL=0), формуладағы dU=0, яғни жүйе энергиясы өзгеріссіз сақталады. Жүйелер қатнасының жекеленген жылулығы үшін, ондағы dQ=0 екені белгілі.

Теңдеу жұмыстық дененің еркінше алынған санды массасы m арналып жазылған, ал меншікті мәндері үшін былай жазылады:

мұндағы q - меншікті жылулық саны; l - меншікті жұмыс; u - меншікті ішкі энергия, q, u, l бірлік өлшемі Дж/кг.
Бұл теңдеу үшін, жылудинамикасының бірінші заңының талдаушы тұжырымдалуын көрсетеді, осыған сәйкес жүйеге жеткізілген жылу, жүйелердің ішкі энергиясына жұмсалады және жұмыстың атқарылуына қарсы денеге түскен сыртқы күш. Олар, қайтымдыға да және сыртқы қайтымсыз процесстер үшін де әділетті. Себебі, қабылданған жағдайдағы жылу алмасуы кезінде, дене мен орта арасының соңғы температура айырмашылығы кезінде, қайтымсыз жылуалмасуына сәйкес келеді.
Қоршаған ортаның жұмыс жүйесін қарастыралық, сыртқы күштердің әрекетінен дене көлемінің өзгеруі жүреді. Механиканың жалпы ережесі бойынша, бұл жұмыс денеге түскен күш көбейтіндісімен, оның жылжуын анықтайды. Егер күш, бет ауданының элементіне әрекет етсе, ол элемент, қысым болады, ал осы элементтің ауданының көбейтіндісінің жылжуы, нормалы бағытпен бетке жатып, сол элементтің беттік көлемі болса, онда элементарлы жұмыс, қоршаған орта жүйесімен жасалу кезіндегі, денекөлемінің шексіз аз өзгеруінің көбейтіндісі ретінде анықталады:

V1 ден V2 дейінгі көлемнің соңғы өзгеруі кезінде:

мұндағы V - көлем, м3.
Газ жағдайының өзгеру процессін зерттеуде, графикалық әдістер (кеңінен пайдаланады) негізінің PV - диаграммасы деп, аталуын кеңінен қолданады.
Дене көлемінің, жұмыстан өзгеруін анықтау жағдайында абцисс өсі бойынша, V шамаларын қояды. Мұндай бейнелерді қолдану, әдетте піспекті қозғалтқыштардың процессін зерттеу кезінде қолданады, мұндағы цилиндр ішіндегі дене көлемінің, піспек жолының жүріп өтуіне, пропорционалды болады.
Газдардың физикалық қасиеттерін зерттеуге статистикалық әдісті қолданайық.
Молекула –кинетикалық теорияның негізгі қағидалары:
1. Барлық заттар бөлшектерден тұрады (молекулалар мен атомдардан);
2. Осы бөлшектер тәртіпсіз, хаостық қозғалыста болады. Бұл қозғалыс жылулық қозғалыс деп аталады;
3. Бөлшектер бір-бірімен өзара әсерлеседі.
Зат бөлшектерінің жылулық қозғалысын қөрнекі түрде көрсететін тәжірибені ағылшын ғалымы Броун жасады. Броун микроскоптың көмегімен сұйықта қалқыған гүл тозаңдарының жылдам, тәртіпсіз қозғалысын бақылады. Осындай зат бөлшектерінің жылулық қозғалысын Броундық қозғалыс деп атайды.
Не нашли, что искали? Воспользуйтесь поиском: