
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Егер газ қысымы өзгермесе, берілген массалы газ үшін көлемнің темпертураға қатынасы тұрақты болады.
Бұл заңды 1802 жылы француз ғалымы Гей - Люссак тэжірибе жүзінде тағайындаған және сондықтан ол Гей - Люссак заңы деп аталады.  қатысқа сәйкес тұрақты қысымда газдың көлемі температураға тәуелді болады, яғни:
қатысқа сәйкес тұрақты қысымда газдың көлемі температураға тәуелді болады, яғни:
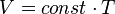
Бұл тәуелділік график түрінде изобара деп аталатын түзумен кескінделеді. Әр түрлі қысымға әр түрлі изобара сәйкес келеді. Қысым артқан сайын, тұрақты температурада Бойль - Мариотт заңы бойынша газдың көлемі кішірейеді. СОндықтан жоғарырақ р2 қысымға сәйкес келетін изобара төменірек р1 қысымға сәйкес келетін изобарадан төменірек жатады. Төменгі температуралар аймағында идеал газдың барлық изобаралары Т=0 нүктесінде түйіседі. Бірақ бұл нақты газдың көлемі шынында да нөлге айналды, ал күй теңдеуі сұйықтарға қолданылмайды. Жылжымалы поршеньді цилиндрдегі газды қыздырғанда оның ұлғаюын изобаралық процесс деуге болады. Онда цилиндрдегі қысымның ұрақтылығы поршеньнің үстіңгі бетіне атмосфералық ауа қысымның әсері арқылы жүзеге асады.
Изохоралық процесс.[өңдеу]
Көлем тұрақты болғанда термодинмикалық жүйе күйінің өзгеру процесін изохоралық деп атайды. Күй теңдеуінен газдың көлемі өзгермеген кездегі кез келген күйінде газ қысымының температураға қатынасы тұрақты болатыны шығады:
 болғанда,
болғанда, 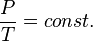
Егер газ көлемі өзгермесе, онда массасы берілген газ үшін қысымның температураға қатынасы тұрақты болады.
Бұл газ заның 1787 жылы француз физигі Ж. Шарль ашқан және мондықтан ол Шарль заңы деп аталады. 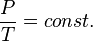 теңдеуіне сәйкес көлем тұрақты болғанда газ қысымы температураға сызықтық тәуелді болады, яғни
теңдеуіне сәйкес көлем тұрақты болғанда газ қысымы температураға сызықтық тәуелді болады, яғни

Бұл тәуелділек графикте түзумен кескінделеді де, ол изохора деп аталады. үрлі көлемге түрліше изохора сәйкес келеді. Температура тұрақты болғанда, Бойль - Мариотт заңына сәйкес, газ көлемі ұлғайғанда оның қысымы азаяды. Сондықтан үлкен V2көлемге төмен жатады.  теңдеуге сәйкес барлық изохоралар Т=0 нүктесінен басталады. Демек, абсолют нөлде идеал газдың қысымы нөлге тең. Кез келген жабық ыдыстағы немесе электр шамындағы газды қыздырғандағы газ қысымының ұлғаюы изохоралық процесс болып табылады. Изохоралық процесс көлемі тұрақты газ термометрлерінде пайдаланылады.
теңдеуге сәйкес барлық изохоралар Т=0 нүктесінен басталады. Демек, абсолют нөлде идеал газдың қысымы нөлге тең. Кез келген жабық ыдыстағы немесе электр шамындағы газды қыздырғандағы газ қысымының ұлғаюы изохоралық процесс болып табылады. Изохоралық процесс көлемі тұрақты газ термометрлерінде пайдаланылады.
Температура» деген ұғымды қалай түсінесіз және қандай температуралық белгілеулер сізге аян? Жылулық құбылыстары, тасымалдың түрлері туралы не айтуға болады?
Температура (лат. temperatura – араластырылуға тиісті, өлшемдес болу, қалыпты күй)[1] – макроскопикалық жүйеніңтермодинамикалық тепе-теңдік күйін сипаттайтын физикалық шама. Егер оқшауланған немесе тұйықталған жүйе термодинамикалық тепе-теңдік күйде болса, онда оқшауланған немесе тұйықталған жүйенің кез келген бөлігінде температура бірдей болады. Ал егер жүйе тепе-теңдік күйде болмаса, онда жылу (энергия) оның температурасы жоғары бөлігінен температурасы төмен бөлігіне қарай ауысып, белгілі бір уақыт өткеннен кейін жүйенің барлық бөліктеріндегі температура өзара теңеседі. Молекула кинетикалық теория тұрғысынан тепе-теңдіктегі жүйенің температурасы сол жүйені құрайтын атомдардың, молекулалардың, т.б. бөлшектердің жылулық қозғалысының қарқындылығын сипаттайды. Мысалы, классикалық статистикалық физиканың заңдарымен сипатталатын жүйе үшін бөлшектердің жылулық қозғалысының орташа кинетикалық энергиясы жүйенің абсолют температурасына тура пропорционал болады. Бұл жағдайда температура дененің жылыну (қызу) дәрежесін сипаттайды. Жалпы жағдайда температура жүйе энергиясының энтропия бойынша алынған туындысымен анықталады және ол әрқашан оң болады. Осылай анықталған температура абсолют температура немесе термодинамикалық шкала температурасы деп аталады. Бірліктердің халықаралық жүйесінде абсолют температураның бірлігіне кельвин (К) қабылданған. Көп жағдайда температураны Цельсий шкаласы (t) бойынша өлшейді. Ал t және Т бір-бірімен: t=T-273,15К теңдігі арқылы байланысқан (мұнда Цельсий градусы кельвинге тең). Дене температурасы термометр арқылы өлшенеді.[2]
Температуралық шкаласы[өңдеу]
Темературалық шкаласы- қалыпты кысым кезінде мұздың еру нүктесі нөл градусқа, ал қайнау нүктесі - 80 градусқ теӊ.
Кельвин температуралық шкаласы[өңдеу]
Кельвин температуралық шкаласы- температура бірлігі ретінде кельвин алынатын термодинамикалык температуралык шкала.
Ремюр температуралық шкаласы[өңдеу]
Ремюр температуралық шкаласы - қалыпты қысымда мұздың еру нүктесі нөл градуска, ал судың кайнау нүктесі 80 градуска сәйкес келетін температуралык шкала. Муздын еру температурсы 0 градуска сайкес келеды.
Фаренгейт темературалық шкаласы[өңдеу]
Фаренгейт темературалық шкаласы - қалыпты қысымда мұздың еру нүктесі 32 градуска, ал судың кайнау нүктесі 212 градуска сэйкес келетін температуралық шкала.
Цельсий темературалық шкаласы[өңдеу]
Цельсий темературалық шкаласы - калыпты кысымда мұздың еру нүктесі нөл градуска, ал судың кайнау нүктесі 100 градуска сәйкес келетін температуралык шкала.
Не нашли, что искали? Воспользуйтесь поиском: