
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Термодинамиканың негізгі заңдары.
Термодинамика заңдылықтары жалпы сипатта қолданылады және заттардың атомдық деңгейдегі құрылымына тәуелді емес. Сондықтан термодинамика ғылым мен техниканың энергетика, қозғалтқыштар, фазалық ауысу, химиялық реакциялар, секілді көптеген салаларында қолданылады.Термодинамиканың физика мен химияның бірқатар салаларында, химиялық технология, аэроғарыштық технология, машина жасау, жасушалық биология, биомедициналық инженерия секілді алуан түрлі салаларда алатын орны ерекше.
Термодинамиканың бірінші бастамасы — термодинамикалық жүйелер үшін керек энергияның сақталу заңы; бұл заң бойынша жүйеге берілетін жылу оның ішкі энергиясын өзгертуге және жүйенің сыртқы күштерге қарсы жұмысына жұмсалады.[1]
Денекүйініңбарлықэнергиясы–микроскопиялыққозғалысыныңтолықтүріндегісыртқыкинетикалықэнергиясыЕкжәнесалмақкүшіөрісі, электрлінемесе магнит өрісіжағдайындағыпотенциалды энергияЕn, соныменқатар, денебөлшектерініңқұрамдықәрекеттері мен қозғалуэнергиясынжасаушыішкі энергия U қосындыларынантұрады:
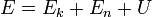
Қаралыпотырғанжылудинамикалықжүйешамаланса, ондадененіңорталықсалмақтықалмасужылдамдығыөте аз (С=0), яғниқозғалыссызжұмыстықденекөлемініңөзгеруітуралысөзболады, сондықтанЕк=0. Айталық, Ер=0 сонымен, бұлжердетолық энергия ішкіменбірдей (E=U), ал жүйеэнергиясыныңөзгеруі–жұмыстықдененің, ішкіэнергиясыныңөзгеруінекелтіреді.
Жылудинамикасыныңбіріншізаңынасәйкес, жұмыстықдененіңэнергиясыкезінде, қабылданғанжағдайғатиістікезіндегіжүйеніңөтуі 1 бастапқыкүйінен 2 соңғымәндерінеартуы, денегеберілгенжылулықdQжәнемәнінекелуіdLістелінгенжүйежұмысынатең: dU=dQ-dLнемесеәдеттебылайжазуқабылданған -

Сыртқыортаменәрекеттестігіжоқболғандағыкезінде (dQ=0 жәнеdL=0), формуладағыdU=0, яғнижүйеэнергиясыөзгеріссізсақталады. Жүйелерқатнасыныңжекеленгенжылулығыүшін, ондағыdQ=0 екенібелгілі.
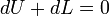
Теңдеужұмыстықдененіңеркіншеалынғансандымассасы m арналыпжазылған, алменшіктімәндеріүшінбылайжазылады:

мұндағы q - меншіктіжылулық саны; l - меншіктіжұмыс; u - меншіктіішкі энергия, q, u, l бірлікөлшемі Дж/кг.
Бұлтеңдеуүшін, жылудинамикасыныңбіріншізаңыныңталдаушытұжырымдалуынкөрсетеді, осығансәйкесжүйегежеткізілгенжылу, жүйелердіңішкіэнергиясынажұмсаладыжәнежұмыстыңатқарылуынақарсыденегетүскенсыртқыкүш. Олар, қайтымдыға да жәнесыртқықайтымсызпроцесстерүшін де әділетті. Себебі, қабылданғанжағдайдағыжылуалмасуыкезінде, дене мен орта арасыныңсоңғы температура айырмашылығыкезінде, қайтымсызжылуалмасуынасәйкескеледі.
Термодинамиканыңекіншібастамасы) — статистикалықнысандардың (мысалы, атомбеидардың, молекулалардың) үлкенсанынантұратынжүйелердіңөзбетіншеықтималдығыаздаукүйденықтималдығымолырақкүйгеауысупроцесін сипаттайтынтабиғаттыңтүбегейлізаңы.Термодинамиканың екінші заңы табиғаттағы процестердің жүру бағытын көрсетеді.
Өзін қоршаған кеңістікте ешқандай қалдық өзгерістер болмайтындай түрде жүретін термодинамикалық процесті қайтымды процесс деп атайды. Қайтымды процесс кезінде термодинамикалық жүйе бастапқы күйіне қайта келеді.
Сыртқы ортада өзгерістер қалатындай түрде жүретін процесті қайтымсыз процесс деп атайды. Қайтымсыз процесс кезінде жүйе бұрынғы күйіне қайтып келмейді. Үйкеліс, кедергі күштерімен жүретін процестер қайтымсыз процесс болып табылады.
Жылу алмасу кезінде жүретін процесс қайтымсыз процесс болып табылады.
Тұйық жүйеде кез келген қайтымсыз процесс жүйенің энтропиясы өсетіндей жүреді (энтропияның өсу заңы).
Термодинамиканың бірінші бастамасы термодинамикалық процестерге энергияның сақталу, айналу заңдарының қолдануға сай етіп береді.
Термодинамиканы 2-ші бастамасы қандай процестер табиғата мүмкін, қандайы процестер мүмкін емес екендігін көрсете отырып термодинамикалық процестердің өту бағытын анықтайды.
Термодинамиканың екінші бастамасының энтропияның өсуі заңына баламалы тағыда екі формулировкасы бар.
1) Кельвин бойынша: нәтижесі жалғыз ғана қыздырғыштан алған жылуы оған баламалы жұмысқа айналу болып табылатын дөңгелек процесс мүмкін емес.
2) Клаузиус бойынша: төмен қыздырылған денеден, жоғары қыздырылған денеге жылудың берілуі жалғыз нәтижесі болып саналатын дөңгелек процесс мүмкін емес.
Термодинамиканың үшінші бастамасы — абсолюттік нөлге жуық температура маңында, реакцияның жылу эффектісі мен максимал жұмысты сипаттайтын қисық сызықтар өзара бірігіп кетеді, ал олардың ортақ жанамасы температуа осіне параллель болады дейтін, химиялық реакцияларға тән эксперименттік нәтижелерді қорытындылаудан туатын постулат.
Термодинамиканың үшінші бастамасы – Нернст-Планк теориясы Кельвиндік нольде (абсолюттік ноль) термодинамикалық жүйенің жағдайын постулаттайды: тепе-теңдік күйде барлық дененің энтропиясы температураның Кельвиндік нолге жуықтаутау шамасына қарай нольге ұмтылады.

 болғанда, жылусыйымдылықтар
болғанда, жылусыйымдылықтар  және
және  нолгетеңболғандықтан
нолгетеңболғандықтан
 ,
,  ,
,  ,
,
 .
.
Не нашли, что искали? Воспользуйтесь поиском: