
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Гетерофункциональные производные бензола как лекарственные средства
Неразрывная связь химии и медицины отчетливо проявляется в области создания и использования лекарственных средств. Еще в XVI в. основатель ятрохимии Парацельс утверждал, что «настоящая цель химии заключается не в изготовлении золота, а в приготовлении лекарств». С давних времен эмпирическим путем происходил отбор биологически активных органических соединений, и появление ряда лекарственных средств часто было обязано случаю. В настоящее время все синтезируемые соединения должны проходить испытания на биологическую активность (биологический скрининг). Это важно для выявления общих закономерностей взаимосвязи структуры соединений с их биологической активностью. Проблема «струк- тура-свойство» служит фундаментом целенаправленного создания эффективных лекарственных средств.
В последние десятилетия появилось множество новых лекарственных средств. Однако большое значение сохраняют некоторые группы известных ранее лекарственных средств, в частности с бензольным ядром в качестве структурной основы.
Сам бензол может быть причиной острых и хронических отравлений. Он оказывает раздражающее действие на кожу, его пары в большой концентрации вызывают возбуждение, расстройство дыхания.
Монофункциональные производные бензола в большинстве случаев также обладают выраженными токсическими свойствами. Фенол, анилин, галогенопроизводные ароматического ряда служат исходными или промежуточными продуктами крупнотоннажной химической промышленности. В связи с этим необходимо учитывать их токсическое действие.
Бензойная кислота. Применяется в виде натриевой соли как отхаркивающее средство. В свободном виде бензойная кислота встречается в некоторых смолах и бальзамах, а также в клюкве, бруснике, но чаще
содержится в связанном виде, например в виде N-бензоильного производного аминоуксусной кислоты, называемого гиппуровой кислотой. Эта кислота образуется в печени из бензойной и аминоуксусной (глицин) кислот и выводится с мочой. В клинической практике по количеству гиппуровой кислоты в моче больных (после приема бензоата натрия) судят об эффективности обезвреживающей функции печени.

и-Аминофенол и его производные. Как гетерофункциональное соединение п -аминофенол может образовывать производные по каждой функциональной группе в отдельности и одновременно по двум функциональным группам. Сам п-аминофенол ядовит; интерес для медицины представляет его производное - парацетамол, оказывающий анальгетическое (обезболивающее) и жаропонижающее действие.

и-Аминобензойная кислота (ПАБК) и ее производные. Эфиры ароматических аминокислот способны в той или иной степени вызывать местную анестезию. Особенно заметно это свойство у пара -производных. В медицине используют анестезин (этиловый эфир ПАБК) и новокаин (2-диэтиламиноэтиловый эфир ПАБК). Новокаин при- меняют в виде соли (гидрохлорида), что связано с необходимостью повышения его растворимости в воде.

Салициловая кислота и ее производные. Салициловая кислота (см. 8.1) относится к группе фенолокислот. Как соединение с орто- расположением функциональных групп она декарбоксилируется при нагревании с образованием фенола.
Салициловая кислота умеренно растворима в воде, дает интенсивное окрашивание с хлоридом железа(Ш), на чем основано качественное обнаружение фенольной гидроксильной группы. Салициловая кислота проявляет антиревматическое, жаропонижающее и антигрибковое действие, но как сильная кислота (рKа 3,0) вызывает раздражение желудочно-кишечного тракта и поэтому применяется только наружно. Внутрь применяют ее производные - соли или эфиры.
Салициловая кислота способна образовывать производные по каждой функциональной группе. Практическое значение имеют салицилат натрия, сложные эфиры по карбоксильной группе - метилсалицилат, фенилсалицилат (салол), а также по гидроксильной группе - ацетилсалициловая кислота (аспирин).

Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике. В связи с этим салол используют также в качестве материала для защитных оболочек некоторых лекарственных средств, нестабильных в кислой среде желудка.
Салициловая кислота впервые была получена путем окисления салицилового альдегида, содержащегося в растении таволге (род Spireae). Отсюда и ее первоначальное название - спировая кислота, с которым связано название аспирин (начальная буква «а» обозначает ацетил). Ацетилсалициловая кислота в природе не найдена.
Из других производных салициловой кислоты большое значение имеет и -аминосалициловая кислота (ПАСК) как противотуберкулезное средство. ПАСК является антагонистом п -аминобензойной
кислоты, необходимой для нормальной жизнедеятельности микроорганизмов.

Сульфаниловая кислота и ее производные. Сульфаниловая (п-аминобензолсульфоновая) кислота существует в виде диполярного иона.

Амид сульфаниловой кислоты (сульфаниламид), известный как стрептоцид, является родоначальником группы лекарственных средств, обладающих антибактериальной активностью и называемых сульфаниламидами.
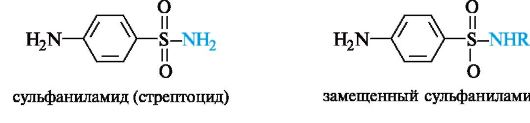
Все сульфаниламиды содержат сульфонамидную группу -SO2NH2.Замена ее другими группами приводит к потере антибактериальной активности. Установлено, что аминогруппа в пара-положении должна оставаться незамещенной, а в бензольное кольцо нельзя вводить дополнительные заместители, так как они снижают антибактериальную активность соединения.
В поиске эффективных антибактериальных средств было синтезировано более 10 тыс. производных сульфаниламида. Однако лишь несколько десятков из них нашли практическое применение. Наибольшую активность проявляют те производные, у которых радикал R имеет гетероциклическую природу
6.4. Иллюстративный материал слайды с уравнениями химических процессов по теме лекции, таблицы с показателями качества рассматриваемых препаратов.
Литература
Основная литература:
1. Арзамасцев А.П. Фармацевтическая химия: учебное пособие, 3-е изд., испр. – М.: ГЭОТАР-Медиа, 2008. – 640 с.
2. Беликов В.Г. Фармацевтическая химия: учебное пособие, 2-е изд. – М.: МЕДпресс-информ, 2008. – 616 с.
3. Руководство к лабораторным занятиям по фармацевтической химии: Э.Н. Аксенова, О.П. Андрианова, А.П. Арзамасцев и др. – М.: Медицина, 2001. – 384 с.
4. Государственная фармакопея Республики Казахстан: первое издание. – 1 том. – Астана: Изд. дом «Жибек жолы», 2008. – 592 с.
Дополнительная литература:
1. Анализ лекарственных смесей / Под ред. А.П. Арзамасцева, В.М. Печенникова, Г.М. Родионова и др. – М.: Компания Спутник+, 2000. – 275 с.
2. Арыстанова Т.А., Ордабаева С.К. Стандартизация лекарственных средств: учебное пособие. – Алматы, 2002. – 98 с.
3. Государственный реестр лекарственных средств. – М.: 2001. – 1277 с.
4. Бейсенбеков А.С., Шаншаров Г.Б., Галымов Е.Г., Бейсенбеков Н.А. Стандартизация лекарств: учебное пособие. – Алматы, 2008. – 167 с.
5. Государственная фармакопея СССР: Х издание. – М.: Медицина, 1968. – 1079 с.
6. Государственная фармакопея СССР: XI издание. – М.: Медицина, 1987. – Т.1. – 334 с.
7. От субстанции к лекарству: учебное пособие / Под ред. чл.-корр. НАН Украины В.П. Черных. – Харьков: изд-во НФаУ «Золотые страницы», 2005. – 1244 с.
Контрольные вопросы
1. Приведите формулы молочной, яблочной, лимонной, изолимонной, винной, β-гидроксимасляной кислоты. Укажите основность этих соединений и их медико-биологическое значение.
2. Постройте все возможные изомеры 2-гидроксипропановой кислоты. Укажите их названия по международной номенклатуре.
3. Объясните почему гликолевая кислота не имеет оптических изомеров.
4. Приведите формулы оптических антиподов молочной и яблочной кислот. Какие из зеркальных изомеров принимают участие в обменных процессах в организме животных и человека? Почему равномолярная смесь зеркальных изомеров оптически неактивна?
5. Приведите уравнения реакций окисления молочной, β-гидроксимасляной и яблочной кислот. Какова биологическая роль продуктов этих реакций?
6. Какое количество гидроксида натрия необходимо для полной нейтрализации 50 г лимонной кислоты? В чем состоит биологическая роль цитрата натрия?
7. Какие типы химических реакций характерны для гидроксикислот? Ответ подтвердите соответствующими уравнениями реакций.
8. В какие специфические реакции вступают гидроксикислоты. Приведите уравнения реакций, происходящих при нагревании с α-гидрокси-, β-гидрокси- и γ-гидроксимасляной кислотой.
9. Расположите следующие кислоты – ацетоуксусную, щавелево-уксусную, α-кетоглутаровую, пировиноградную в порядке возрастания их силы. Ответ аргументируйте и приведите уравнения диссоциации этих кислот.
10. Что общего между ацетоуксусной и β-гидроксимасляной кислотой? Ответ поясните в виде химических реакций и указания биологической роли этих веществ.
11. Какие соединения образуются в результате восстановления оксокислот? Ответ подтвердите примерами химических реакций.
12. Рассчитайте какое количество салициловой кислоты необходимо использовать для
получения 60 г аспирина.
13. Приведите уравнения реакций получения салицилата натрия, метилсалицилата и фе-нилсалицилата. В чем состоит медико-биологическое значение данных соединений?
14. Приведите химические структуры холина, коламина, сфингозина. Что общего междуданными соединениями и в чем заключается их биологическая роль?
15. Напишите структурные формулы ациклических моноаминомонокарбоновых амино-кислот.
16. Приведите структурные формулы ароматических и гетероциклических аминокислот.
17. Напишите структурные формулы моноаминомонокарбоновых и диаминомонокарбоновых аминокислот.
18. В чем состоит различие между заменимыми и незаменимыми аминокислотами? Приведите структурные формулы незаменимых аминокислот.
19. Напишите формулы оптических антиподов серина? Какова биологическая роль L-аминокислот?
20. Какова реакция среды водных растворов лейцина, фенилаланина, глутаминовой кислоты и аргинина? Ответ поясните соответствующими уравнениями реакций диссоциации данных аминокислот.
21. В чем состоят амфотерные свойства аминокислот. Приведите уравнения реакций дис-социации валина в кислой и щелочной средах.
22. Напишите уравнения реакций диссоциации аспарагиновой кислоты в нейтральной, кислой и щелочной средах.
23. Приведите уравнения реакций диссоциации лизина в нейтральной, кислой и щелочной средах.
24. Напишите уравнение реакции получения трипептида N-вал-цис-фен-С.
25. Приведите уравнение реакции получения трипептида N-три-гис-глу-С.
26. Напишите уравнение реакции получения тетрапептида N-гли-иле-тре-мет-С.
27. Напишите уравнение реакции получения тетрапептида N-лей-про-лиз-ала-С.
6.1. Тема. №27. Моноциклические терпены: ментол, валидол, терпингидрат.
Цель
сформировать у студентов знания по лекарственным препаратам терпенов, методам анализа и свойствам данных лекарственных веществ.
Тезисы лекции
Терпенами называют углеводороды, скелет которых построен из звеньев изопрена. Кислородсодержащие производные терпенов (спирты, альдегиды, кетоны) - называют терпеноидами. Терпенами богаты эфирные масла многих растений - мяты, розы, лимона, лаванды и др., смола хвойных деревьев.
Молекулы терпенов могут содержать различное количество связанных между собой остатков изопрена (C5H8):
Н2С=С - СН=СН2.
|
СНЗ
2-Метил-бутадиен-1,3
Общая суммарная формула терпенов: (С5Н8)n. Изопреновые звенья в молекулах терпенов связаны между собой по типу «голова» к «хвосту». Молекулы терпенов могут быть ациклическими, моноциклическими, бициклическими и т.д.
В зависимости от количества изопреновых остатков в молекуле выделяют следующие группы: терпены - C10H16, - сесквитерпены C15H24 (полутора кратные), дитерпены - С20Н32, тритерпены СзоН48, политерпены - (C5H8)n. Терпены получили широкое применение в различных отраслях промышленности (парфюмерной, химической) и в медицине.
Лекарственные препараты из группы терпенов классифицируют по количеству циклов на моноциклические (ментол, валидол и терпингидрат); бициклические - (камфора, бромкамфора, сульфокамфорная кислота и ее новокаиновая соль - (сульфокамфокаин); 3-я группа препаратов представлена моноциклическим дитерпеном ретинола ацетатом (витамин А).
Как правило, все терпены - это легко летучие соединения с характерным запахом (воздействуют на дыхательный центр). Таким свойством обладают ментол, валидол, камфора, в меньшей степени - ретинол. Терпингидрат запаха не имеет. Ментол летуч, tпл. 41-44оС. У камфоры tпл. 174-180оС, но она легко возгоняется при комнатной температуре. Поэтому ментол и камфору хранят в отдельном шкафу, в плотно закрытых банках. Ретинола ацетат имеет tпл. 51-57оС, очень легко окисляется на воздухе, поэтому его хранят в запаянных в токе азота ампулах, в холодильнике.
ЛС этой группы не растворимы в воде, но растворимы в органических растворителях и жирных маслах. Это обусловливает выбор соответствующих лекарственных форм: ментол применяют в виде спиртовых и масляных растворов, мазей и аэрозолей; камфору и ретинола ацетат - и виде масляных растворов; водорастворимое производное камфоры сульфокамфокаин - в виде 10% водного раствора для инъекций, что исключает осложнения в виде олеом, возможные при инъекциях масляных растворов камфары.
Все терпены имеют в своей структуре центры хиральности, являются оптически активными соединениями. Это свойство используется как характеристика подлинности и доброкачественности препаратов (удельное вращение). Характерным свойством терпенов является их легкая изомеризация под действием света, температуры, рН среды, катализаторов, что обусловливает их многообразные взаимопревращения. Это свойство используется при получении ЛС данной группы, но может отмечаться и в процессе хранения.
Некоторые терпены поглощают свет в УФ-области спектра: камфора и ее производные - благодаря наличию кето-группы в cтpyктуре молекулы, ретинол - благодаря наличию сопряженных двойных связей.
Подлинность: Общая реакция для моно- и бициклических терпенов. Это реакция конденсации с ароматическими альдегидами (например, с ванилином) в присутствии концентрированной H2SО4. Она характерна для ментола, валидола и камфары, имеющих свободное (Х-положение в цикле по отношению к спиртовому гидроксилу или кето-группе:
Продукт реакции окрашен в малиновый цвет за счет наличия в структуре системы сопряженных двойных связей.
При конденсации камфоры с ванилином в присутствии концентрированной H2SO4 образуется продукт реакции аналогичного строения.
При конденсации камфоры с другими альдегидами, например с пара-диметиламинобензальдегидом, образуется продукт конденсации, окрашенный в красный цвет, с фурфуролом – в фиолетовый:
п –Диметиламинобензальдегид
Не нашли, что искали? Воспользуйтесь поиском: