
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Условия равновесия и характеристические функции
Критерием равновесия изолированной системы (т.е. системы, которая не обменивается с внешней средой ни теплом, ни работой) является соотношение
dS = 0.
Однако, если система не изолирована от внешнего мира и может каким-либо образом с ним взаимодействовать, то условия равновесия будут иными.
Запишем объединенное уравнение первого и второго законов термодинамики в виде
TdS ³ dU + PdV. (2.15)
Для сложной системы
TdS ³ dU + PdV + d W '. (2.16)
Когда в простой системе осуществляются обратимые процессы
TdS = dU + PdV. (2.17)
Если в сложной системе реализуются обратимые процессы, то
TdS = dU + PdV + d W '. (2.18)
Для систем, единственным видом работы которых является работа расширения (простые системы), наиболее интересны четыре вида условий взаимодействия системы с окружающей средой:
1) V = const, S = const;
2) V = const, T = const;
3) P = const, S = const;
4) P = const, T = const.
Критерии равновесия для каждого из этих четырех случаев взаимодействия системы с окружающей средой определяются следующим образом.
1. Условия взаимодействия: V = const, S = const. Объединенное уравнение первого и второго законов термодинамики для простых систем (2.15) запишем в виде
dU £ TdS – PdV. (2.19)
Из этого соотношения видно, что если в системе изменения объема и энтропии равны нулю (dV = 0, dS = 0), то выполняется условие
dU £ 0. (2.20)
В состоянии равновесия
dU = 0. (2.21)
Таким образом, с приближением к состоянию равновесия внутренняя энергия простой системы убывает и достигает минимума в состоянии равновесия. Другими словами, внутренняя энергия, так же как и энтропия, определяет направление процесса.
2. Условия взаимодействия: P = const, S = const. Преобразуя величину PdV к виду
PdV = d (PV) – VdP (2.22)
и учитывая определение энтальпии для простых систем (H = U + PV), уравнение (2.15) запишем в виде
dH £ TdS + VdP. (2.23)
Отсюда видно, что любой процесс в рассматриваемой системе, у которой dP = 0, dS = 0, протекает таким образом, что выполняется условие
dH £ 0. (2.24)
В состоянии равновесия
dH = 0. (2.25)
Таким образом, с приближением к состоянию равновесия энтальпия такой системы убывает, достигая минимума в состоянии равновесия.
3. Условия взаимодействия: V = const, T = const. Записав величину TdS в виде
TdS = d (TS) – SdT, (2.26)
преобразуем уравнение (2.15)
d (U – TS) £ – SdT – pdV. (2.27)
Введя обозначение
F = U – TS, (2.28)
запишем (2.27) в виде
dF £ – SdT – pdV. (2.29)
Термодинамическая функция F называется энергией Гельмгольца, или изохорно-изотермическим потенциалом. Поскольку эта функция образована из функций состояния U и S, она также является функцией состояния.
Из (2.29) следует, что в системе, для которой dT = 0 и dV = 0, должно выполняться условие
dF £ 0. (2.30)
Следовательно, в состоянии равновесия
dF = 0. (2.31)
Таким образом, с приближением системы к состоянию равновесия изохорно-изотермический потенциал убывает, достигая минимума в состоянии равновесия.
4. Условия взаимодействия: P = const, T = const. С учетом уравнений (2.22) и (2.26) формулу (2.15) можно записать в следующем виде:
d (U + PV – TS) £ – SdT + VdP. (2.32)
Обозначая
G = U + PV – TS = H – TS, (2.33)
выразим (2.32) в виде
dG £ – SdT + VdP. (2.34)
Термодинамическая функция G называется энергией Гиббса или изобарно-изотермическим потенциалом. Эта функция, также как и энергия Гельмгольца, образована из функций состояния H и S, поэтому является функцией состояния.
Из (2.34) видно, что в системе с постоянными температурой и давлением любой процесс протекает таким образом, что выполняется условие
dG £ 0. (2.35)
Следовательно, в состоянии равновесия
dG = 0. (2.36)
Таким образом, с приближением к состоянию равновесия изобарно-изотермический потенциал системы, у которой постоянны температура и давление, убывает, достигая минимума в состоянии равновесия.
В тех случаях, когда система помимо работы расширения производит и другие виды работ (сложная система), критерии равновесия будут несколько иными. Для такой системы из объединенного первого и второго законов термодинамики, записанного в виде (2.16) TdS ³ dU + PdV + + d W ', для рассмотренных выше четырех случаев взаимодействия системы с окружающей средой получим следующие результаты:
1. Для условий взаимодействия V = const, S = const
dU + d W ' £ 0 (2.37)
и в состоянии равновесия работа равна убыли внутренней энергии
dU = – d W '. (2.38)
2. Для условий взаимодействия p = const, S = const
dH + d W ' £ 0 (2.39)
и в состоянии равновесия работа равна убыли энтальпии
dH = – d W '. (2.40)
3. Для условий взаимодействия V = const, T = const
dF + d W ' £ 0 (2.41)
и в состоянии равновесия работа равна убыли изохорно-изотермического потенциала
dF = – d W '. (2.42)
4. Для условий взаимодействия p = const, T = const
dG + d W ' £ 0 (2.43)
и в состоянии равновесия работа равна убыли изобарно-изотермического потенциала
dG = – d W '. (2.44)
Функции U, H, F, G называются характеристическими.
Из уравнений (2.38), (2.40), (2.42) и (2.44) следует, что работа, которая может быть совершена сложной системой при данных условиях взаимодействия с окружающей средой (за вычетом работы расширения), равна убыли соответствующих характеристических функций. Поскольку в состоянии равновесия работа, совершенная системой, максимальна при определенных внешних условиях [см. уравнения (2.38), (2.40), (2.42) и (2.44)], по этой причине характеристические функции U, H, F, G называют термодинамическими потенциалами.
Таким образом, характеристические функции в термодинамике играют роль, аналогичную роли потенциальной энергии в механике. В действительности все они представляют частные виды свободной энергии, т.е. энергии, способной совершать полезную работу. Однако по традиции это название оставлено за изохорно-изотермическим потенциалом F. Точно так же иногда энергию Гиббса (изобарно-изотермический потенциал) называют свободной энтальпией.
Характеристические функции обладают следующим важным свойством: если известна характеристическая функция, выраженная через свои переменные, то из нее можно вычислить любую термодинамическую величину. Из объединенного первого и второго законов термодинамики, записанного в виде
dU = TdS – PdV, (2.45)
следует (на основе свойств полного дифференциала), что

 (2.46)
(2.46)
Таким образом, если функция U выражена через свои переменные V и S, то частные производные по одной из переменных при неизменности другой позволяют определить значения P и T для простой системы. Другими словами, изменение внутренней энергии вследствие изменения энтропии при постоянстве объема физически вызвано сообщением теплоты в обратимом и изохорическом процессе. Изменение внутренней энергии системы вследствие изменения объема при постоянстве энтропии в обратимом адиабатическом процессе физически вызвано совершением работы. Таким образом, определены все термические и механические свойства системы. Именно поэтому данная функция является характеристической.
Точно так же могут быть определены свойства системы с помощью других характеристических функций. Из уравнения
dH = TdS + VdP. (2.47)
следует, что
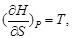
 (2.48)
(2.48)
Записав выражение для энергии Гельмгольца в виде полного дифференциала (для простой системы) в виде
dF = – SdT – PdV, (2.49)
получаем

 (2.50)
(2.50)
Наконец, используя выражение энергии Гиббса, записанной в виде полного дифференциала
dG = – SdT + VdP, (2.51)
имеем

 (2.52)
(2.52)
Следовательно, если та или иная характеристическая функция выражена через свои переменные, то дифференцирование ее по одной из переменных при условии неизменности другой позволяет определить все остальные параметры и другие термодинамические потенциалы.
Можно заметить, что одна из переменных в каждой из четырех пар независимых переменных принадлежит группе тепловых величин (T и S), а другая – группе механических величин (P и V).
Наибольшее значение в конкретных термодинамических расчетах имеют энергия Гиббса G и энергия Гельмгольца F, так как их естественные переменные наиболее удобны для химии.
Расчет изменения функций F и G в химических реакциях можно проводить разными способами. Рассмотрим два из них на примере энергии Гиббса.
1. По определению, G = H – TS. Если продукты реакции и исходные вещества находятся при одинаковой температуре, то стандартное изменение энергии Гиббса в химической реакции определяется по формулам:
 (2.53)
(2.53)
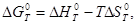 (2.54)
(2.54)
где тепловой эффект можно рассчитать с помощью стандартных энтальпий образования, а стандартное изменение энтропии – по абсолютным энтропиям участников реакции.
2. Аналогично тепловому эффекту реакции, изменение энергии Гиббса можно рассчитать, используя энергии Гиббса образования веществ:
 (2.55)
(2.55)
В термодинамических таблицах обычно приводят абсолютные энтропии и значения термодинамических функций образования соединений из простых веществ при температуре 298 К и давлении 1 атм (стандартное состояние).
Не нашли, что искали? Воспользуйтесь поиском: