
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Какие количества 10%-го и 80%-го растворов азотной кислоты нужно смешать, чтобы получить 1л 60%-го раствора?
Решение: по правилу креста
80 
 50
50
10 
 20
20
т.е. исходные растворы кислот нужно смешивать в соотношении 20:50.
По справочнику находим, что плотность 60%-го раствора HNO3 составляет 1,365, поэтому 1л нужного нам раствора весит 1365г. Это количество раствора нужно разделить на две части в соотношении 20:50. Составляем пропорции:
Из 20г 10%-го раствора получим 20+50г р-ра
Из Х г------------------------------------1365г р-ра
 .
.
т.е. нужно взять 390г 10%-го раствора.
Аналогично: из 50г 80%-го раствора----------------70г
Х--------------------------------------1365г
 .
.
Для удобства пересчитывают эти количества в объеме на единицы. Для 10%-го раствора HNO3 плотность равна 1,455, поэтому объем раствора, необходимый для смешивания будет равен:
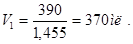
Для 60% -го раствора плотность равна 1,455, поэтому объем раствора равен:
 .
.
Пример 5. При решении задач на разбавление растворов чистым растворителем нужно второй раствор в правиле «креста» считать за раствор с концентрацией 0.
Сколько воды следует добавить к 100г 40%-ой щелочи натрия, чтобы получить 5%-ый раствор?
Решение: по правилу «креста»
40 
 5
5

 0 35
0 35
т.е.  ,
,
далее определяем количество воды, которое нужно смешать со 100г щелочи:
5 - 35
100 - X

Пример 6. При решении задач на смешивание растворов, концентрации которых выражены в молях или нормальностях, моляльностях, также можно применять правило «креста».
Сколько нужно взять 0,2М и 1М растворов, чтобы приготовить 1000мл 0,4м раствора?
Решение: по правилу «креста»:
1 
 0,2
0,2

 0,4
0,4
0,2 0,6
 , тогда
, тогда
 ,
,
 .
.
Пример 7. Сколько воды нужно добавить к 1000мл. 1,15н раствора NaOH, чтобы получить 1,0Н раствор?
Решение: по правилу «креста»
 1,15 1 1 - 0,15
1,15 1 1 - 0,15

 1 1000 - X
1 1000 - X
 0 0,15
0 0,15
 .
.
Пример 8. Сколько воды и серной кислоты, удельного веса 1,82 г/см3 следует взять для приготовления 5л 2Н раствора?
Решение: Пересчитаем концентрацию серной кислоты на нормальность. По справочнику находим, что если плотность H2SO4 равна 1,82, то она содержит 91,11г. H2SO4 в 100г раствора.
В 100г раствора - 91,11г
В 1820г (1литр) - Х

Эквивалент H2SO4 = 49, поэтому нормальность будет равна:

Далее применяем правила «креста»:

 33,8 2.
33,8 2.

 2
2
0 31,8
т.е. отношение объемов

Из 1 литра H2SO4 плотностью 1,82 получается (15,9+1)л. раствора. Из Х – 5л. р-ра.
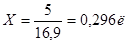
Из 15,9л. H2O получится 16,9л. 2Н р-ра
Из Хл. H2O -----------5л. 2Н р-ра.
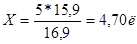
Не нашли, что искали? Воспользуйтесь поиском: