
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Amp;5. Молекула-кинетикалық теорияның және термодинамиканың физикалық негіздері. 4 страница
 5.206. Қуаты 14,7 квт бу машинасы, 1 caғ ішіндегі істеген жұмысында жылу шығарғыштық қабілеті 3,3 ∙107 дж/кг-ға тең 8,1 кг көмір пайдаланады. Қазанның температурасы 200°С, ал тоңазытқыштың температурасы 58°С. Машинаның фактыға негізделген
5.206. Қуаты 14,7 квт бу машинасы, 1 caғ ішіндегі істеген жұмысында жылу шығарғыштық қабілеті 3,3 ∙107 дж/кг-ға тең 8,1 кг көмір пайдаланады. Қазанның температурасы 200°С, ал тоңазытқыштың температурасы 58°С. Машинаның фактыға негізделген  1 п. ә. коэффициентін тауып және оны сол температуралардың аралығында Карноның циклі бойынша жұмыс істейтін идеал жылу машинасының п. ә. коэффициентімен салыстыру керек.
1 п. ә. коэффициентін тауып және оны сол температуралардың аралығында Карноның циклі бойынша жұмыс істейтін идеал жылу машинасының п. ә. коэффициентімен салыстыру керек.
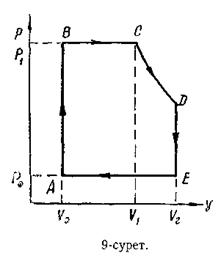
5.207. Қуаты 20 ат күшіне тең бу машинасы поршенінің ауданы 200 см2, ал поршеньнің жүрісі l = 45 см. ВС изобаралық процесі (9-сурет), поршень қозғалғандағы, оның жүрісінің үштен бір бөлігінде өтеді. Vo көлемді, V1 және V2 көлемдермен салыстырғанда ескермесе де болады.
Қазандағы будың қысымы 16 ат, тоңазытқыштағы будың қысымы 1 ат. Адиабата көрсеткішін 1,3-ке тең деп алып, машинаның 1 мин ішінде қанша цикл жасайтынын табу керек.
 5.208. Карбюраторлы және газды төрт тактілі іштен жанатын двигательдің циклі 10-суретте керсетілген: а) поршеньнің бірінші жүрісінде цилиндрдің ішіне жанар май сорылады (карбюраторларлы двигательдерде жанар май қоспасы, карбюраторлардың ішінде дайындалатын, бензин буының ауамен араласқан қоспасы; газды двигательдердегі жұмысшы қоспа газ — ауа газ-генераторлық құрылыстан келеді), бұл жағдайда ро = const болады және көлем v2 -ден v1 -ге дейін өседі (АВ тармағы — сорылу); б) поршеньнің екінші жүрісінде (ВС тармағы — сығылу) жанар май v1 – ден
5.208. Карбюраторлы және газды төрт тактілі іштен жанатын двигательдің циклі 10-суретте керсетілген: а) поршеньнің бірінші жүрісінде цилиндрдің ішіне жанар май сорылады (карбюраторларлы двигательдерде жанар май қоспасы, карбюраторлардың ішінде дайындалатын, бензин буының ауамен араласқан қоспасы; газды двигательдердегі жұмысшы қоспа газ — ауа газ-генераторлық құрылыстан келеді), бұл жағдайда ро = const болады және көлем v2 -ден v1 -ге дейін өседі (АВ тармағы — сорылу); б) поршеньнің екінші жүрісінде (ВС тармағы — сығылу) жанар май v1 – ден 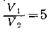 V2-гe дейін адиабаталық сығылады, осы уақытта температура То-ден Т1-ге дейін жоғарылайды, ал қысым Ро-ден р1 -ге дейін артады; в) одан әрі жанар майдың ұшқынынан от алуы болады, осы уақытта тұрақты көлемде қысым р1- ден р2-ге дейін артады (CD тармағы), температура Т2 мәніне дейін өседі; г) поршеньнің үшінші жүрісінде жанар майдың v2 -ден v1 -ге дейінгі адиабаталық ұлғаюы болады да (жұмыс жүрісі — DE тармақ), температура Т3-ке дейін төмендейді; д) поршеньнің ең шеткі қалпында (Е нүктеде) сыртқа шығаратын клапан ашылады да, тұрақты көлемде қысым ро-ге дейін төмендейді (ЕВ тармақ); е) поршеньнің төртінші жүрісі — изобаралық сығылу (ВА тармақ — итеріп шығарушы — жұмыс істеген газды итеріп шығару).
V2-гe дейін адиабаталық сығылады, осы уақытта температура То-ден Т1-ге дейін жоғарылайды, ал қысым Ро-ден р1 -ге дейін артады; в) одан әрі жанар майдың ұшқынынан от алуы болады, осы уақытта тұрақты көлемде қысым р1- ден р2-ге дейін артады (CD тармағы), температура Т2 мәніне дейін өседі; г) поршеньнің үшінші жүрісінде жанар майдың v2 -ден v1 -ге дейінгі адиабаталық ұлғаюы болады да (жұмыс жүрісі — DE тармақ), температура Т3-ке дейін төмендейді; д) поршеньнің ең шеткі қалпында (Е нүктеде) сыртқа шығаратын клапан ашылады да, тұрақты көлемде қысым ро-ге дейін төмендейді (ЕВ тармақ); е) поршеньнің төртінші жүрісі — изобаралық сығылу (ВА тармақ — итеріп шығарушы — жұмыс істеген газды итеріп шығару).
Сығылу коэффициентін және адиабатаның көрсеткішін 1,33-ке тең деп алып, циклдің п. ә. коэффициентін табу керек.
5.209. Карбюраторлы іштен жанатын двигатель цилиндріндегі газ 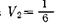 V1 дейін политропиялы сығылады (сығылу коэффициенті 6-ға тен,). Бастапқы қысым 9 ∙ 104 н/м2-ге, ал бастапқы температура 127°С-ге тең деп алып, сығылудан кейінгі, цилиндрдегі газдың қысымы мен температурасын табу керек. Политропия көрсеткіші 1,3-ке тең.
V1 дейін политропиялы сығылады (сығылу коэффициенті 6-ға тен,). Бастапқы қысым 9 ∙ 104 н/м2-ге, ал бастапқы температура 127°С-ге тең деп алып, сығылудан кейінгі, цилиндрдегі газдың қысымы мен температурасын табу керек. Политропия көрсеткіші 1,3-ке тең.
5.210. Карбюраторлы іштен жанатын двигатель цилиндрінде газ политропиялы сығылады. Сығылғаннан кейінгі температурасы 427°С-ге тең болады. Газдың бастапқы температурасы 140°С. Сығылу коэффициенті 5,8. Политропа көрсеткіші неге тең болады?
5.211. Карбюраторлы іштен жанатын двигатель цилиндрінің диаметрі 10 см, поршеньнің жүрісі 11 см. 1) Газдың бастапқы қысымы 1 ат, газдық бастапқы температурасы 127°С және сығылудан кейінгі камерадағы ақырғы қысым 10 ат десек, онда сығылу жүргізілетін камераның көлемі қандай болады? 2) Сығылудан кейінгі камерадағы температура қандай? 3) Сығылу уақытындағы істелінген жұмысты табу керек. Политропия көрсеткіші 1,3-ке тең.
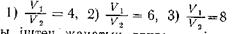 5.212. Политропа көрсеткішін 1,3-ке тең деп және сығылу дәрежелеріне тең деп, карбюраторлы іштен жанатын двигательдің п. ә. коэффициентін табу керек.
5.212. Политропа көрсеткішін 1,3-ке тең деп және сығылу дәрежелеріне тең деп, карбюраторлы іштен жанатын двигательдің п. ә. коэффициентін табу керек.
5.213. «Победа» автомобилінің карбюратор двигателі 1 а. /с./сағ-қа ең аз дегенде 265 г бензин жұмсайды. Үйкеліске, жылу өткізгіштікке және тағы басқа да кететiн шығындарды табу керек. Сығылу коэффициенті 6,2; бензиннің жылу шығарғыштық қабілеті 4,6 ∙ 107 дж/кг. Политропа көрсеткішін 1,2-ге тең деп аламыз.
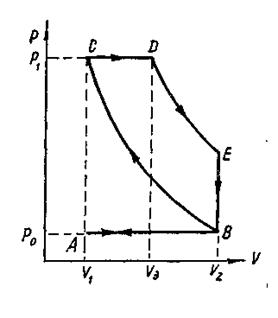 5.214. Дизельдің төрт тактілі двигателінің циклі 11-суретте көрсетілген: а) АВ тармағы — цилиндрдің ішіне ауа сорылып кіргізіледі (ро=1 ат); б) ВС тармағы — р1 қысымға дейін ауа адиабаталы сығылады; в) сығылу тактісінің аяғында цилиндрдің ішіне сұйық отын бүркіледі, ол ыстық ауада тұтанып жанады да, осы уақытта поршень алдымен изобаралы, (CD тармағы), содан кейін адиабаталы болып (DE тармағы) оңға қарай қозғалады; г) адиабаталық ұлғаюдың соңында ауа шығарғыш клапан ашылады да қысым ро-ге дейін кемиді (ЕВ тармағы); д) поршень сол жаққа қарай қозғалғанда қоспа цилиндрдің ішінен сыртқа шығарылады (ВА тармағы). Дизельдік двигателінің п. ә. коэффициентін табу керек.
5.214. Дизельдің төрт тактілі двигателінің циклі 11-суретте көрсетілген: а) АВ тармағы — цилиндрдің ішіне ауа сорылып кіргізіледі (ро=1 ат); б) ВС тармағы — р1 қысымға дейін ауа адиабаталы сығылады; в) сығылу тактісінің аяғында цилиндрдің ішіне сұйық отын бүркіледі, ол ыстық ауада тұтанып жанады да, осы уақытта поршень алдымен изобаралы, (CD тармағы), содан кейін адиабаталы болып (DE тармағы) оңға қарай қозғалады; г) адиабаталық ұлғаюдың соңында ауа шығарғыш клапан ашылады да қысым ро-ге дейін кемиді (ЕВ тармағы); д) поршень сол жаққа қарай қозғалғанда қоспа цилиндрдің ішінен сыртқа шығарылады (ВА тармағы). Дизельдік двигателінің п. ә. коэффициентін табу керек.
5.215. Дизельдің іштен жанатын двигателінің 16-ға тең болатын адиабаталық сығылу дәрежесі бар, ал адиабаталық ұлғаю дәрежесі 6,4-ке тең. Егер двигательдің қуаты 50 ат күші, политропа көрсеткіші 1,3 және бензиннің жылу шығарғыштық қабілеті 4,6 ∙ 107 дж/кг болса, онда двигательдің бір сағатта тұтынатын мұнайының ең аз дегендегі мөлшері қандай болады?
5.216. —20°С температурада тұрған 10 г мұзды 100°С температурада буға айналдырғандағы энтропияның өзгерісін табу керек.
5.217. 0°С-дегі 1 г суды 100°С-дегі буға айналдырғандағы энтропияның өсуін табу керек.
5.218. 0°С тұрған 1 кг мұзды еріткендегі энтропияның өзгерісін табу керек.
5.219. Балқу температурасында тұрған 640 г балқыған қорғасынды 0°С тұрған мұздың үстіне құяды. Осы процестегі энтропияньщ өзгерісін табу керек.
5.220. 8 г оттегінің 80°С температурадағы 10 л көлемнен, 300°С температурадағы 40 л көлемге ауысқандағы энтропияның өзгерісін табу керек.
5.221. 6 г сутегінің 1,5 • 105 н/м2 қысымдағы 20 л көлемнен 1 • 105 н/м2 қысымдағы 60 л көлемге ауысқандағы энтропияның өзгерісін табу керек.
5.222. 6,6 г сутегінің көлемі екі еселенгенге дейін изобаралы ұлғаяды. Осы уақыттағы энтропияның өзгерісін табу керек.
5.223. 8 г гелийдің V1 = 10 л көлемнен V2 = 25 л көлемге дейін изобаралы ұлғайғандағы энтропияның өзгерісін табу керек.
5.224. 6 г оттегінің қысымы 105 н/м2-ден 0,5 • 105 н/м2-ге дейін изотермалы ұлғайғандағы энтропияның өзгерісін табу керек.
5.225. 10,5 г азот v1 = 2 л көлемнен v 2 = 5 л көлемге дейін изотермалы ұлғаяды. Осы процестегі энтропияның өсуін табу керек.
5.226. 10 г оттегі t1 = 50°С-ден t 2=150°С-ге дейін қыздырылады. Қыздыруды: 1) изохоралы және 2) изобаралы өтеді деп алып, энтропияның өзгерісін табу керек.
5.227. Екі атомды газдың 1 киломолін қыздырғанда, оның абсолют температурасы 1,5 есе артады. Қыздыруды: 1) изохоралы және 2) изобаралы өтеді деп алып, энтропияның өзгерісін табу керек.
5.228. 22 г азотты қыздырудың нәтижесінде оның абсолют температурасы 1,2 есе өсіп, ал энтропиясы 4,19 дж/град-қа. артты. Қыздыру қандай жағдайда өткізілді (тұрақты көлемде ме немесе тұрақты қысымда ма)?
5.229. 5 • 194-есептің шартын пайдаланып газдың А күйден В күйге ауысқандағы энтропияның өзгерісін табу керек. Ауысуды АСВ және ADB жолдарымен өтті деп есептейміз (8-суретті қараңыздар).
5.230. 0°С температурада және 2 кГ/см2 қысымда тұрған бір куб. метр ауа, v1 көлемнен v 2 = 2 v1 көлемге дейін изотермалы ұлғаяды. Осы процестегі энтропияның өзгерісін табу керек.
5.231. Карноның цикліндегі екі адиабатаның арасындағы учаскедегі энтропияның өзгерісі 1 ккал/град-қа тең. Екі изотерманың арасындағы температураның айырымы 100°-қа тең. Осы циклде жылу мөлшерінің қаншасы жұмысқа айналады?
§6 Нақты газдар
Бір киломоль үшін берілген нақты газ күйінің теңдеуі (Ван – дер-Ваальс теңдеуі) төмендегідей:
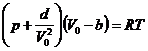
Мұндағы 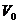 - бір киломоль газдың көлемі, а және
- бір киломоль газдың көлемі, а және 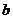 - тұрақты, әр түрлі газдар үшін әрқилы болады,
- тұрақты, әр түрлі газдар үшін әрқилы болады,  - қысым, Т – абсолют температура және
- қысым, Т – абсолют температура және  -газ тұрақтысы.
-газ тұрақтысы.
Ван – дер – Ваальстың газдың кез келген М массасына қатысты теңдеуінің түрі төмендегіше:
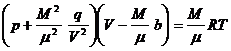
Мұндағы 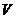 - барлық газдың көлемі,
- барлық газдың көлемі,  -бір киломольдің массасы.
-бір киломольдің массасы.
Бұл теңдеудегі 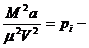 молекулалардың өз ара күшімен қамтамасыз етілген қысым, және
молекулалардың өз ара күшімен қамтамасыз етілген қысым, және 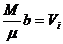 - молекулалардың меншікті көлемімен байланысты болатын көлем.
- молекулалардың меншікті көлемімен байланысты болатын көлем.
Берілген газдың а және 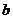 тұрақтылары, оның
тұрақтылары, оның 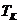 кризистік температурасымен,
кризистік температурасымен, 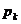 кризистік қысымымен және
кризистік қысымымен және 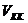 кризистік көлемімен мынадай қатынастар арқылы байланысады:
кризистік көлемімен мынадай қатынастар арқылы байланысады:
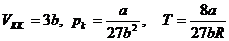
Бұл теңдеуді а және 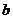 тұрақтылары қатысты шешуге болады:
тұрақтылары қатысты шешуге болады:
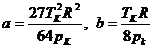
Егер келтірілген шамаларды енгізсек,
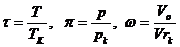
Онда Ван – дер-Ваальстың теңдеулерінің түрі мынадай болады (бір киломель үшін):
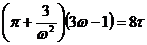
6.1 Ван – дер-Ваальстың теңдеуіне енетін а және 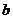 тұрақтыларының СИ бірліктеріндегі атауларын табу керек.
тұрақтыларының СИ бірліктеріндегі атауларын табу керек.
6.2 Кейбір газдар үшін 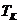 және
және 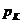 кризистік шамалар жайындағы мәліметтерді пайдаланып, олар үшін Ван-дер-Ваальстың теңдеуіне енетін а және
кризистік шамалар жайындағы мәліметтерді пайдаланып, олар үшін Ван-дер-Ваальстың теңдеуіне енетін а және 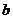 тұрақтыларды табу керек.
тұрақтыларды табу керек.
6.3 2 атм қысымдағы 820 см3 көлемді алып тұрған 2 г азоттың температурасы қандай болады? Газды; 1) идеал деп және 2) наөты деп қарастыру керек.
6.4 28 атм қысымдағы, 90 см3 көлемді алып тұрған 3,5 г оттегінің температурасы қандай? Газдарды: 1) идеал және 2) нақты газ деп қарастырыңыздар.
6.5 108 н/м2 қысымда 10 г гелийдің алып тұрғ,ан көлемі 100 см3. Газдарды: 1) идеал газ деп және 2) нақты газ деп қарастырып, олардың температурасын табу керек.
6.6 1 кмоль көмір қышқыл газ 1000С температурада тұр. Газдарды: 1) нақты газ және 2) идеал газ деп алып, олардың қысымын табу керек. Есепті: а) 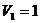 м3 және б)
м3 және б) 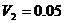 м3 көлемдер үшін шығару керек.
м3 көлемдер үшін шығару керек.
6.7 Көлемі 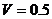 м3 жабық ыдыста
м3 жабық ыдыста 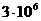 н/м2 қысымдағы 0,6 кмоль көмір қышқыл газы бар. Ван-дер-Ваальстың теңдеуін пайдаланып, газдың қысымын екі есе өсіру үшін, оның температурасын неше есе өсіру керек екендігін табу керек.
н/м2 қысымдағы 0,6 кмоль көмір қышқыл газы бар. Ван-дер-Ваальстың теңдеуін пайдаланып, газдың қысымын екі есе өсіру үшін, оның температурасын неше есе өсіру керек екендігін табу керек.
6.8 1 кмоль оттегі 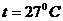 температурада және
температурада және 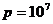 н/м2 қысымда тұр. Берілген жағдайда оттегі өзін нақты газ сияқты ұстайды деп есептеп газдың көлемін табу керек.
н/м2 қысымда тұр. Берілген жағдайда оттегі өзін нақты газ сияқты ұстайды деп есептеп газдың көлемін табу керек.
6.9 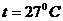 температурада және
температурада және 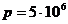 н/м2 қысымда 1 кмоль азот тұр. Берілген жағдайда азот өзін нақты газ сияқты ұстайды деп есептеп газдың көлемін табу керек.
н/м2 қысымда 1 кмоль азот тұр. Берілген жағдайда азот өзін нақты газ сияқты ұстайды деп есептеп газдың көлемін табу керек.
6.10 Оттегі үшін 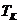 және
және 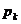 кризистік шамалары белгілі деп алып, оның молекулаларының эффективті диаметрін табу керек.
кризистік шамалары белгілі деп алып, оның молекулаларының эффективті диаметрін табу керек.
6.11 Азот молекулаларының эффективті диаметрін екі түрлі тәсілмен: 1) қалыпты жағдайдағы молекуланың еркін жолының орташа ұзындығының 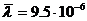 см берілген мәні бойынша, 2) Ван-дер-Ваальстың теңдеуіндегі
см берілген мәні бойынша, 2) Ван-дер-Ваальстың теңдеуіндегі 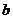 тұрақтысының белгілі шамасы бойынша табу керек.
тұрақтысының белгілі шамасы бойынша табу керек.
6.12 Қалыпты жағдайдағы көмір қышқыл газының еркін жолының орташа ұзындығын табу керек. Көмір қышқыл газ үшін кризистік температураны 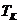 және қысымды
және қысымды 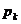 белгілі деп есептеп, молекуланың эффективті диаметрін есептеп шығару керек.
белгілі деп есептеп, молекуланың эффективті диаметрін есептеп шығару керек.
6.13 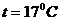 температурадағы және
температурадағы және 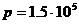 н/м2 қысымдағы гелийдің диффузия коэффициентін табу керек. Гелий үшін
н/м2 қысымдағы гелийдің диффузия коэффициентін табу керек. Гелий үшін 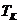 және
және 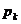 белгілі деп есептеп, гелий атомының эффективті диаметрін есептеп шығару керек.
белгілі деп есептеп, гелий атомының эффективті диаметрін есептеп шығару керек.
6.14 00С температурадағы бір киломоль көмір қышқыл газ үшін 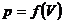 изотермасын құраңыздар. Газды: 1) идеал газ және 2) нақты газ деп қарастырыңыздар. Нақты газ үшін м3/кмоль-мен берілген.
изотермасын құраңыздар. Газды: 1) идеал газ және 2) нақты газ деп қарастырыңыздар. Нақты газ үшін м3/кмоль-мен берілген. 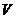 -ның мәндерін төмендегіге тең деп алыңыздар: 0,07; 0,08; 0,10; 0,12; 0,14; 0,16; 0,18; 0,20; 0,25; 0,30; 0,35 және 0,40, ал идеал газ үшін
-ның мәндерін төмендегіге тең деп алыңыздар: 0,07; 0,08; 0,10; 0,12; 0,14; 0,16; 0,18; 0,20; 0,25; 0,30; 0,35 және 0,40, ал идеал газ үшін 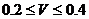 м3/кмоль интервалында.
м3/кмоль интервалында.
6.15 Қалыпты жағдайдағы молекулалардың өз ара әсер күштеріне сәйкес келген бір киломоль газдың ішіндегі қысымды табу керек. Осы газдың кризистік температурасы және кризистік қысымы сәйкес 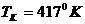 -ге және
-ге және  атм-,а тең болады.
атм-,а тең болады.
6.16 Сутегі үшін молекулалардың өз ара әсер күші өте азғантай болып келеді; бұл жағдайда көбінесе маңызды роль атқаратын молекуланың меншікті өлшемдері. 1) Осындай жартылай идеал газ күйінің теңдеуін жазу керек. 2) Молекулалардың меншікті өлшемін ескерусіз қалдырып, 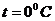 температурадағы және
температурадағы және 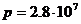 н/м2 қысымдағы кейбір көлемде тұрған сутегі молекуласы киломолінің санын тапқанда қандай қате жібергенімізді табу керек.
н/м2 қысымдағы кейбір көлемде тұрған сутегі молекуласы киломолінің санын тапқанда қандай қате жібергенімізді табу керек.
6.17 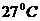 температурадағы 0,25 кг азот тұрған ыдыстың көлемі 10 л. 1) газ қысымының қандай бөлігі молекулалардың өз ара әсер күштеріне сәйкес қысымды құрады? 2) ыдыстың көлемінің қандай бөлігі молекуланың меншікті көлемін құрады?
температурадағы 0,25 кг азот тұрған ыдыстың көлемі 10 л. 1) газ қысымының қандай бөлігі молекулалардың өз ара әсер күштеріне сәйкес қысымды құрады? 2) ыдыстың көлемінің қандай бөлігі молекуланың меншікті көлемін құрады?
6.18 Кейбір газдың 0,5 кмолі 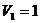 м3 көлемді алып тұрады. Газды
м3 көлемді алып тұрады. Газды 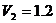 м3 көлемге дейін ұлғайтқан уақыттарда молекулалардың өз ара әсер күшіне қарсы
м3 көлемге дейін ұлғайтқан уақыттарда молекулалардың өз ара әсер күшіне қарсы 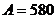 кГм-ге тең жұмыс істелді. Осы газ үшін Ван-дер Ваальстың теңдеуіндегі а тұрақтысын табу керек.
кГм-ге тең жұмыс істелді. Осы газ үшін Ван-дер Ваальстың теңдеуіндегі а тұрақтысын табу керек.
6.19 20 кг азот бостықта 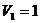 м3-ден
м3-ден 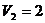 м3-ге дейін адиабаталы ұлғаяды. Ван – дер – Ваальстың теңдеуіне енетін а тұрақтысын азот үшін белгілі деп алып, осы ұлғаюдағы температураның төмендеуін табу керек.
м3-ге дейін адиабаталы ұлғаяды. Ван – дер – Ваальстың теңдеуіне енетін а тұрақтысын азот үшін белгілі деп алып, осы ұлғаюдағы температураның төмендеуін табу керек.
6.20 Үш атомды газдың 0,5 кмолі бостыққа қарай 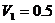 м3-ден
м3-ден 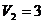 м3-ге дейін адиабаталы ұлғаяды. Осы уақыттағы газдың температурасы 12,20-қа төмендейді. Осы белгілерге сүйеніп Ван – дер-Ваальстың теңдеуіндегі а тұрақтысын табу керек.
м3-ге дейін адиабаталы ұлғаяды. Осы уақыттағы газдың температурасы 12,20-қа төмендейді. Осы белгілерге сүйеніп Ван – дер-Ваальстың теңдеуіндегі а тұрақтысын табу керек.
6.21 1) Мына температураларда: а) 310С және б) 500С көмір қышқыл газын сұйық көмір қышқылына айналдыру үшін қандай қысым жұмсау керек болады? 2) 1 кг сұйық көмір қышқылының алатын ең үлкен көлемі қандай? 3) Сұйық көмір қышқылының буларының ең үлкен серпімділігі қандай?
6.22. Ван – дер – Ваальстың теңдеуіндегі 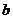 тұрақтысын белгілі деп алып, кризистік күйдегі су буларының тығыздығын табу керек.
тұрақтысын белгілі деп алып, кризистік күйдегі су буларының тығыздығын табу керек.
6.23 Гелий үшін 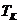 және
және 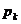 кризистік шамалардың мәнін белгілі деп алып, кризистік күйдегі гелийдің тығыздығын табу керек.
кризистік шамалардың мәнін белгілі деп алып, кризистік күйдегі гелийдің тығыздығын табу керек.
6.24 920 атмқысымда 1 кмоль оттегі 0,056 м3 көлемді алады. Келтірінді шамалармен алынған Ван – дер – Ваальс теңдеуін пайдаланып газдың температурасын табу керек.
6.25 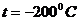 температурада 1 кмоль гелий
температурада 1 кмоль гелий 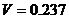 м3 көлемді алады. Келтірінді шамалармен алынған Ван – дер – Ваальс теңдеуін пайдаланып газдың қысымын табу керек.
м3 көлемді алады. Келтірінді шамалармен алынған Ван – дер – Ваальс теңдеуін пайдаланып газдың қысымын табу керек.
6.26 Газдың көлемі мен қысымы, осы шамалардың кризистік мәнінен екі есе үлкен болатындығын белгілі деп, газдың қысымы оның кризистік қысымынан неше есе үлкен болатындығын табу керек.
Не нашли, что искали? Воспользуйтесь поиском: