
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Химические свойства амфотерных оксидов
Амфотерные оксиды – твердые вещества, труднорастворимые в воде. Они взаимодействуют:
1) с сильными основаниями (щелочами), реакции между твёрдыми веществами, например:
Al2O3 + 6NaOH  2Na3AlO3 + 3H2O↑,
2Na3AlO3 + 3H2O↑,
ортоалюминат натрия
Al2O3 + 2NaOH  2NaAlO2 + H2O↑ или
2NaAlO2 + H2O↑ или
метаалюминат натрия
реакции в растворе: Al2O3 + 2NaOH + 3H2O → 2Na[Al(OН)4],
тетрагидроксоалюминат натрия
Al2O3 + 6NaOH + 3H2O → 2Na3[Al(OН)6].
гексагидроксоалюминат натрия
2) с кислотами (кроме оксидов алюминия Al2O3 и хрома Cr2O3), например:
CuO + 2HCl → CuCl2 + H2O,
PbO + 2CH3COOH → Pb(CH3COO) + H2O.
3) с кислотными и основными оксидами, например:
ZnO + SO3 → ZnSO4,
ZnO + K2O → K2ZnO2.
4) с простыми веществами металлами и неметаллами – сильными восстановителями, (кроме Al2O3), например:
Cr2O3 + 2Al → Al2O3 + 2Cr,
CuO + C → CO + Cu.
Гидроксиды
Гидроксидами называются сложные вещества – продукты взаимодействия оксидов с водой (это условное определение, т.к. большинство основных оксидов с водой не взаимодействует). Гидроксиды подразделяются на основания, кислородные кислоты и амфотерные гидроксиды.
Основания
Основаниями называют соединения, в которых положительно заряженный ион металла связан с отрицательно заряженными одним или несколькими гидроксид – ионами и при диссоциации в качестве анионов образуют только гидроксид – ионы 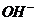 , к ним относятся: KOH, NH4OH, Ca(OH)2, Мg(OH)2 и т.д.
, к ним относятся: KOH, NH4OH, Ca(OH)2, Мg(OH)2 и т.д.
Основания –  классифицируют по следующим признакам:
классифицируют по следующим признакам:
1) По числу гидроксильных групп 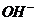 в молекуле основания – различают кислотность оснований и подразделяют их на:
в молекуле основания – различают кислотность оснований и подразделяют их на:
− однокислотные KOH, NаОН, NH4OH и др.;
− двухкислотные Ва(ОН)2, Ca(OH)2, Мg(OH)2 и др.
2) По степени растворимости в воде:
− растворимые (щелочи);
− труднорастворимые (смотри таблицу растворимости).
Большинство оснований труднорастворимо в воде. Растворимые в воде основания называются щелочами. Растворимые в воде основания образованы щелочными и щелочноземельными металлами. К растворимым основаниям относится гидроксид аммония NH4OH.
Труднорастворимые основания образованы остальными металлами, например: Мg(OH)2, Fe(OH)2 и др.
3) По степени диссоциации (α) различают:
− сильные электролиты α = 1;
− слабые электролиты α < 1.
Нужно помнить: ряды сильных и слабых оснований (таблица 3).
Номенклатура (название) оснований:
Таблица 3 – Формулы и названия оснований
Не нашли, что искали? Воспользуйтесь поиском: