
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
2 страница. 39. В чем заключается принцип несовместимости Паули?
39. В чем заключается принцип несовместимости Паули? Может ли быть на каком-нибудь подуровне атома p7 или d12-электронов? Почему? Составьте электронную формулу атома элемента с порядковым номером 22 и укажите его валентные электроны.
40. Составьте электронные формулы атомов элементов с порядковыми номерами 32 и 42, учитывая, что у последнего происходит провал одного
5s-электрона на 4d-подуровень. К какому электронному семейству относится каждый из этих элементов?
Периодическая система элементов Д. И. Менделеева
Пример 1.
Составьте электронные формулы атомов элементов № 20 и № 53. На каких энергетических уровнях и подуровнях находятся валентные электроны?
Решение.
Порядковый номер элемента, равный заряду ядра атома, указывает число электронов в структуре атома. Согласно принципу «минимума энергии» (см. пример 2.4) заполнение электронами энергетических уровней и подуровней идет в следующем порядке:
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, (5d1), 4f14, 5d2 - 10, 6p6, 7s2, (6d1 - 2), 5f14, 6d3 - 10, 7p.
Цифрой указывается значение главного квантового числа n – энергетический уровень, буквой - значение орбитального квантового числа l - энергетический подуровень. Индекс справа вверху показывает число электронов на данном подуровне. Суммарное число индексов должно совпадать с числом электронов в атоме, т. е. с его порядковым номером. При записи электронной формулы используют только главное и орбитальное квантовые числа.
Электронные формулы атомов элементов № 20 и № 53 имеют вид:
№ 20 (Ca) - 1s2, 2s2, 2p6, 3s2, 3p6, 4s2 ,
№ 53 (I) - 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p5.
Валентные электроны в атоме расположены на последнем энергетическом уровне и на заполняющемся подуровне. У Ca это 4s2, у I - 5s2 5p5. Поскольку в атоме кальция последним заполняется электронами s-подуровень, то он относится к семейству s-элементов, а I - к семейству p-элементов.
Пример 2.
Определите, каким элементам соответствуют приведенные электронные структуры:
а) …. 4s2 3d6,
б) …. 6s2 5d1 4f7,
в) …. 5s2 4d10 5p2?
Решение.
В электронной формуле главное квантовое число n (пишется цифрой) определяет энергетический уровень и совпадает с номером периода в периодической таблице Д. И. Менделеева. Число валентных электронов (электроны последнего энергетического уровня) равно номеру группы, в котором находится элемент.
В примере 2а n = 4, следовательно, элемент находится в четвертом периоде. Число валентных электронов (показатель степени в электронной формуле) равно
2 + 6 = 8, т. е. элемент расположен в восьмой группе - это железо.
В примере 2б n = 6, элемент шестого период, в атоме заполняется электронами f-подуровень (7  ) при частично заполненном d-подуровне (1
) при частично заполненном d-подуровне (1  ). Один электрон на d-подуровне имеет лантан № 57, за ним в таблице расположены лантаноиды (№ 58-71, f-элементы) и семь электронов на f-подуровне у гадолиния.
). Один электрон на d-подуровне имеет лантан № 57, за ним в таблице расположены лантаноиды (№ 58-71, f-элементы) и семь электронов на f-подуровне у гадолиния.
В примере 2в n = 5, элемент пятого периода. Валентные электроны 2 + 2 = 4, т. е. это элемент четвертой группы - олово.
Пример 3.
Заряды ядер элементов в периодической системе непрерывно увеличиваются, а свойства простых веществ повторяются периодически. Как это объяснить?
Решение.
Д. И. Менделеев заметил, что свойства элементов периодически повторяются с возрастанием значений их массовых чисел. Он расположил открытые к тому времени 63 элемента в порядке увеличения их атомных масс с учетом химических и физических свойств. Менделеев считал, что открытый им периодический закон является отражением глубоких закономерностей во внутреннем строении вещества, он констатировал факт периодических изменений свойств элементов, но причины периодичности не знал.
Дальнейшее изучение строения атома показало, что свойства веществ зависят от заряда ядра атомов, и элементы можно систематизировать, основываясь на их электронной структуре. Свойства простых веществ и их соединений зависят от периодически повторяющейся электронной структуры атомов и «электронные аналоги» являются также и «химическими аналогами».
Распишем электронные формулы атомов элементов главных подгрупп второй и седьмой групп.
Элементы второй группы имеют общую электронную формулу валентных электронов ns2. Распишем их электронные формулы:
Be 1s2 2s2,
Mg 1s2 2s2 2p6 3s2,
Ca 1s2 2s2 2p6 3s2 3p6 4s2,
Sr 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2.
У элементов седьмой группы общая электронная формула валентных электронов ns2 np5, а полные электронные формулы имеют вид:
F 1s2 2s2 2p5,
Cl 1s2 2s2 2p6 3s2 3p5,
Br 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5,
I 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p5.
Итак, электронные структуры атомов периодически повторяются у элементов одной группы, поэтому периодически повторяются и их свойства, так как они зависят в основном от электронного строения валентных электронов. Элементы одной группы имеют общие свойства, но есть и отличия. Это можно объяснить тем, что хотя атомы и имеют одинаковую электронную структуру валентных электронов, но эти электроны расположены на разном расстоянии от ядра, сила притяжения их к ядру при переходе от периода к периоду ослабевает, они становятся более подвижными, что отражается на свойствах веществ.
Задания
41. Исходя из положения германия, цезия и технеция в периодической системе, составьте формулы следующих соединений: мета и ортогерманиевой кислот, дигидрофосфата цезия и оксида технеция, отвечающего его высшей степени окислении. Изобразите графически формулы этих соединений.
42. Что такое энергия ионизации? В каких единицах она выражается? Как изменяется восстановительная активность s- и p-элементов в группах периодической системы с увеличением порядкового номера? Почему?
43. Что такое электроотрицательность? Как изменяется электроотрицательность р-элементов в периоде, в группе периодической системы с увеличением порядкового номера?
44. Исходя из положения германия, молибдена и рения в периодической системе, составьте формулы следующих соединений: водородного соединения германия, рениевой кислоты и оксида молибдена, отвечающего его высшей степени окисления. Изобразите графически формулы этих соединений.
45. Что такое сродство к электрону? В каких единицах оно выражается? Как изменяется окислительная активность неметаллов в периоде и в группе периодической системы с увеличением порядкового номера? Ответ мотивируйте строением атома соответствующего элемента.
46. Составьте формулы оксидов и гидроксидов элементов третьего периода периодической системы, отвечающих их высшей степени окисления. Как изменяется химический характер этих соединений при переходе от натрия к хлору?
47. Какой из элементов четвертого периода – ванадий или мышьяк – обладает более выраженными металлическими свойствами? Какой из элементов образует газообразное соединение с водородом? Ответ мотивируйте, исходя из строения атомов данных элементов.
48. Какие элементы образуют газообразные соединения с водородом? В каких группах периодической системы находятся эти элементы? Составьте формулы водородных и кислородных соединений хлора, теллура и сурьмы, отвечающих их низшей и высшей степеням окисления.
49. У какого элемента четвертого периода – хрома или селена – сильнее выражены металлические свойства? Какой из этих элементов образует газообразное соединение с водородом? Ответ мотивируйте строением атомов хрома и селена.
50. Какую низшую степень окисления проявляют хлор, сера, азот и углерод? Почему? Составьте формулы соединений алюминия с данными элементами в этой их степени окисления. Как называются соответствующие соединения?
51. У какого из p-элементов пятой группы периодической системы – фосфора или сурьмы – сильнее выражены неметаллические свойства? Какой из водородных соединений данных элементов более сильный восстановитель? Ответ мотивируйте строением атома этих элементов.
52. Исходя из положения металла в периодической системе, дайте мотивированный ответ на вопрос; какой из двух гидроксидов более сильное основание: Ba(OH)2 или Mg(OH)2; Ca(OH)2 или Fe(OH)2; Сd(ОН)2 или Sr(OH)2?
53. Почему марганец проявляет металлические свойства, а хлор – неметаллические? Ответ мотивируйте строением атомов этих элементов. Напишите формулы оксидов и гидроксидов хлора и марганца.
54. Какую низшую степень окисления проявляют водород, фтор, сера и азот? Почему? Составьте формулы соединений кальция с данными элементами в этой их степени окисления. Как называются соответствующие соединения?
55. Какую низшую и высшую степени окисления проявляют кремний, мышьяк, селен и хлор? Почему? Составьте формулы соединений данных элементов, отвечающих этим степеням окисления.
56. К какому семейству относятся элементы, в атомах которых последний электрон поступает на 4f- и 5f-орбитали? Сколько элементов включает каждое из этих семейств? Как отражается на свойствах этих элементов электронное строение их атомов?
57. Атомные массы элементов в периодической системе непрерывно увеличиваются, тогда, как свойства простых тел изменяются периодически. Чем это можно объяснить?
58. Какова современная формулировка периодического закона? Объясните, почему в периодической системе элементов аргон, кобальт, теллур и торий помещены соответственно перед калием, никелем, йодом и протактинием, хотя и имеют большую атомную массу?
59. Какую низшую и высшую степени окисления проявляют углерод, фосфор, сера и йод? Почему? Составьте формулы соединений данных элементов, отвечающих этим степеням окисления.
60. Какую высшую степень окисления могут проявлять германий, ванадий, марганец и ксенон? Почему? Составьте формулы оксидов данных элементов, отвечающих этой степени окисления.
Химическая связь и строение молекул.
Конденсированное состояние вещества
Пример 1.
Исходя из теории ковалентной связи, изобразите в виде валентных схем строение молекул: HCl, H2O, NH3.
Решение.
Согласно методу валентных схем (метод ВС), ковалентная связь образуется путем перекрывания электронных облаков неспаренных электронов. Эта связь двухэлектронная, двуцентровая.
Выпишем валентные электроны атомов, образующих указанные молекулы, и распределим их по орбиталям:
H 1s1,
Cl 2s2 2p5,
O 2s2 2p4,
N 2s2 2p3.
При образовании молекулы HCl происходит перекрывание неспаренных s-электрона атома водорода и p-электрона атома хлора:
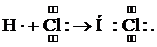
В молекуле воды перекрываются два неспаренных p-электрона атома кислорода и два s-электрона атомов водорода:
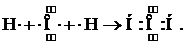
И, наконец, в молекуле аммиака три неспаренных p-электрона атома азота перекрываются с тремя s-электронами атомов водорода:
Н
 .
.
Во всех трех случаях у атомов при обобществлении электронов происходит достройка внешнего энергетического уровня до устойчивой двухэлектронной (гелиевой) конфигурации у атомов водорода или восьмиэлектронной (неоновой) у атомов кислорода и азота.
Пример 2.
Почему энергия двойной связи С = С (613,2 кДж) не равна удвоенному значению энергии одинарной связи С - С (348,6 кДж)?
Решение.
Энергия связи в значительной мере зависит от способа перекрывания электронных облаков при образовании связи. Если область перекрывания лежит на линии связи - это s-связь. Если область перекрывания электронных облаков перпендикулярна линии связи, то это p-связь. s- и p-связи неравноценны по энергии, прочнее s-связь.
s s s
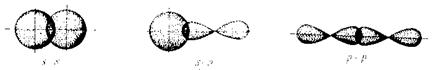
s–s s–p p–p
p p p
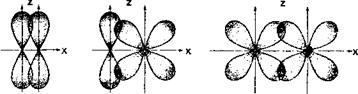
p–p p–d d–d
Соединяющиеся атомы не могут образовывать между собой более одной
s-связи. Поэтому одинарная связь С-С – это одна s-связь с энергией 348,6 кДж. 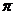 -связь двойной связи С=С равна 264,6 кДж, поэтому энергия двойной связи С=С не равна удвоенному значению одинарной связи С-С.
-связь двойной связи С=С равна 264,6 кДж, поэтому энергия двойной связи С=С не равна удвоенному значению одинарной связи С-С.
Пример 3.
Как изменяется полярность связи и прочность молекул в ряду HF, HCl, HBr, HI?
Решение.
Если ковалентная связь образована при взаимодействии разных атомов, то электронное облако связи всегда смещается к атому с большей относительной электроотрицательностью и связь будет полярной, т. е. полярность связи зависит от электроотрицательности атомов. Чем больше разность относительных электроотрицательностей, тем полярнее связь. Элементы F, Cl, Br, I находятся в одной группе периодической системы Д. И. Менделеева. В группе электроотрицательность сверху вниз падает, значит, самый электроотрицательный элемент - фтор и поэтому связь в молекуле будет самой полярной.
Приведенные в условии задачи молекулы двухатомны, и прочность их определяется прочностью связи водород-галоген. Прочность же связи при прочих равных условиях зависит от длины связи, т. е. от радиуса атома галогена. По группе сверху вниз радиусы атомов увеличиваются, длина связи галогена с водородом растет, а прочность связи соответственно падает, так как чем длиннее связь, тем она менее прочна. Уменьшается и прочность молекул.
Пример 4.
Какие химические связи имеются в ионах [NH4]+, [BF4]-?
Решение.
Напишем валентные электроны взаимодействующих атомов:
N 2s2 2p3,
B 2s2 2p1,
F 2s2 2p5,
H 1s1.
При образовании молекулы аммиака (см. пример 3.1) атом азота не исчерпал все валентные возможности, так как у него осталась свободной ещё одна пара электронов. При взаимодействии с ионом водорода H+, имеющего незанятую 1s-орбиталь, образуется ещё одна ковалентная связь:
NH3 + H+ 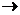 [NH4]+.
[NH4]+.
Такая ковалентная связь, когда атом-комплексообразователь (азот) предоставляет для образования связи пару электронов, а атом-лиганд - (водород) свободную орбиталь, называется дативной.
Для образования молекулы BF3 атом бора переходит в возбужденное состояние с тремя неспаренными электронами:
B 2s2 2p1 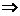 B* 2s1 2p2.
B* 2s1 2p2.
Три образующихся гибридных облака (sp2-гибридизация) перекрываются с тремя p-облаками трех атомов фтора и получается молекула BF3. Но у атома бора остается свободная орбиталь, а у иона фтора имеются свободные электронные пары (F0 + 1  = F-) Поэтому в ионе [BF4]- четвертая ковалентная связь образуется по донорно-акцепторному механизму:
= F-) Поэтому в ионе [BF4]- четвертая ковалентная связь образуется по донорно-акцепторному механизму:
BF3 + F- 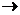 [BF4]-.
[BF4]-.
Атом бора - комплексообразователь дает для связи пустую орбиталь (акцептор), а ион фтора - лиганд, дает пару электронов (донор).
Итак, в ионах [NH4]+ и [BF4]- четыре ковалентные связи образованы разными способами:
а) одноэлектронный 1:1,
б) дативный 2:0,
в) донорно-акцепторный 0:2.
Первая цифра указывает число электронов комплексообразователя, вторая - лиганда.
Все четыре связи одинаковы по энергии, длине и другим параметрам, т. е. это не новый тип связи, а разные механизмы образования одной ковалентной связи.
Задания
61. Какую химическую связь называют ковалентной? Чем можно объяснить направленность ковалентной связи? Как метод валентных связей (ВС) объясняет строение молекулы воды?
62. Какая ковалентная связь называется s-связью и какая полярной? Что служит количественной мерой полярности ковалентной связи? Составьте электронные схемы строения молекул N2, H2O, HJ. Какие из них являются диполями?
63. Какой способ образования ковалентной связи называется донорно-акцепторным? Какие химические связи имеются в ионах [Cu(NH3)4]2+ и SbF4–? Укажите донор и акцептор.
64. Как метод валентных связей (ВС) объясняет линейное строение молекулы BeCl2 и тетраэдрическое – СН4?
65. Какая ковалентная связь называется s-связью и какая p-связью? Разберите на примере строения молекулы азота.
66. Сколько неспаренных электронов имеет атом хлора в нормальном и возбужденном состояниях? Распределите эти электроны по квантовым ячейкам. Чему равна валентность хлора, обусловленная неспаренными электронами?
67. Распределите электроны атома серы по квантовым ячейкам. Сколько неспаренных электронов имеют ее атомы в нормальном и возбужденном состояниях? Чему равна валентность серы, обусловленная неспаренными электронами?
68. Что называется электрическим моментом диполя? Какая из молекул HCl, HBr, HJ имеет наибольший момент диполя? Почему?
69. Какие кристаллические структуры называются ионными, атомными, молекулярными и металлическими? Кристаллы каких веществ: алмаз, хлорид натрия, диоксид, углерода, цинк – имеют указанные структуры?
70. Составьте электронные схемы строения молекул Сl2, H2S, ССl4. В каких молекулах ковалентная связь является полярной? Как метод валентных связей (ВС) объясняет угловое строение молекулы H2S?
71. Чем отличается структура кристаллов NаСl от структуры кристаллов натрия? Какой вид связи осуществляется в этих кристаллах? Какие кристаллические решетки имеют натрий и NaCl? Чему равно координационное число натрия в этих решетках?
72. Какая химическая связь называется водородной? Между молекулами каких веществ она образуется? Почему Н2O и НF, имея меньшую молекулярную массу, плавятся и кипят при более высоких температурах, чем их аналоги?
73. Какая химическая связь называется ионной? Каков механизм ее образования? Какие свойства ионной связи отличают её от ковалентной? Приведите два примера типичных ионных соединений. Напишите уравнения превращения соответствующих ионов в нейтральные атомы.
74. Что следует понимать под степенью окисления атома? Определите степень окисления атома углерода и его валентность, обусловленную числом неспаренных электронов в соединениях СН4, СН3ОН, НСООН, СО2.
75. Какие силы молекулярного взаимодействия называются ориентационными, индукционными и дисперсионными? Когда возникают и какова природа этих сил?
76. Какая химическая связь называется координационной или донорно-акцепторной? Разберите строение комплексного иона [Zn(NH3)4]2+. Укажите донор и акцептор. Как метод валентных связей (ВС) объясняет тетраэдрическое строение этого иона?
77. Какие электроны атома бора участвуют в образовании ковалентных связей? Как метод валентных связей (ВС) объясняет симметричную треугольную форму молекулы BF3?
78. Как метод молекулярных орбиталей объясняет парамагнитные свойства молекулы кислорода? Нарисуйте энергетическую схему образования молекулы O2 по методу молекулярных орбиталей (МО).
79. Нарисуйте энергетическую схему образования молекулы F2 по методу МО. Сколько электронов находится на связывающих и разрыхляющих орбиталях?
80. Как метод молекулярных орбиталей объясняет большую энергию диссоциации молекулы азота? Нарисуйте энергетическую схему образования молекулы N2 по методу МО. Сколько электронов находится на связывающих и разрыхляющих орбиталях?
Энергетика химических процессов
(термохимические расчеты)
Пример 1.
Вычислите энтальпию образования хлорида меди, если известно, что при образовании 8,10 г этой соли выделилось 13,39 кДж тепла.
Решение.
Раздел химии, в котором изложено количественное изучение тепловых эффектов реакций, называется термохимией. Было установлено, что если при образовании соединения выделяется какое-то количество теплоты, то при разложении этого соединения в тех же условиях то же количество теплоты поглощается. Таким образом, в любом процессе соблюдается закон сохранения энергии:
Q = DU + A.
Это равенство показывает, что если к системе подвести теплоту Q, то она расходуется на изменение ее внутренней энергии DU = U2 - U1 и на совершение работы A. Если давление постоянно, то Qp = DU + PDV. Сумму DU + PDV обозначили H и назвали энтальпией (теплосодержанием) системы.
Стандартной энтальпией образования DH0 называется изменение энтальпии в реакции образования 1 моля химического соединения из простых веществ при стандартных условиях (298 К, 101325 Па). Энтальпия образования простых веществ приравнивается к нулю.
Запишем термохимическое уравнение реакции образования хлорида меди:
Cu(К) + Cl2(Г) = CuCl2(К) DH0 -?
Мольная масса хлорида меди - 134,44 г/моль. При образовании 8,10 г этой соли выделилось 13,39 кДж тепла. Чтобы найти стандартную энтальпию, рассчитаем количество теплоты, выделяющееся при образовании 134,44 г (1 моля) хлорида меди:
DH0 =  = 222,24 кДж.
= 222,24 кДж.
Пример 2.
Вычислите теплоту образования оксида железа, исходя из уравнения
8Al + 3Fe3O4 = 4Al2O3 + 9Fe, DH0 = -3326 кДж.
Энтальпия образования оксида алюминия равна 1669 кДж/моль.
Решение.
В основе термохимических расчетов лежит закон Гесса: «Тепловой эффект реакции зависит только от конечного и начального состояния веществ и не зависит от промежуточных стадий процесса». Часто в термохимических расчетах используется следствие из закона Гесса: «Тепловой эффект реакции равен сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом коэффициентов реакции»:
DH0х.р. = 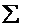 n × DH0продуктов -
n × DH0продуктов - 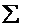 n × DH0исходных веществ.
n × DH0исходных веществ.
Распишем тепловой эффект реакции восстановления железа, используя следствие из закона Гесса:
DH0х.р. = (9 · DH0(Fe) + 4 · DH0(Al2O3) - (8 · DH0(Al) + 3 · DH0(Fe3O4).
Поскольку энтальпии образования простых веществ равны нулю, а теп-ловой эффект реакции и энтальпия образования оксида алюминия даны в условии задачи, то можно рассчитать энтальпию образования оксида железа.
-3326 = [9 · 0 + 4 · (-1669)] - (2 · 0 + 3DH0(Fe3O4),
DH0(Fe3O4) = 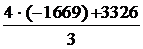 = -1116,7 кДж/моль.
= -1116,7 кДж/моль.
Пример 3.
Вычислите энтальпию перехода графита в алмаз, если известно, что энтальпия образования CO2 из графита равна - 393,5 кДж/моль, а из алмаза -
395,4 кДж/моль.
Решение.
Разность энтальпий реакций, идущих от различных начальных фазовых состояний к одинаковому конечному состоянию продукта, есть энтальпия фазового перехода. Энтальпию перехода графита в алмаз измерить непосредственно невозможно, но ее можно рассчитать по разности энтальпий сгорания графита и алмаза. Распишем эти термохимические уравнения:
1. С(графит) + O2 (Г) = CO2(Г), DH1 = -393,3 кДж,
2. С(алмаз) + O2(Г) = CO2(Г), DH2 = -395,4 кДж,
DH0превращ. = DH0сгорания С(гр.) - DHсгорания С(алмаза) = DH1 - DH2 =
= [(-393,3) - (-395,4)] = 2,1 кДж.
Задания
81. Вычислите тепловой эффект реакции восстановления 1 моль Fe2О3 металлическим алюминием. Ответ: –847,7,кДж.
82. Газообразный этиловый спирт С2H5ОН можно получить при взаимодействии этилена С2H4 (г) и водяных паров. Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект. Ответ: –45,76 кДж.
83. Вычислите тепловой эффект реакции восстановления оксида железа(II) водородом, исходя из следующих термохимических уравнений:
FeO (к) + СО (г) = Fe (к) + СО2 (г); DH = –13,18 кДж
СО (г)+ 1/2O2 (г) = СО2, (г); DH = –283,0 кДж
Н2 (г) + 1/2О2 (г) = Н20 (г); DH = –241,83 кДж
Ответ: +27,99 кДж.
84. При взаимодействии газообразных сероводорода и диоксида углерода образуются пары воды и сероуглерод CS2 (г). Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект. Ответ: +65,43 кДж.
85. Напишите термохимическое уравнение реакции между СО (г) и водородом, в результате которой образуются СН4 (г) и H2O (г). Сколько теплоты выделится при этой реакция? Ответ: 206,16 кДж.
86. При взаимодействии газообразных метана и сероводорода образуются сероуглерод CS2 (г) и водород. Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект. Ответ: +230,43 кДж.
87. Кристаллический хлорид аммония образуется при взаимодействии газообразных аммиака и хлорида водорода Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект. Сколько теплоты выделится, если в реакции было израсходовано 10 л аммиака в пересчете на нормальные условия? Ответ: 78,97 кДж.
88. Вычислите энтальпию образования метана, исходя из следующих термохимических уравнений:
H2 (г) + 1/2О2 (г) = Н2О (ж) DH = –285,84 кДж
С (к) + О2, (г) = СО2, (г); DH =.–393,51 кДж
СН4 (г) + 2О2, (г) = 2Н2О (ж) + СО (г); DH = –890,81 кДж
Ответ: –74,88 кДж.
89. Вычислите энтальпию образования гидроксида кальция, исходя из следующих термохимических уравнений:
Са (к) + 1/2О2, (г) = СаО (к); DH = –635,60 кДж
Н2, (г) +1/2О2 (г) = Н2О (ж); DH = –285,84 Дж
СаО (к) + Н2О (ж) = Са(ОН)2 (к); DH = –65,06 кДж
Ответ; –986,50 кДж.
Не нашли, что искали? Воспользуйтесь поиском: