
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
5 страница. 189. Какое из веществ KHCO3, CH3COOH, NiSQ4, Na2S будет взаимодействовать с раствором серной кислоты?
в) NH4Cl и Ba(OH)2.
189. Какое из веществ KHCO3, CH3COOH, NiSQ4, Na2S будет взаимодействовать с раствором серной кислоты? Выразите эти реакции молекулярными и ионно-молекулярными уравнениям.
190. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) Hg(NO3)2 и NaJ; б) Pb(NO3)2 и KJ
в) CdSO4 и Na2S.
191. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) СаСO3 + 2Н+ = Ca2+ + H2O + CO2
б) А1(ОН)3 + ОH– =А1O 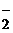 + 2Н2O
+ 2Н2O
в) РЬ2+ + 2J– =РbJ2.
192. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Ве(ОН)2 и NaOH; б) Сu(ОН)2 и HNO3;
в) ZnOHNO3 и HNO3.
193. Составите, молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) Na3PO4 и CaCl2; б) К2СО3 и BaCI2;
в) Zn(OH)2 и КОН.
194. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Fe (ОН)3 + 3Н+ = Fe3+ + 3Н2О
в) Cd2+ + 2OH– = Cd(OH)2
в) H+ + NO 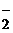 = HNO2
= HNO2
195. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) CdS и HCI; б) Cr(OH)3 и NaOH; в) Ва(ОН)2 и CoCI2.
196. Составьте молекулярные уравнения реакции, которые выражаются ионно-молекулярными уравнениями:
а) Zn2+ + H2S = ZnS + 2H+
я) HCO 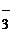 + H+ = H2O + CO2
+ H+ = H2O + CO2
в) Ag+ + Cl– = AgCI
197. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) H2SO4 и Ва(ОН)2; б) FeCl3 и NH4OH;
в) CH3COONa и HCI.
198. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) FeCl3 и КОН; б) NiSO4 и (NH4)2S;
в) MgCO3 и HNO3.
199. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Be (ОН)2 + 2 ОН– = BeO  + 2H2O
+ 2H2O
б) СН3СОО– + Н+ = СН3СООН
в) Ba2+ + SO  = BaSO4
= BaSO4
200. Какое из веществ: NaCl, NiSO4, Ве(ОН)2, KHCO3 будет взаимодействовать с раствором гидроксида натрия. Выразите эти реакции молекулярными и ионно-молекулярными уравнениями.
Гидролиз солей
Пример 1.
Какое значение pH (больше или меньше 7) имеют растворы следующих солей: Na2SO4, Na2S, NaCl, CuSO4? Ответ мотивируйте, составив молекулярные и ионные уравнения гидролиза соответствующих солей.
Решение.
Гидролиз солей - это реакция обменного разложения между водой и ионами соли, ведущая к образованию слабого электролита, нарушающая диссоциацию воды и, как правило, изменяющая pH раствора. Поэтому гидролизу не подвергаются соли, образованные сильным основанием и сильной кислотой, так как они не могут дать слабых электролитов.
Если гидролизу подвергаются многозарядные ионы, гидролиз всегда протекает ступенчато с преобладанием первой стадии и образованием основных и кислых солей. Гидролиз можно усилить, если раствор подогреть или сильно разбавить.
Из солей, приведенных в условии задачи, NaCl и Na2SO4 образованы сильными основаниями и сильными кислотами, поэтому они гидролизу не подвергаются, pH растворов этих солей будет примерно равен 7.
Соль Na2S образована сильным основанием NaOH и слабой кислотой H2S. Гидролиз пойдет по слабому звену - аниону ступенчато:
Na2S D 2Na+ + S2-,
S2- + HOH D HS- + OH-,
Na2S + H2O D NaHS + NaOH.
Выше записано краткое ионное уравнение гидролиза. Чтобы написать на его основе молекулярное уравнение, необходимо к ионам краткого ионного уравнения дописать до компенсации зарядов противоионы от исходной соли, в данном случае ионы Na+.
Соль CuSO4 образована слабым основанием Cu(OH)2 и сильной кислотой H2SO4. Гидролиз пойдет по слабому звену - катиону Cu2+:
CuSO4 D Cu2+ + SO  .
.
Краткое ионное уравнение гидролиза:
Cu2+ + HOH D (CuOH)+ + H+.
Молекулярное уравнение гидролиза:
2CuSO4 + 2H2O D (CuOH)2SO4 + H2SO4.
Пример 2.
Составьте молекулярные и ионные уравнения гидролиза, происходящего при сливании растворов Cr2(SO4)3 и H2S, зная, что образующийся сульфид хрома не существует в водной среде и полностью гидролизуется.
Решение.
При сливании растворов солей происходит следующая обменная реакция:
Cr2(SO4)3 + 3K2S D Cr2S3 + 3K2SO4.
Соль K2SO4 образована сильным основанием KOH и сильной кислотой H2SO4 и гидролизу не подвергается. Соль Cr2S3 образована слабым основанием Cr(OH)3 и слабой кислотой H2S, поэтому гидролиз пойдет по катиону и по аниону до конца.
Краткое ионное уравнение гидролиза соли Cr2S3:
2Cr3+ + 3S2- + 6HOH D 2Cr(OH)3¯ + 3H2S.
Молекулярное уравнение реакции с учетом гидролиза соли:
Cr2(SO4)3 + 3K2S + 6H2O D 3K2SO4 + 2Cr(OH)3¯ + 3H2S.
Задания
201. Составьте ионно-молекулярное и молекулярное уравнения совместного гидролиза, происходящего при смешивании растворов K2S и AlCl3. Каждая из взятых солей гидролизуется необратимо до конца.
202. Какое значение рН (>7,»7,<7) имеют растворы солей МnСl2, Na2CO3, Ni(NO3)2? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
203. Какие из солей Al2(SО4)3, K2S, Pb(NO3)2, КС1 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
204. При смешивании растворов FeCl3 и Na2CO3, каждая из взятых солей гидролизуется необратимо до конца. Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями.
205. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей CH3COOK, ZnSO4, AI(NO3)3. Какое значение рН (>7,»7, <7) имеют растворы этих солей?
206. Какое значение рН (>7,»7, <7) имеют растворы солей Li2S, А1Сl3, NiSO4? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
207. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей РЬ(NO3)2, Na2CO3, CoCl2. Какое значение рН (>7,»7, <7) имеют растворы этих солей?
208. Составьте ионно-молекулярное и молекулярное уравнения гидролиза соли, раствор которой имеет: а) щелочную реакцию; б) кислую реакцию..
209. Какое значение рН (>7,»7, <7) имеют растворы солей Na3PO4, K2S, CuSО4? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
210. Составьте ионные и молекулярные уравнения гидролиза солей CuCl2, Cs2CO3, ZnCl2. Какое значение рН (>7,»7, <7) имеют растворы этих солей?
211. Какие из солей RbCI, Cr2(SO4)3, Ni(NO3)2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
212. При смешивании растворов CuSO4 и K2CO3 выпадает осадок основной соли (CuOH)2CO3 и выделяется CO2. Составьте ионно-молекулярное и молекулярное уравнения происходящего гидролиза
213. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей K2S, Cs2CO3, NiCl2, Рb(СН3СОО)2. Какое значение рН (>7,»7, <7) имеют растворы этих солей?
214. При смешивании растворов AI2(SO4)3 и Na2CO3 каждая из взятых солей гидролизуется необратимо до конца. Составьте ионно-молекулярное и молекулярное уравнения происходящего совместного гидролиза.
215. Какие из солей NaBr, Na2S, K2CO3, СоСl2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
216. Какие из солей KNO3, CrCl3, Cu(NО3)2, NаСN подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
217. Составьте ионно-молекулярное и молекулярное уравнения совместного гидролиза, происходящего при смешивания растворов Сr(NО3)3 и Na2S? Каждая из взятых солей гидролизуется необратимо до конца.
218 Какое значение рН (>7,»7, <7) имеют растворы следующих солей: К3РO4, Рb(NОз)2, Na2S? Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей.
219. Какие из солей К2СО3, FeCl3, K2SO4, ZnCl2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
220. При смешивании растворов Al2(SO4)3 и Na2S каждая из взятых солей гидролизуется необратимо до конца. Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями.
КОНТРОЛЬНОЕ ЗАДАНИЕ 2
Окислительно-восстановительные реакции
Пример 1.
Какие из приведенных ниже реакций являются окислительно-восстановительными? Укажите для каждой из них окислитель и восстановитель.
1. Fe + 2HCl = FeCl2 + H2.
2. FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl.
3. Ba(NO3)2 + K2SO4 = BaSO4 + 2KNO3.
4. 2KI + Cl2 = 2KCl + I2.
Решение.
Окислительно-восстановительными называются реакции, протекающие с изменением степеней окисления атомов. Степень окисления – это условный заряд, появляющийся на атоме в результате смещения электронного облака к более электроотрицательному атому. Степень окисления может быть отрицательной, положительной и нулевой.
Окисление – это процесс отдачи электронов, сопровождающийся повышением степени окисления. Атомы, молекулы и ионы, отдающие электроны, называются восстановителями.
Восстановление – процесс присоединения электронов, сопровождающийся понижением степени окисления. Атомы, молекулы и ионы, принимающие электроны, называют окислителями.
Определим степени окисления атомов.
1.  + 2
+ 2  Cl =
Cl =  Cl2 +
Cl2 +  2.
2.
Железо и водород меняют степени окисления. Следовательно, данная реакция относится к окислительно-восстановительным:
 - 2
- 2  =
=  – процесс окисления, железо – восстановитель.
– процесс окисления, железо – восстановитель.
2  + 2
+ 2  =
=  2 – процесс восстановления, ион водорода – окислитель.
2 – процесс восстановления, ион водорода – окислитель.
2. 
 2 + 2
2 + 2 
 =
=  2 + 2
2 + 2  .
.

Степени окисления атомов в веществах не изменяются, поэтому реакция не является окислительно-восстановительной.
3.  (
( 3)2 +
3)2 +  = 2
= 2  3 +
3 + 
Эта реакция также не относится к окислительно-восстановительным, степени окисления атомов постоянны.
4. 2K  +
+  2 = 2K
2 = 2K  +
+  2.
2.
Хлор и йод меняют степени окисления, это - окислительно-восстано-вительная реакция:
2  -2
-2  =
=  2– процесс окисления, ион йода – восстановитель,
2– процесс окисления, ион йода – восстановитель,
 2 + 2
2 + 2  = 2
= 2  – процесс восстановления, молекула хлора – окислитель.
– процесс восстановления, молекула хлора – окислитель.
Пример 2.
Какой процесс окисления или восстановления происходит при следующих превращениях:

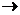
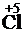 ;
; 
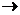
 ;
; 
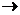
 ;
;

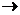
 ;
; 
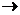
 ;
; 
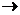
 ?
?
Решение.
Повышение степени окисления происходит в результате отдачи электронов (окисления), понижение – за счет присоединения электронов (восстановления):

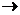
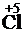
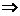
 - 6
- 6  =
= 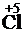 – окисление,
– окисление,

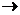

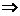
 - 8
- 8  =
=  – окисление,
– окисление,

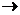

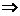
 + 3
+ 3  =
=  – восстановление,
– восстановление,

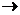

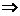
 - 2
- 2  =
=  – окисление,
– окисление,

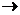

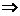
 - 3
- 3  =
=  – окисление,
– окисление,

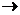

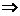
 + 1
+ 1  =
=  – восстановление.
– восстановление.
Пример 3.
Реакция выражается схемами:
1. KClO3 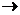 KClO4 + KCl.
KClO4 + KCl.
2. (NH4)2S + K2Cr2O7 + H2O 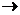 S + Cr(OH)3 + NH3 + KOH.
S + Cr(OH)3 + NH3 + KOH.
Составьте электронные уравнения, расставьте коэффициенты, укажите окислитель и восстановитель.
Решение.
Для подбора коэффициентов уравнения воспользуемся методом электронного баланса.
1. Записываем уравнение реакции и находим атомы, меняющие степень окисления:
K  O3 ® K
O3 ® K  O4 + K
O4 + K  .
.
2. Составляем электронные уравнения и находим окислитель и восстано-витель:
Cl+5 – 2  = Cl+7, Cl+5 – восстановитель,
= Cl+7, Cl+5 – восстановитель,
Cl+5 + 6  = Cl–1, Cl+5 – окислитель.
= Cl–1, Cl+5 – окислитель.
В этом уравнении Cl+5(KClO3) является одновременно и окислителем, и восстановителем. Такая окислительно-восстановительная реакция называется реакцией диспропорционирования (самоокисления-самовосстановления).
3. Находим коэффициенты для окислителя, восстановителя и продуктов их превращения. Число электронов, отданных восстановителем, должно быть равно числу электронов, принятых окислителем. Для этого находим наименьшее общее кратное и множители:

 Cl+5 – 2
Cl+5 – 2  = Cl+7 3 (1)
= Cl+7 3 (1)
Cl+5 + 6  = Cl– 1 (2)
= Cl– 1 (2)
Ставим эти множители в уравнение (1). Перед KClO3 ( ) ставится суммарный множитель (3 + 1 = 4). Коэффициенты у формул остальных веществ подбираются как обычно, путем сопоставления числа атомов в правой и левой частях уравнения:
) ставится суммарный множитель (3 + 1 = 4). Коэффициенты у формул остальных веществ подбираются как обычно, путем сопоставления числа атомов в правой и левой частях уравнения:
4KClO3 = 3KClO4 + KCl.
По той же методике расставим коэффициенты во втором уравнении:
3(NH4)2S–2 + K2Cr2+6O7 + H2O = 3S0 + 2Cr+3(OH)3 + 2KOH + 6NH3
 |  |
S–2 – 2  = S0 3
= S0 3
Cr+6 + 6  = 2Cr+3 1
= 2Cr+3 1
Пример 4.
Диоксид азота при растворении в воде образует смесь двух кислот. Напишите уравнение реакции.
Решение.
Исходными веществами являются вода и диоксид азота NO2. Кислород и водород имеют в молекуле воды степени окисления (-2) и (+1), характерные и устойчивые для них. Следовательно, реакция происходит только за счет изменения степени окисления азота. В молекуле NO2 азот находится в промежуточной степени окисления (+4), он может и отдавать, и принимать электроны по схеме:
N+4 – 1  = N+5 – окисление,
= N+5 – окисление,
N+4 + 1  = N+3 – восстановление.
= N+3 – восстановление.
Поэтому при растворении NO2 в воде образуются азотная ( ) и азотистая (
) и азотистая ( ) кислоты:
) кислоты:
2NO2 + H2O = HNO3 + HNO2.
Задания
221. Исходя из степени окисления хлора в соединениях HCl, HClO3, НСlO4, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
КВr + KВrO2 + H2SO4 ® Br2 + K2SO4 + Н2О.
222. Реакции выражаются схемами
P + HJO3 + H2O ® H3PO4 + HJ,
KMnO4 + KNO2 + H2SO4 = MnSO4 + KNO3 + K2SO4 + H2O.
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое – восстановителем; какое вещество окисляется, какое – восстанавливается.
223. Составьте электронные уравнения и укажите, какой процесс – окисление или восстановление – происходит при следующих превращениях:
As3– ® As5+; N3++ ® N3–; S2– ® S°.
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
Na2SO3 + KMnO4+ Н2О ® Na2SO4 + MnO2 + KOH.
224. Исходя из степени окисления фосфора в соединениях РН3, Н3РО4, Н3РО3, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему? На основании электронных уравнений расставьте коэффициента в уравнении реакции, идущей по схеме
PbS + HNO3 ®S + Pb (NO3)2 + NO + H2O.
225. Реакции выражаются схемами.
Не нашли, что искали? Воспользуйтесь поиском: