
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
4 страница. 132. Напишите выражение для константы равновесия гетерогенной системы CО2 + С D 2CO
132. Напишите выражение для константы равновесия гетерогенной системы CО2 + С D 2CO. Как изменится скорость прямой реакции – образования СО, если концентрацию СО2 уменьшить в четыре раза? Как следует изменить давление, чтобы повысить выход СО?
133. Напишите выражение для константы равновесия гетерогенной системы C + H2O (г) D СО + Н2. Как следует изменить концентрацию и давление, чтобы сместить равновесие в сторону обратной реакции – образования водных паров?
134. Равновесие гомогенной системы
4HCl (г) +O2 (г) D 2H2О (г) + Cl2 (г)
установилось при следующих концентрациях реагирующих веществ: [Н2О] = 0,14 моль/л; [Сl2] = 0,14 моль/л; [НС1] = 0,20 моль/л; [O2] = 0,32 моль/л. Вычислите исходные концентрации хлороводорода и кислорода
Ответ: [HCI]исх. = 0,48 моль/л; [О2]исх. = 0,39 моль/л.
135. Вычислите константу равновесия для гомогенной системы
СО (г) + Н2О (г) D СО2 (г) + Н2 (г)
если равновесные концентрации реагирующих веществ: [СО] = 0,004 моль/л; [H2O] = 0,064 моль/л; [СО2] = 0,016 моль/л; [H2]-=0,016 моль/л. Ответ: К = 1.
136. Константа равновесия гомогенной системы
СО (г) + Н2О (г) D СО2 (г) + Н2 (г)
при некоторой температуре равна 1. Вычислите равновесные концентрации всех реагирующих веществ, если исходные концентрации: [CO] = 0,10 моль/л;
[H2O] = 0,40 моль/л. Ответ: [CO2] = [H2] = 0,08 моль/л [СО] = 0,02 моль/л;
[Н2О] = 0,32 моль/л.
137. Константа равновесия гомогенной системы N2 + 3H2 D 2NH3 при температуре 400 0С равна 0,1. Равновесные концентрации водорода и аммиака соответственно равны 0,2 и 0,08 моль/л. Вычислите равновесную и исходную концентрацию азота. Ответ: 8 моль/л; 8,04 моль/л.
138. При некоторой температуре равновесие гомогенной системы
2NO + O2 D 2N2 установилось при следующих концентрациях реагирующих веществ: [NO] = 0,2 моль/л; [О2] = 0,1 моль/л; [NO2] = 0,1 моль/л. Вычислите константу равновесия и исходную концентрацию NO и О2.
Ответ: К = 2,5; [NO] = 0,3 моль/л; [О2] = 0,15 моль/л.
139. Почему при изменении давления смещается равновесие системы
N2 + 3H2 D 2NH3 и не смещается равновесие системы N2 + O2 D 2NO? Напишите выражения для констант равновесия каждой из данных систем.
140. Исходные концентрации NO и Cl2 в гомогенной системе
2NО + Cl2 D 2NOCl составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если, к моменту наступления равновесия прореагировало
20 % NО. Ответ: 0,416.
Способы выражения концентрации растворов
Пример 1.
К 1 литру раствора с массовой долей HCl 20 % (d = 1,100 г/см3) добавили 400 см3 раствора с массовой долей HCl 5 % (d = 1,024 г/см3). Вычислите массовую долю HCl в полученном растворе.
Решение.
В условии задачи требуется рассчитать массовую долю (w), которая показывает, сколько граммов вещества растворено в 100 граммах раствора:
w =  ,
,
где m - масса растворенного вещества, г; r - плотность раствора, г/см3; V - объем раствора, мл.
Рассчитаем массу HCl, содержащейся в 1000 · 1,100 = 1100 г раствора из соотношения:
в 100 г раствора с массовой долей HCl 20 % содержится 20 г HCl,
в 1100 г раствора HCl содержится Х г HCl.
Отсюда, X =  = 220 г;
= 220 г;
400 см3 растворас массовой долей HCl 5 % весят m = r · V = 400 · 1,024 = 409,6 г, а количество HCl в этом растворе определим из соотношения:
в 100 г раствора с мвссовой долей HCl 5 % содержится 5 г HCl,
в 409,6 г - Х г HCl.
Найдем X: X = 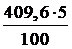 = 20,48 г.
= 20,48 г.
Общая масса раствора после сливания будет 1100 + 409,6 = 1509,6 г. Количество растворенной в нем кислоты будет 220 + 20,48 =240,48 г.
Массовую долю HCl и полученном растворе вычислим из соотношения:
в 1509,6 г раствора HCl содержится 240,48 г HCl,
в 100 г раствора HCl содержится Х г HCl.
Отсюда X =  = 15,93 г, а w (HCl) = 15,93 %.
= 15,93 г, а w (HCl) = 15,93 %.
Пример 2.
Вычислите молярную концентрацию раствора сульфата калия,
20 мл которого содержат 1,74 г этой соли.
Решение.
Молярная концентрация указывает на количество молей вещества в 1000 мл раствора. Ее вычисляют по формуле, (моль/л):
См =  моль/л,
моль/л,
где m - масса растворенного вещества, г; М - молярная масса растворенного вещества, г; V - объем раствора, мл.
Молярная масса сульфата калия (К2SO4) равна:
39,10 + 32,06 + 4 · 16 = 174 г/моль.
Рассчитаем массу сульфата калия, содержащегося в 1 литре раствора, из соотношения:
в 20 мл раствора К2SO4 содержится 1,74 г К2SO4;
в 1000 мл - Х г К2SO4.
Тогда Х =  = 87 г.
= 87 г.
Молярная масса сульфата калия 174,26 г/моль, а 87 г этой соли составят
87: 174,26 = 0,5 молей.
Итак, в 1 литре раствора сульфата калия содержится 0,5 молей этой соли. Следовательно, раствор 0,5 молярный (0,5 М). Эту же задачу можно решить по формуле
См =  = 0,5моль/л.
= 0,5моль/л.
Пример 3.
Сколько граммов оксида кальция содержится в 200 мл 0,3 н. раствора? Рассчитайте титр раствора.
Решение. Молярная концентрация эквивалентов или нормальная концентрация (Сэкв) показывает, сколько молей эквивалентов вещества содержится в 1 литре раствора, ее рассчитывают по формуле, (моль/л):
Сэкв =  .
.
Здесь m - масса растворенного вещества, г; Мэкв. - молярная масса эквивалента вещества, г/моль; V - объем раствора, мл.
Титр раствора (Т) показывает, сколько граммов вещества содержится в 1 мл раствора. Титр раствора связан с нормальной концентрацией соотношением, (г/мл):
Т = 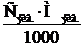 , г/мл,
, г/мл,
Рассчитаем молярную массу эквивалента гидроксида кальция:
Мэкв.Ca(OH)2 =  = 37 г/моль
= 37 г/моль
и массу Ca(OH)2 в 200 мл раствора по формуле
Сэкв =  . Þ Мэкв. =
. Þ Мэкв. =  = 2,22 мль/л.
= 2,22 мль/л.
Зная нормальную концентрацию раствора, можно рассчитать его титр:
Т =  = 0,0111 г/мл.
= 0,0111 г/мл.
Задания
141. Вычислите молярную и нормальную концентрации раствора с массовой долей хлорида кальция 20%, плотность которого 1,178 г/см3. Ответ: 2,1 М; 4,2 н.
142. Чему равна нормальная концентрация раствора с массовой долей NaOH 30 %, плотность которого 1,328 г/см3? К 1 л этого раствора прибавили 5 л воды. Вычислите массовую долю NaOH в полученнм растворе. Ответ: 9,96 н.; 6.3%.
143. К 3 л раствора с массовой долей HNO3 10%, плотность которого 1,054 г/см3, прибавили 5 л раствора той же кислоты с массовой долей 2% плотностью 1,009 г/см3. Вычислите массовую долю и молярную концентрации полученного раствора, если считать, что его объем равен 8 л. Ответ: 5,0 %; 0,82 М.
144. Вычислите нормальную и моляльную концентрации раствора HNO3 с массовой долей 20,8 %, плотность, которого 1,12 г/см3. Сколько граммов кислоты содержится в 4 л этого раствора? Ответ: 3,70 н.; 4,17 м; 931,8 г.
145. Вычислите молярную, нормальную и моляльную концентрации раствора с массовой долей хлорида алюминия 16 %, плотность которого 1,149 г/см3.
Ответ: 1,38 М; 4,14 н; 1,43 м.
146. Сколько и какого вещества останется в избытке, если к 75 см3 0,3 н. раствора H2SO4 прибавить 125 см3 0,2 н. раствора КОН? Ответ: 0,14 г КОН.
147. Для осаждения в виде AgCl всего серебра, содержащегося в 100 см3 раствора AgNO3, потребовалось 50 см3 0,2 н раствора НСl. Чему равна нормальная концентрация раствора AgNO3? Сколько граммов АgCl выпало в осадок?
Ответ: 0,1 н; 1,433 г.
148. Какой объем раствора с массовой долей НСl 20,01% (плотность
1,100 г/см3) требуется для приготовления 1 л раствора с массовой долей HCl
10,17 % (плотность 1,050 г/см3)? Ответ: 485,38 см3.
149. Смешали 10 см3 раствора с массовой долей HNO3 10 % (плотность 1,056 г/см3) и 100 см3 раствора с массовой долей HNO3 30 % (плотность 1,184 г/см3). Вычислите массовую долю HNO3 в полученном растворе. Ответ: 28,38 %.
150. Какой объем раствора с массовой долей КОН 50 % (плотность
1,538 г/см3) требуется для приготовления 3 л раствора с массовой долей КОН 6 % (плотность 1,048 г/см3)? Ответ: 245,5см3.
151. Какой объем раствора с массовой долей карбоната натрия 10 % (плотность 1,105 г/см3) требуется для приготовления 5 л раствора с массовой долей карбоната натрия 2 % (плотность 1,02 г/см3)? Ответ: 923,1 см3.
162. На нейтрализацию 31 см3 0,16 н. раствора щелочи требуется 217 см3 раствора H2SO3. Чему равны нормальная концентрация и титр раствора H2SO4?
Ответ: 0,023 н.; 1,127×10–3 г/см3.
153. Какой объем 0,3 н. раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г NaOH в 40 см3? Ответ: 26,6 см3.
154. На нейтрализацию I л раствора, содержащего 1,4 г КОН, требуется 50 см3 раствора кислоты. Вычислите нормальную концентрацию раствора кислоты.
Ответ: 0.53 н.
155. Сколько граммов HNO3 содержалось в растворе, если на нейтрализацию его потребовалось 35 см3 0,4 н. раствора NaOH? Чему равен титр раствора NaOH? Ответ: 0,882 г, 0,016 г/см3.
156. Сколько граммов NaNO3 нужно растворить в 400 г воды, чтобы приготовить раствор с массовой долей NaNO3 20 %? Ответ: 100 г.
157. Смешали 300 г раствора с массовой долей NaCl 20 % и 500 г раствора c массовой долей NaCl 40 %. Чему равна массовая доля NaCl в полученном растворе? Ответ: 32,5%.
158. Смешали 247 г раствора с массовой долей серной кислоты 62 % и 145 г раствора с массовой долей серной кислоты 18%. Какова массовая доля серной кислоты в полученном растворе после смешения?
Ответ: 45,72 %.
159. Из 700 г раствора серной кислоты с массовой долей 60 % выпариванием удалили 200 г воды. Чему равна массовая доля серной кислоты в оставшемся растворе? Ответ: 84 %.
160. Из 10 кг раствора с массовой долей растворенного вещества 20 % при охлаждении выделилось 400 г соли. Чему равна массовая доля растворенного вещества охлажденного раствора? Ответ 16,7 %.
Свойства растворов
Пример 1.
Вычислите температуры кристаллизации, и кипения раствора с массовой долей сахара C12H22O11 5 %.
Решение.
При растворении в растворителе нелетучего вещества давление пара растворителя над раствором уменьшается, что вызывает повышение температуры кипения раствора и понижение температуры его замерзания по сравнению с чистым растворителем. При этом, согласно закону Рауля, повышение температуры кипения (Dtкип.) и понижение температуры замерзания (Dtзам.) раствора пропорционально моляльной концентрации раствора:
DТк = Э · Cm, DТз = К · Сm.
Здесь Cm - моляльная концентрация раствора (число молей растворенного вещества в 1000 г растворителя); Э - эбуллиоскопическая константа растворителя, град; К - криоскопическая константа растворителя, град.
Так как молярная концентрация  ,
,
где m - масса растворенного вещества, г; M - молярная масса растворенного вещества, г/моль; m1 - масса растворителя, г, то формулы закона Рауля можно записать следующим образом:
DТк =  , DТз =
, DТз =  .
.
Эти формулы позволяют определить температуры замерзания и кипения растворов по их концентрации, а также находить молекулярную массу растворенного вещества по понижению температуры замерзания и повышению температуры кипения раствора.
Для воды криоскопическая константа (К) и эбуллиоскопическая константа (Э) соответственно равны 1,86 и 0,52 град. Молярная масса сахара 342 г/моль. Рассчитаем понижение температуры кристаллизации раствора с массовой долей сахара 5 %:
DТз =  = 0,29 °С.
= 0,29 °С.
Вода кристаллизуется при 0 °С, следовательно, температура кристал-лизации раствора будет 0 - 0,29 = - 0,29 °С.
Из формулы рассчитываем повышение температуры кипения этого раствора:
DТк =  = 0,06 °С.
= 0,06 °С.
Вода кипит при 100 °С. Следовательно, температура кипения этого раствора будет 100 + 0,06 = 100,06 °С.
Пример 2.
Рассчитайте, при какой температуре будет кристаллизоваться раствор, содержащий в 200 г бензола, 12 г нафталина?
Решение.
Криоскопическая константа бензола равна 5,10 град. Молярная масса нафталина C10H8 = 128 г/моль. Из формулы понижение температуры замерзания этого раствора
DТз =  = 2,38 °С.
= 2,38 °С.
Бензол кристаллизуется при 5,53 °С. Таким образом, температура кристаллизации раствора равна: 5,5 - 2,38 = 2,15 °С.
Пример 3.
В каком количестве воды следует растворить 20 г глюкозы, чтобы получить раствор с температурой кипения 100,2 °С?
Решение.
Температура кипения воды 100 °С. Повышение температуры кипения раствора DТк = 100,2 - 100 = 0,2 °С. Молярная масса глюкозы
C6H12O6 - 180 г/моль.
Из формулы находим количество воды, в котором нужно растворить 20 г глюкозы, чтобы получить раствор с температурой кипения 100,2 °С:
DТк =  ,
, 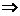 m1 =
m1 =  , =
, =  = 289 г.
= 289 г.
Пример 4.
При растворении 6,9 г глицерина в 500 г воды температура замерзания понизилась на 0,279 °С. Определите молярную массу глицерина.
Решение.
Для расчета молярной массы глицерина преобразуем формулу и подставим известные величины:
DТз =  .
. 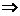 M =
M =  =
=  = 92 г/моль.
= 92 г/моль.
Здесь 1,86 - криоскопическая константа воды.
Пример 5.
Раствор, приготовленный из 1 кг этилового спирта (C2H5OH) и 9 кг воды, залили в радиатор автомобиля. Вычислите температуру замерзания раствора.
Решение.
Молярная масса этилового спирта равна 44 г/моль, криоскопическая константа - 1,85 град. По формуле находим понижение температуры замерзания раствора:
DТз =  . DТз =
. DТз =  = 4,7 °С.
= 4,7 °С.
Вода кристаллизируется при 0 °С, следовательно, температура кристаллизации раствора этилового спирта будет 0 - 4,7 = - 4,7 °С.
Задания
161. Раствор, содержащий 0,512 г неэлектролита в 100 г бензола, кристаллизуется при 5,296°С. Температура кристаллизации бензола 5,5 °С. Криоскопическая константа 5,1 град. Вычислите мольную массу растворенного вещества.
Ответ: 128 г/моль.
162. Вычислите массовую долю сахара С12Н22О11 в водном растворе, зная температуру кристаллизации раствора (–0,93 °С). Криоскопическая константа воды 1,86 град. Ответ: 14,6 %.
163. Вычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды
1,86 град.
164. Раствор, содержащий 3,04 г камфары C10H16O в 100 г бензола, кипит при 80,714 °С. Температура кипения бензола 80,2 °С. Вычислите эбуллиоскопическую константу бензола.
165. Вычислите массовую долю водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,39°С. Эбуллиоскопическая константа воды 0,52 град. Ответ: 6,45 %.
166. Вычислите мольную массу неэлектролита, зная, что раствор, содержащий 2,25 г этого вещества в 250 г воды, кристаллизуется при –0,279°С. Криоскопическая константа воды 1,86 град. Ответ: 60 г/моль.
167. Вычислите температуру кипения раствора с массовой долей нафталина С10Н8 5 % в бензоле. Температура кипения бензола 80,2 °С. Эбуллиоскопическая константа его 2,57 град. Ответ: 81,25 °С.
168. Раствор, содержащий 25,65 г некоторого неэлектролита в 300 г воды, кристаллизуется при –0,465 °С. Вычислите мольную массу растворенного вещества. Криоскопическая константа воды 1,86 град. Ответ: 342 г/моль.
169. Вычислите криоскопическую константу уксусной кислоты, зная, что раствор, содержащий 3,56 г антрацена С14H10 в 100 г уксусной кислоты, кристаллизуется при 15,718 °С. Температура кристаллизации уксусной кислоты 16,65 °С.
170. Равные массовые количества камфары С10Н16О и нафталина С10Н8 растворены в одинаковых количествах бензола. Какой из растворов кипит при более высокой температуре?
171. Температура кристаллизации раствора, содержащего 66,3 г некоторого неэлектролита в 500 г воды, равна –0,558 0С. Вычислите мольную массу растворенного вещества. Криоскопическая константа воды 1,86 град. Ответ: 442 г/моль.
172. Сколько граммов анилина C6H5NH2 следует растворить в 50 г этилового эфира чтобы температура кипения раствора была выше температуры кипения этилового эфира на 0.53 0С. Эбуллиоскопическая константа этилового эфира
2,12 град. Ответ: 1,16 г.
173. Вычислите температуру кристаллизации раствора с массовой долей этилового спирта C2H5OH 2 %, зная, что криоскопическая константа воды
1,86 град. Ответ: –0,82 °С.
174. Сколько граммов мочевины (NH2)2CO следует растворить в 75 г воды, чтобы температура кристаллизации понизилась на 0,465 0C? Криоскопическая константа воды 1,86 град. Ответ: 1,12 г,
175. Вычислите массовую долю глюкозы С6Н12О6 в водном растворе, зная, что этот раствор кипит при 100,26 0С. Эбуллиоскопическая константа воды
0,52 град. Ответ: 8,25 %.
176. Сколько граммов фенола С6Н5ОН следует растворить в 125 г бензола, чтобы температура кристаллизации раствора была ниже температуры кристаллизации бензола на 1,7 0С? Криоскопическая константа бензола 5,1 град.
Ответ: 3,91 г.
177. Сколько граммов мочевины (NH2)2CO следует растворить в 250 г воды, чтобы температура кипения повысилась на 0,26 °С? Эбуллиоскопическая константа воды 0,52 град. Ответ: 7,5 г.
178. При растворении 2,3 г некоторого неэлектролита в 125 г воды температура кристаллизации понижается на 0,372 0С. Вычислите мольную массу растворенного вещества. Криоскопическая константа воды 1,86 град.
Ответ: 92 г/моль.
179. Вычислите температуру кипения водного раствора с массовой долей пропилового спирта C3H7OН 15 %, зная, что эбуллиоскопическая константа воды 0,52 град. Ответ: 101,52 0С.
180. Вычислите массовую долю метанола CH3OH в воде, температура кристаллизации которого –2,79 °С. Криоскопическая константа воды 1,86 град.
Ответ: 4,58 %.
Ионно-молекулярные (ионные) реакции обмена
Пример 1.
Составьте молекулярные и ионные уравнения реакций, протекающих между веществами:
1. AgNO3 + FeCl3 ®
2. Na2S + HCl ®
3. HCN + KOH ®
4. Zn(OH)2 + NaOH ®
Решение.
Реакции в растворах электролитов протекают между ионами, их записывают с помощью ионных уравнений. Большинство этих реакций относят к типу обменных, и сущность их сводится к соединению ионов в молекулы новых веществ. Обязательным условием протекания реакций обмена между электролитами в растворах является образование:
малорастворимых веществ,
слабых электролитов,
газообразных веществ,
комплексных ионов.
При составлении ионного уравнения все перечисленные выше вещества пишутся в виде молекул, а сильные электролиты - в виде ионов, независимо от того, в левой или правой частях уравнения они находятся.
Распишем реакции, приведенные в условии задачи в молекулярном и ионном виде.
Молекулярное уравнение:
1. 3AgNO3 + FeCl3 = 3AgCl¯ + Fe(NO3)3.
Полное ионное уравнение:
3Ag+ + 3NO  + Fe3+ + 3Cl- = 3AgCl¯ + 3Fe3+ + 3NO
+ Fe3+ + 3Cl- = 3AgCl¯ + 3Fe3+ + 3NO  .
.
Если из правой и левой частей уравнения исключить одинаковые ионы, то получим краткое ионное уравнение, выражающее суть данной реакции.
Краткое ионное уравнение:
3Ag+ + 3Cl- = 3AgCl¯.
Подобным образом расписываем остальные реакции.
2. Na2S + 2HCl =2NaCl + H2S.
2Na+ + S2– + 2H+ + 2Cl– =2Na+ + 2Cl– + H2S.
2H+ + S2– = H2S.
3. HCN + KOH = KCN + H2O.
HCN + K+ + OH- = K+ + CN- + H2O.
HCN + OH- = CN- + H2O.
4. Zn(OH)2¯ + 2NaOH = Na2[Zn(OH)4].
Zn(OH)2¯ + 2Na+ + 2OH- = 2Na+ + [Zn(OH)4]2-.
Zn(OH)2¯ + 2OH- = [Zn(OH)4]2-.
Пример 2.
К растворам NaCl, HNO3, CuSO4, KNO3 прибавили раствор гидроксида натрия. В каком случае произошла реакция? Напишите молекулярные и ионные уравнения этих реакций.
Решение.
Чтобы определить, произошла или нет реакция, распишем молекулярные и ионные уравнения:
1. NaCl + NaOH = NaOH + NaCl,
Na+ + Cl- + Na+ + OH- = Na+ + OH- + Na+ + Cl-.
В левой и правой частях уравнения одни и те же ионы, нет никакого изменения, реакция не идет.
2. HNO3 + NaOH = NaNO3 + H2O,
H+ + NO  + Na+ + OH- = Na+ + NO
+ Na+ + OH- = Na+ + NO  + H2O,
+ H2O,
H+ + OH- = H2O.
Реакция протекает с образованием слабого электролита - воды.
3. CuSO4 + 2NaOH = Cu(OH)2¯ + Na2SO4,
Cu2+ + SO  + 2Na+ + 2OH- = Cu(OH)2¯ + 2Na+ + SO
+ 2Na+ + 2OH- = Cu(OH)2¯ + 2Na+ + SO  .
.
Cu2+ + 2OH– = Cu(OH)2
Реакция протекает с образованием осадка гидроксида меди.
4. KNO3 +NaOH = KOH + NaNO3,
K+ + NO  + Na+ + OH- = K+ + OH- + Na+ + NO
+ Na+ + OH- = K+ + OH- + Na+ + NO  .
.
Реакция не идет, левая и правая части уравнения идентичны.
Задания
181. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) NaHCO3 и NаOH; б) K2SiО3 и НСl; в) BaCl2 и Na2SO4.
182. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) K2S и НСl; б) FеSO4 и (NH4)2S; в) Сг(ОН)3 и КОН.
183. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Mg2+ + СО  = MgCО3
= MgCО3
б) Н+ + ОН– = Н2О
184. Какое из веществ: AI(OH)3, H2SO4, Ba(OH)2 будет взаимодействовать с гидроксидом калия? Выразите эти реакции молекулярными и ионно-молекулярными уравнениями.
185. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) КНСОз и H2SO4 б) Zn(OH).2 и NaOH;
в) CaCI2 и AgNO3,.
186. Составьте молекулярные и инонно-молекулярные уравнения взаимодействия в растворах между: a) CuSO4 и H2S, BaCO3 и HNO3, в) FeCI3 и КОH.
187. Составьте во три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Сu2+ + S2– = CuS
б) SiО  + 2H+ = H2SiO3
+ 2H+ = H2SiO3
188. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия а растворах между; a) Sn(OH)2 и НС1; б) BeSO4 и КОН;
Не нашли, что искали? Воспользуйтесь поиском: