
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Лабораторные работы.
Работа 1. Зависимость скорости реакции от концентрации реагирующих веществ.
Реакция между серной кислотой и тиосульфатом натрия сопровождается выделением серы и раствор мутнеет:
Na2S2O3 + H2SO4 = Na2SO4 + S¯ + SO2 + H2O
Данная реакция состоит из следующих стадий:
Na2S2O3 + H2SO4 = Na2SO4 + H2S2O3 (I) (очень быстро)
H2S2O3 = H2SO3 + S¯ (2) (медленно)
H2SO3 = SO2 + H2O (3) (быстро)
Скорость суммарного процесса определяется медленной стадией - разложением тиосерной кислоты (2): u = k.C(H2S2O3)
Время от начала реакции до момента появления мути зависит от скорости этой реакции. Чем меньше концентрация Na2S2O3, тем больше будет этот промежуток времени (меньше скорость реакции). За скорость можно условно принять величину, обратную времени протекания реакции: u (усл.) = 1/t.
Выполнение эксперимента:
В три пробирки налейте по 3 мл раствора серной кислоты. В три другие налейте: в первую – 9 мл раствора Na2S2O3, во вторую – 6 мл раствора и 3 мл воды, а в третью – 3 мл раствора Na2S2O3 и 6 мл воды. Затем к каждому из подготовленных растворов прилейте по 3 мл раствора серной кислоты, встряхните и отметьте, через сколько секунд после приливания кислоты появится муть. Результаты запишите в журнал по следующей форме:
| № про-бир-ки | V(p-pa H2SO4)мл | V(p-pa Na2S2O3)мл | V(H2O) мл | Объём смеси, мл | Время появ-ления мути,с |
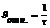 с-1
с-1
| Относит. С(Na2S2O3) |
| t1 = | 3C | ||||||
| t2 = | 2C | ||||||
| t3 = | 1C |
Обработка результатов эксперимента
Выразите относительную скорость в виде десятичной дроби, а результаты эксперимента представьте в виде графика зависимости скорости реакции от концентрации. Для этого по горизонтальной оси отметьте три точки, отстоящие от начала координат на 1 с, 2 с и 3 с, где с - произвольно выбранный отрезок, соответствующий единице относительной концентрации. Из каждой точки восстановите перпендикуляр, длина которого пропорциональна величине относительной скорости реакции. Линия, соединяющая верхние концы перпендикуляров, будет выражать собой графическую зависимость скорости реакции от концентрации. Сформулируйте вывод, характеризующий результат эксперимента.
Работа 2. Зависимость скорости реакции от температуры.
Выполнение эксперимента.
Налейте в три пробирки по 6 мл раствора Na2S2O3, а в другие три - по 6 мл раствора H2SO4 и разделите их на три пары по пробирке с растворами тиосульфата и серной кислоты в каждой паре. Растворы первой пары пробирок слейте при комнатной температуре (лучше раствор Na2S2O3 к раствору H2SO4), одновременно включите секундомер и отметьте время появления мути. Растворы второй пары нагрейте на 100С, а третьей пары - на 200С выше комнатной температуры. Для этого поместите соответствующую пару пробирок в химический стакан с водой и нагрейте последний до требуемой температуры. За температурой следите по термометру, опущенному в воду. Сливайте по-парно содержимое пробирок и отмечайте, через сколько секунд появится муть. Результаты запишите в журнал по форме:
| № пробирок | V(р-ра H2SO4), мл | V (р-ра Na2S2O3), мл | t0 С | Время появления мути, с | uотн = 1/t, с-1 |
| ком. t0C | t1= | ||||
| +100 | t2= | ||||
| +200 | t3= |
Обработка результатов эксперимента.
Результаты выразите в виде графика, аналогично работе №1. По горизонтальной оси отметьте три точки, соответствующие трём значениям температур (t0ком., +100, +200). Сделайте вывод о том, как зависит скорость изучаемой реакции от температуры.
Работа 3. Зависимость скорости реакции от концентрации катализатора.
Ионы Сu2+ повышают скорость разложения тиосерной кислоты.
Выполнение эксперимента.
В три пробирки налейте из бюретки по 1 мл раствора Na2S2O3, затем в одну из них прибавьте 1 мл раствора катализатора (раствор СuSO4) и 3 мл воды; во вторую - 2 мл раствора катализатора и 2 мл воды; в третью - 3 мл раствора катализатора и 1 мл воды. Таким образом, во всех трех пробирках будет по 5 мл раствора с одинаковой концентрацией Na2S2O3, но с разной концентрацией СuSO4.
Рассчитайте концентрацию Na2S2O3 и ионов Сu2+ в приготовленных растворах.
В три другие пробирки налейте по 5 мл раствора H2SO4. Затем попарно смешайте приготовленные растворы Na2S2O3 и H2SO4. По секундомеру отметьте время от момента смешивания до помутнения раствора. Полученные результаты запишите в журнал по форме:
| № пробирок | Концентрация ионов Сu2+, моль/л | Время появления мути, с | uотн = 1/t, с–1 |
Обработка результатов эксперимента.
Рассчитайте условную скорость реакции при различных концентрациях Сu2+. Постройте график зависимости скорости реакции от концентрации катализатора. На основании полученной зависимости сделайте вывод о влиянии ионов Сu2+ на скорость разложения тиосерной кислоты.
ЗАНЯТИЕ 9
Тема: Химическое равновесие.
Химическое равновесие устанавливается в системах, в которых протекают обратимые химические реакции. Количественно оно характеризуется константой равновесия (K).
Для гомогенной реакции общего вида: аА + вВ ↔ сС + dD
Kс = 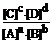 , где
, где
[A], [B], [C], [D] - равновесные молярные концентрации веществ A, B, C и D.
Для гетерогенной реакции вида:
1) A(г) + 2B(ТВ) ↔ AB2(ж) Kс = 
2) А(г) + 2В(ж) ↔ АВ2(ж) Kс = 
3) А(ж) + 2В(тв) ↔ АВ2(ж) Kс = 
Таким образом, концентрация твёрдого вещества (всегда), жидкого (в реакциях с газами) не входит в выражение константы равновесия, как и в кинетическое уравнение химической реакции.
Константа равновесия, равная отношению констант скоростей прямой (k1) и обратной (k2) реакции зависит от температуры и от природы реагирующих веществ, но не зависит от их концентрации:
K =  .
.
На состояние химического равновесия оказывают влияние концентрация реагирующих веществ, температура, а для газов - и давление. При изменении одного из этих параметров равновесие нарушается и концентрации всех реагирующих веществ изменяются до тех пор, пока не установится новое равновесие, но уже при других значениях равновесных концентраций. Такой переход называется сдвигом или смещением химического равновесия.
О направлении сдвига равновесия судят по принципу Ле Шателье, в соот-ветствии с которым увеличивается скорость той реакции (прямой или обрат-ной), которая ослабляет внешнее воздействие. Действительно, если увеличить, например, концентрацию [С], то должна уменьшиться концентрация [D], и
увеличиться концентрация [А] и [В], т.е. это приведёт к смещению равновесия в сторону исходных веществ.
Задачи с решениями.
1. При состоянии равновесия в системе N2(г) + 3H2(г) ↔2NH3(г); DН = -92,4кДж концентрации веществ равны: [N2] = 3моль/л; [H2] = 9моль/л; [NH3] = 4моль/л. Определите: а) константу равновесия реакции; б) исходные концентрации N2 и H2; в) в каком направлении сместится равновесие с ростом температуры; с уменьшением объёма реакционного сосуда?
Решение:
а) Kс = 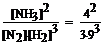 = 0,0073.
= 0,0073.
Kс << 1, т.е. равновесие смещено влево, преобладает обратная реакция.
б) исходная концентрация вещества складывается из прореагировавшей и равновесной:
C(N2) = C ¢ (N2) + [N2]
C(H2) = C ¢ (H2) + [H2]
Из уравнения реакции видно, что для образования 2 моль NH3 расходуется 1 моль N2 и 3 моль Н2. Т.к. в момент равновесия [NH3] = 4 моль/л, то С ¢ (N2) = 2 моль/л; C ¢ (H2) = 6 моль/л.
C(N2) = 3 + 2 = 5 (моль/л),
C(H2) = 9 + 6 = 15 (моль/л).
в) при увеличении температуры равновесие сместится влево, в сторону эндотермической реакции; при уменьшении объёма реакционного сосуда увеличивается давление и равновесие смещается вправо, в сторону уменьшения числа молей газовой смеси.
Ответ: Kс = 0,0073; 5 моль/л N2, 15 моль/л Н2.
2. Константа равновесия реакции FeO(K) + CO(г)  Fe(K) +CO2(г) при некоторой
Fe(K) +CO2(г) при некоторой
температуре равна 0,5. Найдите равновесные концентрации CO и CO2, если начальные концентрации составляли: C(CO2) = 0,05 моль/л; C(CO2) = 0,01 моль/л.
Решение: Kс =  = 0,5.
= 0,5.
Пусть х моль СО прореагировало, тогда по уравнению реакции из х моль СО получилось х моль СО2.
[CO] = C(CO) - C'(CO) = (0,05 - х) моль/л
[CO2] = C(CO2) - C'(CO) = (0,01 + х) моль/л
Kс =  = 0,5
= 0,5
(0,01 + х) = 0,5(0,05 - х); 0,01 + х = 0,025 - 0,5 х; 1,5 х = 0,015;
х =  = 0,01
= 0,01
[CO] = 0,05 - 0,01 = 0,04 (моль/л)
[CO2] = 0,01 + 0,01 = 0,02 (моль/л)
Ответ: [CO] = 0,04 M, [CO2] = 0,02 M.
3. При отравлениях арсенатами в крови обнаруживают 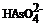 ионы, способные замещать
ионы, способные замещать  ионы в процессе метаболизма. Рассчитайте равновесную кон-центрацию
ионы в процессе метаболизма. Рассчитайте равновесную кон-центрацию  ионов в водном растворе, если [
ионов в водном растворе, если [ 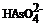 ] = 10-4 моль/л, а константа равновесия для реакции
] = 10-4 моль/л, а константа равновесия для реакции 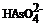 ↔ H++
↔ H++  при 250 равна 10-12.
при 250 равна 10-12.
Решение:
1) По закону действующих масс: Kс =  = 10-12.
= 10-12.
2) По уравнению реакции: 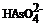 ↔ H+ +
↔ H+ + 
[  ] = [H+] и пусть равно х моль/л, тогда Kс =
] = [H+] и пусть равно х моль/л, тогда Kс =  = 10-12.
= 10-12.
x = 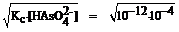 = 10-8 моль/л.
= 10-8 моль/л.
Ответ: 10-8 моль/л.
4. Чему равна массовая доля водорода и йода, превращающихся в йодоводород, если они взяты в реакцию по 1 моль каждый, а константа равновесия при температуре опыта равна 4?
Решение:
Составим таблицу: H2 + I2 ↔ 2HI
Взято, моль/л 1 1
К моменту равновесия прореагировало х х
Осталось 1- х 1- х
Образовалось 2 х
Если равновесные концентрации водорода и йода составляют 1 - х, а йодоводорода 2 х моль/л, то
Kс =  = 4, х = 0,5 (моль/л).
= 4, х = 0,5 (моль/л).
Таким образом, массовые доли Н2 и I2, превратившихся в HI, равны и составляют 50%.
Ответ: 50%.
5. Для реакции 2 CO2 ↔ 2CO + O2 при 20000С состав равновесной смеси выражается объёмными долями: 85,2% CO2, 9,9%CO и 4,9%O2, а общее давление в системе составляет 101,3 кПа. Чему равна константа равновесия этой реакции при данной температуре, выраженная через:
а) парциальные давления реагирующих веществ (Kp),
б) их молярные концентрации (Kс)?
Решение:
Парциальное давление газа равно общему давлению, умноженному на объёмную долю газа в смеси, поэтому:
а) р(CO2) = 101,3 . 0,852 = 86,3 (кПа)
б) p(CO) = 101,3 . 0,099 = 10,0 (кПа)
в) p(O2) = 101,3 . 0,049 = 4,9 (кПа)
Kp =  = 0,067.
= 0,067.
Для данной реакции Dn = 3-2= 1. Тогда Kc =  =3,6.
=3,6.
Ответ: Kp = 0,067; Kc = 3,6.
6. Какими способами в системе: 2SO2 + O2 ↔ 2SO3 - DH можно смещать равновесие в сторону большего выхода SO3 при заданной концентрации SO2?
Решение:
По принципу Ле Шателье это достигается:
а) повышением концентрации О2;
б) уменьшением концентрации SO3 (удаления из сферы реакции);
в) повышением давления;
г) понижением температуры до такого ее значения, при котором скорость реакции еще достаточна для относительно быстрого достижения равновесия.
Вопросы и задачи для самоподготовки.
1. Какие реакции называют: а) необратимыми; б) обратимыми; в) прямыми; г) обратными? Приведите соответствующие примеры.
2. Одинаковы или различны значения констант скоростей для прямой и обратной реакции? Объясните.
3. Как изменяются скорости прямой и обратной реакции? Чем обусловлено и в какое состояние приводит данную систему?
4. Что называют химическим равновесием? Почему оно является ди-намическим? Какие концентрации реагирующих веществ называют равновесными?
5. Что называют константой химического равновесия? Зависит ли эта величина от природы реагирующих веществ, их концентрации, температуры, давления?
6. Объясните, почему числовое значение константы равновесия определяет глубину превращения исходных веществ в продукты реакции.
7. Почему в выражение для константы равновесия не входят концентрации веществ, находящихся в твердой фазе?
8. Какими параметрами характеризуется химическое равновесие? Перечислите.
9. Какой процесс называют смещением (сдвигом) химического равновесия.
10.На конкретных примерах покажите, как смещается равновесие системы под влиянием изменения: а) концентрации одного из реагирующих веществ,б) температуры, в) давления.
11.Скорость какой химической реакции (экзо- или эндотермической) больше увеличивается при нагревании равновесной системы?
12. Влияет ли катализатор на положение равновесия и почему? Зависит ли константа равновесия от катализатора?
13. Для какой реакции - прямой или обратной - энергия активации больше, если прямая реакция идет с выделением теплоты?
14. Если при данной температуре константа скорости прямой реакции имеет большее значение, чем константа скорости обратной, то какая из них будет экзотермической?
15. Напишите выражение Kр для следующих реакций:
а) 2NО(г)+О2(г) ↔2 NО2(г)
б) СH3СООН(р) ↔СН3СОО- (р)+ Н+(р)
в) МgСО3(к) ↔ МgО(к)+ СО2(г)
г) [НgJ4]2- (р) ↔Нg2+(р)+ 4I- (р)
д) Н2О(ж) ↔ Н+(р)+ ОН- (р)
е) 3Fe(к)+ 4Н2О(ж) ↔ Fe3О4(к)+ 4Н2(г)
16. При 4500С константа равновесия реакции Н2 + I2↔ 2НI равна 50,0. Чему равна константа равновесия реакции диссоциации НI при той же температуре? Ответ: 0,02.
17. Найдите значение константы равновесия для гомогенной реакции А + В ↔ С + D, если исходные концентрации веществ А и В были равны по 0,8 моль/л, а равновесная концентрация вещества С равна 0,6моль/л. Ответ: 9.
18. Какое значение имеет константа равновесия Kр реакции: 2НI(г) ↔ Н2(г) + I2(г) при 4480С, если парциальные равновесные давления газов при этой температуре составляют: p (HI) = 40,5 кПа, р (H2) = 75,2кПа, р (I2) = 0,436 кПа? Ответ: 0,02.
19. В системе РСI5(г) ↔ РСI3(г) + СI2(г) равновесиe при 500 K установилось, когда исходная концентрация РСI5, равная I моль /л, уменьшилась до 0,46 моль/л. Найдите значение Kс этой реакции при указанной температуре. Ответ: 0,634.
20. Рассчитайте константу равновесия реакции: 4НСI (г)+ О2 (г) ↔ 2СI2(г) + 2Н2О(г), если начальные количества веществ были 2,4 моль НСI и 1,2 моль О2, а к моменту наступления равновесия осталось непрореагировавшим 0,8 моль хлороводорода. Объём реакционного сосуда равен 4 л. Ответ: 0,625.
21.Определите константу равновесия реакции: N2(г)+ 3Н2(г) ↔ 2NH3(г), если при некоторой температуре в реакционный сосуд, объёмом 10 л введено 0,05 моль N2 и 0,52 моль Н2, а к моменту установления равновесия образовалось 0,04 моль аммиака. Ответ: 54,8.
22. При 6500С константа равновесия системы СО2(г)+Н2(г) ↔ СО(г)+Н2О(г) равна единице. В начальный момент концентрации СО2 и Н2 были соответственно равны 0,2 и 0,8 моль/л. Вычислите равновесные концентрации всех реагирующих веществ.
Ответ: 0,04; 0,64; 0,16; 0,16 моль/л.
23. Для реакции FeO(к) + CO(г) ↔ Fe(к) + CO2(г) константа равновесия при 10000С равна 0,5. Начальные концентрации СО и СО2 были соответственно равны 0,05 и 0,01 моль /л. Найдите их равновесные концентрации. Ответ: 0,04 и 0,02 моль/л.
24. Найдите константу равновесия реакции N2O4  2NO2, если начальная концентрация N2O4 составляла 0,08 моль/л, а к моменту наступления равновесия диссоциировало 50% N2O4. Ответ: 0,16.
2NO2, если начальная концентрация N2O4 составляла 0,08 моль/л, а к моменту наступления равновесия диссоциировало 50% N2O4. Ответ: 0,16.
25. Будет ли влиять на равновесную концентрацию СО2 в системе СаСО3(к) ↔ СаО(к) + СО2(г) введение дополнительного количества: а)СО2, б) СаСО3?
Ответ: а) да; б) нет.
26. Какие условия будут способствовать большему выходу SO3 по реакции SO2 + 1/2О2 ↔ SO3; DН0298 = -98,9 кДж/моль? Какая масса SО2 израсходуется при образовании SO3 массой 10 г? Ответ: 8 г.
27. В какую сторону сместится равновесие реакции:
а) 2Н2S(г) ↔2H2(г) + S2(к) ; DН = 40,13 кДж
б) N2O4(ж) ↔2NO2(г); DН = 66,55 кДж
в) СО(г) + Н2О(г) ↔СО2(г) + Н2(г); DН = -40,96кДж
1) при повышении температуры;
2) при повышении давления?
28. В какую сторону будет смещаться равновесие при повышении температуры в системе:
а) N2 (г) + 3H2 (г) ↔ 2NH3 (г), DH0298 = -92,4 кДж
б) 2CO2 (г) ↔ 2CO(г) + O2 (г), DH0298 = 566 кДж
в) 4HCl(г) + O2(г) ↔ 2Cl2(г) + 2H2O(ж), DH0298 = -202,4 кДж
29. Укажите, какими изменениями концентрации реагирующих веществ можно сместить вправо равновесие реакции: CO2(г)+C(графит) ↔ 2CO(г).
30. В каком направлении сместится равновесие реакции A2 (г) + B2 (г) ↔ 2AB(г), если давление увеличить в 2 раза и одновременно повысить температуру на 100? Температурные коэффициенты скорости прямой и обратной реакций равны соответственно 2 и 3. Каков знак DHо этой реакции? Ответ: влево, DHо < 0.
Не нашли, что искали? Воспользуйтесь поиском: