
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Примеры выполнения задания. Пример 1.Сколько граммов 30 % (по массе) раствора NaCl надо добавить к 300 г воды, чтобы получить 10 % раствор соли?
Пример 1. Сколько граммов 30 % (по массе) раствора NaCl надо добавить к 300 г воды, чтобы получить 10 % раствор соли? (ответ: 150 г).
| Дано | Решение |
| w1(NaCl) = 30 % | Массовая доля (w) – отношение количества граммов растворенного вещества к массе раствора.
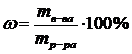
|
| w2(NaCl) = 10 % | |
| m¢(H2O) = 300 г | |
| m1(NaCl) =? |

m2(р-ра) = m1(р-ра) + m¢(H2O) = m + 300

30m = 10m + 3000
20m = 3000
m = 150.
ответ: чтобы получить 10 % раствор соли, необходимо взять 150 г 30 % раствора NaCl.
Пример 3. Вычислите молярную, нормальную и моляльную концентрации 16 %-го раствора хлорида алюминия плотностью 1,149 г/см3. Объем раствора 4 л.
| Дано | Решение |
| w(AlСl3) = 16 % | Массовая доля (w) AlСl3 – отношение количества граммов растворенного вещества к массе раствора. Поэтому расчет навески AlСl3 можно проводить по следующей формуле: |
| r(р-ра) = 1,149 г/см3 | |
| Cм (AlСl3) =? | |
| Cн (AlСl3) =? | |
| Cm(AlСl3) =? |
 , m(р-ра)= V(р-ра) ´ r(р-ра) Þ
, m(р-ра)= V(р-ра) ´ r(р-ра) Þ 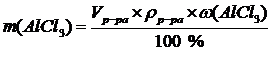
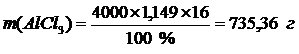 .
.
1. Молярная концентрация – число молей растворенного вещества в 1 л раствора:
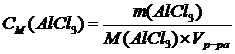
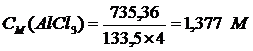 .
.
2. Нормальная концентрация – число эквивалентов растворенного вещества в 1 л раствора
m (AlCl3 )
С N = ___________________
1/3 М(AlCl3 ) х V (р-ра)
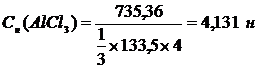
3. Моляльная концентрация – показывает, сколько молей растворенного вещества содержится в 1 килограмме растворителя.
Массу AlСl3 в 1000 г воды (растворителя) находим из соотношения:
| (100 – 16) г Н2О | – | 16 г AlСl3 |
| 1000 г Н2О | – | m г AlСl3 |
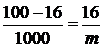 Þ
Þ 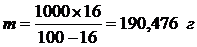 .
.
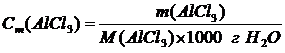 , [моль/1 кг Н2О]
, [моль/1 кг Н2О]
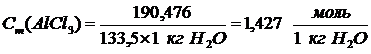 .
.
Пример 4. Раствор содержащий 0,512 г неэлектролита в 100 г бензола, кристаллизуется при 5,296 °С. Температура кристаллизации бензола 5,5 °С. Криоскопическая константа 5,1 °. Вычислите мольную массу растворенного вещества.
| Дано | Решение |
| m(X) = 0,512 г | Согласно 2 закону Рауля понижение температуры кристаллизации раствора (Dt) по сравнению с температурами кристаллизации выражаются уравнением
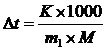 , ,
|
| m(C6H6) = 100 г | |
| t(р-р) = 5,296 °С | |
| t(C6H6) = 5,5 °С | |
| K = 5,1 ° | |
| M(X) =? |
где K – криоскопическая постоянная.
m и М – соответственно масса растворенного вещества и его мольная масса; m1–масса растворителя.
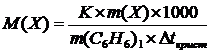
Dt = t(C6H6) – t(р-р)

Ответ: мольная масса растворенного вещества 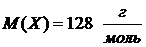 .
.
Пример 5. Рассчитайте степень гидролиза и значение рН в 0,1 М растворе ацетата натрия, 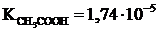 .
.
| Дано | Решение |
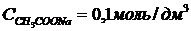
| CH3COONa + H2O Û CH3COOH + NaOH
CH3COO– + H2O Û CH3COOH + OH–
1. Константа гидролиза соли:
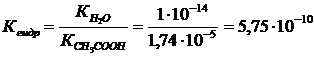 . .
|

| |
| h =? | |
| pH =? |
2. Степень гидролиза соли:
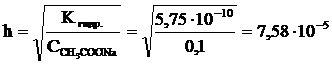 или 0,00758 %.
или 0,00758 %.
3. Молярная концентрация гидроксид-ионов:
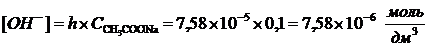
4. Водородный показатель:
pH = 14 + lg[ОН–] = 14 + lg7,58´10–6 = 8,88
Ответ: степень гидролиза h = 0,00758 %, pH = 8,88.
Пример 6. Образуется ли осадок хлорида свинца, если смешать равные объемы растворов соляной кислоты с концентрацией 0,02 моль/дм3 и нитрата свинца с молярной концентрацией 0,01 моль/дм3?
Решение
1. Pb(NO3)2 + 2HCl ® PbCl2¯ + HNO3;
2. PbCl2 (тв.) Û Pb2+ + 2Cl–;
3. ПР(PbCl2) =[Pb2+] . [Cl–]2 = 1,6 . 10–5;
4. Соль и кислота – сильные электролиты:
Pb(NO3)2 Û Pb2+ + 2NO3–;
HCl Û Н+ + Cl–;
поэтому: С0(Pb2+) = 0,01 моль/дм3; С0(Cl–) = 0,02 моль/дм3.
При сливании общий объем раствора увеличился вдвое. Следовательно, после сливания растворов концентрации ионов уменьшились вдвое и стали равны:
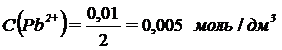 ;
;
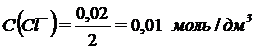 ;
;
5. Пс = С(Pb2+) . С2(Cl–) = 0,005 . (0,01)2 = 5 . 10–7;
6. 5 . 10–7 < 1,6 . 10–5; Пс < ПР
Ответ: полученный раствор является ненасыщенным, осадок не образуется.
Задание 4.
Не нашли, что искали? Воспользуйтесь поиском: