
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Метамизол натрия (анальгин)
Строение и свойства

Метамизол натрия - соль сульфоновой кислоты, по силе сравнимой с H2SO4. При определении подлинности и в количественном анализе используют реакцию окисления диоксида серы SO2, образующегося при разложении метамизола натрия.
Метамизол натрия легко растворяется в воде, поэтому удобен для парентерального введения, pH водного раствора 6,0-7,5.
Контроль качества
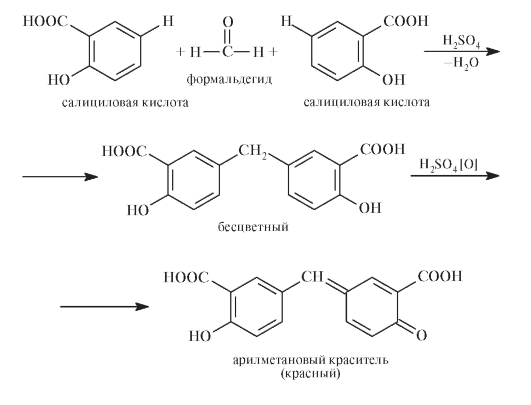
Определение подлинности. Метамизол натрия подвергается гидролитическому разложению в водном растворе во всей области водных значений рН (НД рекомендует при рН <3). Например, при кипячении метамизола натрия с хлороводородной кислотой образуется метиламинофеназон, сернистый ангидрид и формальдегид:

Последующая конденсация формальдегида с салициловой кислотой в среде H2SO4 (конц.) приводит к образованию арилметанового красителя красного цвета:
Реакции окисления метамизола натрия: при добавлении к подкисленному раствору ЛВ окислителя [соль Fe(III), калия йодат KIO3 и др.] наблюдается появление синего или фиолетового окрашивания. Например, фильтровальная бумага, пропитанная раствором KIO3 в смеси с крахмалом и помещенная над горлышком пробирки с нагретой смесью ЛВ и минеральной кислоты, окрашивается в синий цвет:
- 1-я стадия - гидролиз ЛВ;
- 2-я стадия - окисление продуктов гидролиза. Появляется синяя окраска (йод-крахмальный комплекс). При избытке реактива выделяется бурый осадок йода:
5so2 + 2 kio3 + 4h2o = 4h2so4 + i2 + k2so4
После минерализации метамизола натрия проводят характерные реакции на сульфаты. Субстанцию прокаливают в смеси натрия и калия карбонатов в течение 10 мин. Плав охлаждают, растворяют в азотной кислоте и фильтруют. Сульфат-ионы обнаруживают с помощью раствора бария хлорида (см. приложение 4).
В растворе метамизола натрия ионы натрия можно обнаружить по реакции с цинк-уранил ацетатом.
Испытания на чистоту. Раствор ЛВ, приготовленного из 2,0 г ЛВ в 40 мл воды, не должен изменять окраску при добавлении 0,1 мл фенолфталеина.
Родственные примеси обнаруживают методом ТСХ.
Сульфаты - не более 0,1%.
Тяжелые металлы - не более 20 мкг/г.
Потеря в массе при высушивании - не более 4,9-5,3%.
Количественное определение. Для определения содержания метамизола в ЛС используют его восстановительные свойства. Йодометрическое титрование проводят прямым методом до появления желтого окрашивания смеси. Для этого навеску ЛВ растворяют в спирте в сухой колбе, прибавляют 0,01 моль/л раствора HCl и титруют 0,1 моль экв/л раствором йода:
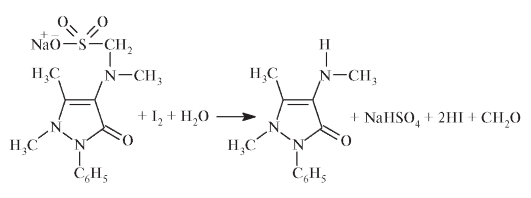
Поскольку окислительно-восстановительная реакция протекает с переносом двух электронов, молярная масса эквивалента метамизола натрия Мэ = 1/2М.
Не нашли, что искали? Воспользуйтесь поиском: