
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Равновесие ионного обмена на цеолитах
Особенности ионообменных свойств цеолитов связаны со строением их кристаллической решетки и распределением обменных катионов по различным возможным позициям в каналах или полостях разнообразных кристаллических структур.
1. Катионы, имеющие диаметр больше чем 0,22–0,25 нм, не могут проникать в малые полости цеолитов А, Х, Y и замещать находящиеся там ионы Na. Катионы малых размеров при комнатных температурах не проникают в эти полости из-за высоких энергий гидратации и больших размеров частично гидратированных катионов. Кроме того, в результате дефектов кристаллической решетки, закупорки части пор при формовании гранул часть катионов натрия оказывается блокированной и не может принимать участие в реакции ионного обмена.
2. В кислых растворах происходит разрушение кристалличнской решетки цеолитов А и Х. Более кислотостойки цеолиты Y, но и они при многоцикловом повторении ионообменных процессов в кислых растворах постепенно теряют свои ионообменные свойства. Поэтому оптимальным является использование цеолитов при рН 5–8.
Процесс ионного обмена можно представить уравнением:
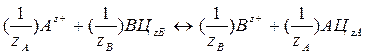 , (20)
, (20)
где  ,
,  – обмениваемые катионы, z – их заряды.
– обмениваемые катионы, z – их заряды.
Эквивалентные доли обмениваемых катионов в растворе и в цеолите определяются следующим образом:
 , (21)
, (21)
где АS – отношение числа эквивалентов обмениваемого катиона А к общему числу эквивалентов катионов в растворе; сА, сВ – концентрации ионов А и В в равновесном растворе, моль/л; (AZ + BZ) = 1 и (AS + BS) = 1; AS, AZ, BS, BZ – эквивалентные доли обмениваемых катионов в растворе и в цеолите; индексами «Z» и «S» обозначены соответственно цеолит и раствор.
Изотерма ионного обмена представляет собой кривую зависимости AZ от AS при заданной общей концентрации равновесного раствора и постоянной температуре (рис. 26). Избирательность цеолита по отношению к одному из двух ионов выражается коэффициентом разделения α, который определяется по уравнению:
 . (22)
. (22)
где  и
и  – концентрации катионов А и В в растворе и цеолите.
– концентрации катионов А и В в растворе и цеолите.
|

Если избирательность к иону А выше, α > 1. Коэффициент разделения зависит от общей концентрации раствора, температуры и величины А S.
Если α = 1, обмен является идеальным и подчиняется закону действующих масс. Однако в большинстве случаев изотерма обмена отклоняется от диагональной линии, соответствующей α = 1, что указывает на избирательность по отношению к одному из двух ионов. У большинства неорганических ионообменников изотермы начинаются в левом нижнем углу диаграммы и заканчиваются в правом верхнем углу. Изотермы обмена на цеолитах часто имеют другую форму, что обусловлено недоступностью внутрикристаллических пустот цеолитов для некоторых ионов, а также наличием катионов в тех участках структуры, где обмен произойти не может, т.е. так называемым ионно-ситовым эффектом. При этом изотерма заканчивается на диаграмме в точке, где степень обмена меньше 1.
На рис. 26 приведены 5 типов изотерм, показывающих: а) избирательность цеолита к катиону А при всех степенях обмена, изотерма проходит над диагональю; б) изменение знака избирательности катиона А при увеличении степени обмена, изотерма имеет S-образную форму; в) избирательность цеолита к катиону В при всех степенях обмена, изотерма расположена под диагональю; г) неполноту обмена (хотя цеолит вначале проявляет избирательность к катиону А), вследствие ионно-ситового эффекта полный обмен не достигается. Степень обмена х макс < 1, где х – отношение числа эквивалентов катиона В в цеолите к числу грамм-эквивалентов Al в цеолите; д) необычная форма изотермы с петлей гистерезиса наблюдается в том случае, когда обмен приводит к образованию двух фаз цеолитов.
Получение
Промышленные способы получения цеолитов можно разделить на две группы:
1. Получение цеолитов в виде кристаллических порошков высокой чистоты или в виде гранул из реакционноспособных алюмосиликатных гелей или гидрогелей.
2. Получение цеолитов в виде порошков высокой чистоты или в виде гранул, не содержащих связующего, из глинистых минералов, в частности каолина.
В основу первого промышленного способа получения цеолитов положены результаты лабораторных синтезов. Сырьем для получения натриевой формы цеолитов являются силикат натрия, гидроксид алюминия и едкий натр. Гидроксид алюминия растворяют в кипящем растворе едкого натра, разбавляют и таким образом получают рабочий раствор алюмината натрия. Силикат-глыбу разваривают острым паром, после чего раствор жидкого стекла разбавляют водой для получения требуемой концентрации.
Принципиальная схема получения гранулированных цеолитов со связующими добавками представлена на рис. 27 [1].

Рис. 27. Схема получения гранулированных цеолитов со связующими добавками [1]:
1 − смеситель; 2 – кристаллизатор; 3,11 – фильтры; 4 – бегуны; 5 – увлажнитель;
6 – гранулятор; 7 – сушилка; 8 – сито; 9 – печь; 10 − реактор
Смесь растворов силиката и алюмината натрия поступает в смеситель 1, где при интенсивном перемешивании образуется гидрогель, который направляют в кристаллизатор 2. Нагрев геля в кристаллизаторе осуществляют глухим или острым паром. В зависимости от соотношения реагентов, температуры, времени выдерживания получают цеолиты разного типа.
Образовавшийся кристаллит отделяют от маточного раствора в фильтр-прессе 3, где одновременно происходит его отмывка от избытка щелочи водой. Маточный раствор повторно используют для получения рабочих растворов. Выделение кристаллита из раствора может быть осуществлено также центрифугированием. Частицы кристаллита имеют размер от 1 до 15 мкм и за редким исключением не могут применяться как адсорбенты технологических процессов. Поэтому в качестве связующего в бегунах 4 к кристаллиту добавляется 15–20 % пластичной каолинитовой или бентонитовой глины, обладающей высокой проницаемостью.
Выходящая из бегунов паста имеет влажность около 35 %, что обеспечивает консистенцию, которая необходима для грануляции. В некоторых случаях пасту дополнительно увлажняют в аппарате 5. В таблеточной машине 6 получают гранулы определенного размера, обычно от 2 до 4 мм. Гранулы подвергают сушке при 120–150 оС в аппарате 7, ленточного или иного типа. В барабанном вращающемся сите 8 от высушенных гранул отсеивают мелочь и возвращают ее в аппарат 4. Для придания гранулам термической и механической прочности их подвергают прокалке во вращающейся печи 9 при 575−650 оС. Длительность прокалки от 6 до 24 ч. В печи гранулы движутся противотоком к дымовому газу, получаемому в результате сжигания бессернистого природного газа. Готовые цеолиты упаковывают в герметичную тару.
При получении другой ионообменной формы цеолита (например, кальциевой формы) кристаллит с фильтра 3 направляют в реактор 10, где происходит катионный обмен в среде раствора хлористого кальция. Кальциевую форму кристаллита выделяют на фильтре 11, после чего гранулируют по описанной выше схеме.
Основные отличия в технологии при получении цеолитов типов А и Х заключаются в температурном режиме стадии кристаллизации и в условиях приготовления гидрогеля.
При гранулировании в цеолит добавляют связующее, создающее вторичную пористость. В зависимости от процесса, в котором применяют цеолит, к качеству связующего предъявляются различные требования. Обычно стремятся, чтобы удельная поверхность связующего не превышала 10 м2/г. Часто в качестве связующего применяют глины. В тех случаях, когда переработке подвергаются легко полимеризующиеся продукты, связующее должно быть каталитически неактивным. Введение связующего уменьшает концентрацию частиц кристаллита в объеме адсорбента, в связи с чем уменьшается его адсорбционная способность. Обычно добавка связующего к цеолиту составляет 18–20 %. Это − каолин, бентонитовые глины.
Введение связующего уменьшает равновесную емкость цеолита, а в ряде случаев приводит и к ухудшению кинетических свойств адсорбента. Поэтому была разработана технология получения гранулированных цеолитов без связующего. В этом случае при получении цеолитов кристаллы соединяются в агломераты, что исключает необходимость применения связующего. Кристаллизацию цеолитов проводят при более высокой концентрации реагирующих компонентов. Высококонцентрированные алюмосиликатные гидрогели готовят формованием в гранулы мелкодисперсного сухого кремнезема и концентрированного раствора алюмосиликата натрия. Аморфные гранулы сушат, прокаливают и отсеивают от пыли. После этого проводят кристаллизацию во вращающихся аппаратах, через которые циркулирует горячий щелочной раствор алюмината натрия. Вращение кристаллизаторов уменьшает опасность слипания и срастания гранул. Температура при кристаллизации 95–100 оС. Затем гранулы промывают водой, сушат воздухом и упаковывают.
В качестве сырья для получения цеолитов без связующего используют и природные материалы. На рис. 28 приведена схема получения шарикового цеолита NaA без связующего на основе природного сырья – каолина. Цеолиты без связующего характеризуются высокой механической прочностью.
Введение в состав исходных гранул не менее 30 мас. % высокодисперсного цеолита А или Х позволяет получить при последующей

Рис. 28. Схема получения цеолита NaA из каолина [1]:
1 – вращающаяся печь; 2 – шаровая мельница; 3 – топка; 4 – формовочная машина;
5 – сушилка; 6 – кристаллизатор; 7 – емкость для щелочного раствора; 8 – насос
кристаллизации продукт со степенью кристалличности, близкой к 100 % [32]. Технологии реализованы на ООО «Ишимбайский специализированный химический завод катализаторов», ОАО «Салаватнефтеоргсинтез» и ОАО «Реал Сорб».
Применение
Появление на рынке адсорбентов гранулированных цеолитов вызвало к жизни ряд новых процессов. К таким процессам относятся прежде всего циклические адсорбционные процессы очистки и разделения газовых смесей, регенерация сорбента в которых происходит за счет снижения общего давления. В англоязычной научной литературе они получили название PSA, от английского «Pressure Swing Adsorption» [1]. Их разновидностью являются процессы с вакуумной регенерацией или VSA (Vacuum Swing Adsorption). В отечественной литературе такие процессы носят название короткоцикловая безнагревная адсорбция (КБА). Процессы, в которых регенерация адсорбента осуществляется за счет повышения температуры, называются процессами TSA «Thermal Swing Adsorption».
На 90 % рынок адсорбентов обеспечивают три типа цеолитов, характеристики которых приведены в табл. 6.
Цеолиты типа А чаще всего используются для разделения относительно малых молекул по ситовому признаку. Цеолиты Х и Y имеют размер входного окна 0,74 нм и самый большой свободный объем. Эти цеолиты используются для адсорбции относительно больших молекул. Третий широко используемый промышленностью цеолит – типа ZSM-5. Часто в аналогичных процессах используется его чисто силикатный аналог – силикалит, обладающий той же самой каркасной структурой.
Перечень основных процессов очистки и разделения газовых и жидких сред, в которых используются цеолиты, приведен в табл. 8 и 9.
Цеолиты с высоким содержанием алюминия и, следовательно, высокой катионной плотностью чрезвычайно активны по отношению к воде. Их равновесная емкость по воде составляет ~ 25 г/100 г. Цеолиты обладают рядом преимуществ перед другими осушителями: высокой поглотительной способностью в области малых парциальных давлений паров воды, и возможностью осушки при высоких температурах [1]. При 200 оС адсорбционная способность цеолитов по воде еще значительна, тогда как у силикагелей и оксида алюминия она практически равна нулю. Использование цеолитов позволяет в ряде случаев (например, при осушке природного газа на промыслах и газоперерабатывающих заводах) избежать стадии охлаждения осушаемого газа, что приводит к значительному сокращению энергозатрат и упрощению схемы. В качестве осушителя чаще всего используется цеолит NaA как самый дешевый из синтетических цеолитов.
При осушке природного газа цеолитами NaA высшие углеводороды, присутствующие в газе, не проникают через входные окна этих цеолитов, в то же время при использовании для этих целей цеолитов NaX отмечалось некоторое уменьшение поглотительной способности по парам воды вследствие предадсорбции высокомолекулярных соединений.
Ввиду чрезвычайной гидрофильности цеолитов для регенерации этих адсорбентов необходимо использовать высокие температуры. Учитывая относительную трудность регенерации цеолитов, основную осушку газов со значительным содержанием водяных паров иногда целесообразно проводить более дешевым и легче регенерируемым жидким или твердым сорбентом, а глубокую доосушку – цеолитами.
Таблица 8
Процессы очистки с использованием цеолитовых адсорбентов [1,27,29]
| Процесс | Очищаемый поток | Г/Ж | Адсорбент | Примечания |
| Осушка | Природный газ | Газ | NaA | Процесс с термической регенерацией адсорбента (TSA) |
| Воздух | Газ | NaA | Процессы с термической и безнагревной регенерацией адсорбента (TSA и PSA) | |
| Фреоны | Г/Ж | KA | Нерегенеративный процесс или процесс TSA | |
| Газ крекинга | Газ | КА | TSA | |
| Органические растворители | Жидкость | КА | TSA | |
| Кислые газы | Газ | Шабазит | TSA | |
| Удаление СО2 | Воздух субмарин или космических кораблей | Газ | NaA | VSA |
| Удаление Н2S | Коксовый газ | Газ | СаА или Са-шабазит | TSA |
| Удаление SОx, NОx | Воздух | Газ | Силикалит | TSA |
| Удаление Kr85 | Воздух | Газ | Силикалит или деалю-минированный НМ | Хроматографический метод |
| Удаление I129 | Воздух | Газ | AgX, AgМ | TSA |
| Концентри-рование спиртов | Водные растворы | Жидкость | КА, NaA | TSA |
Таблица 9
Не нашли, что искали? Воспользуйтесь поиском:

 AZ + BS.
AZ + BS.