
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Протолитическая теория кислот и оснований
Протолиз – процесс передачи протона.
Протолиты – кислоты и основания, отдающие и принимающие протоны.
Кислота – молекула или ион, способные отдавать протон. Каждой кислоте соответствует сопряженное с нею основание. Сила кислот характеризуется константой кислоты Кк.
Н2CO3 + Н2O ↔ Н3O+ + HCO3¯
Кк = 4 × 10-7
[Al(Н2O)6]3+ + Н2O ↔ [Al(Н2O)5OH]2+ + Н3O+
Кк = 9 × 10-6
Основание – молекула или ион, способные принимать протон. Каждому основанию соответствует сопряженная с ним кислота. Сила оснований характеризуется константой основания К0.
NH3 × Н2O (Н2O) ↔ NH4+ + OH¯
К0= 1,8 ×10-5
Амфолиты – протолиты, способные к отдаче и к присоединению протона.
HCO3¯ + H2O ↔ Н3O+ + CO32-
HCO3¯ – кислота.
HCO3¯ + H2O ↔ Н2CO3 + OH¯
HCO3¯ – основание.
Для воды: Н2O+ Н2O ↔ Н3O+ + OH¯
K(H2O) = [Н3O+][OH¯] = 10-14 и рН = – lg[H3O+].
Константы Кк и К0 для сопряженных кислот и оснований связаны между собой.
НА + Н2O ↔ Н3O+ + А¯,
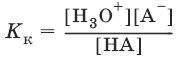
А¯ + Н2O ↔ НА + OH¯,

Отсюда
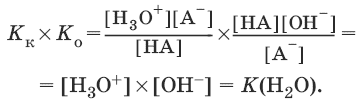
Не нашли, что искали? Воспользуйтесь поиском: