
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Свойства углерода и его соединений
Характерные степени окисления углерода, электронные формулы соответствующих ионов, химические свойства и примеры соединений приведены в таблице.
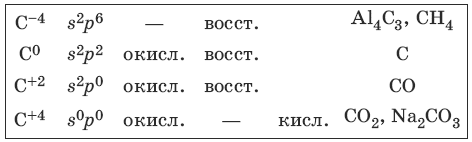
Свойства углерода
2С + O2(недостаток) → t → 2CO
С + O2(избыток) → t → CO2
С + CO2 → t → 2CO
С + CuO → t → Cu + CO
4С + Fe3O4 → t → 3Fe + 4CO
ЗС + СаО → t → СаС2 + CO
2С + Са → t → СаС2
ЗС + 4Al → t → Al4С3
С + 4НNO3(конц.) → t → CO2 + 4NO2 + 2Н2O
Свойства оксида углерода (II) – угарного газа
2CO + O2 → t → 2CO2
ЗCO + Fe2O3 → t → 2Fe + ЗCO2
CO + CuO → t → Cu + CO2
CO + H2O → t, катализатор → CO2 + Н2
CO + NaOH → t, p → HCOONa
Свойства оксида углерода(IV) – углекислого газа
CaCO3 + 2HCl = CaCl2 + Н2O + CO2↑
CaCO3 → t → СаО + CO2
CO2 + Н2O ↔ Н2CO3 ↔ H+ + HCO3¯ ↔ 2Н+ + CO32-
CO2 + Са(OH)2 = CaCO3↓ + Н2O
CO2 + Н2O + CaCO3↓ = Са(HCO3)2
CO2 + 2Mg → t → С + 2MgO
Свойства карбонатов и гидрокарбонатов
NaOH + CO2 = NaHCO3
2NaOH + CO2 = Na2CO3 + H2O
Са(HCO3)2 → 100 °C → CaCO3↓ + Н2O + CO2↑
CaCO3 → 1000 °C → СаО + CO2
2NaHCO3 → t → Na2CO3+ Н2O + CO2↑
NaHCO3+ CH3COOH = CH3COONa + Н2O + CO2↑
CaCO3 + Н2O + CO2 = Са(HCO3)2
Са(HCO3)2 + Са(OH)2 = CaCO3↓ + 2Н2O
Na2CO3 + H2O ↔ NaHCO3 + NaOH
NaHCO3 + (Н2O) ↔ NaOH + (Н2O) + CO2
Свойства карбидов
СаС2 + 2Н2O = Са(OH)2 + С2Н2
Al4С3 + 12HCl = 4AlCl3 + ЗCH4
Не нашли, что искали? Воспользуйтесь поиском: