
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Основные положения теории окислительно-восстановительных
Реакций.
1. Окисление – процесс отдачи электронов атомом, молекулой или ионом:
Атом Zn – 2 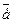 = Zn2+
= Zn2+
Молекула Н2 – 2 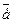 = 2Н+
= 2Н+
Ион 2Cl- -2 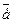 = Cl2.
= Cl2.
2. Восстановление – процесс присоединения электронов атомом, молекулой или ионом:
Атом S + 2 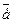 = S2-
= S2-
Молекула O2 + 4 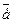 = 2O2-
= 2O2-
Ион Fe3+ + 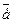 = Fe2+.
= Fe2+.
3. Окислители – это вещества, в состав которых входят атомы, присоединяющие электроны. В реакции они восстанавливаются, при этом степень окисления понижается:
Э + n 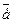 = Эn-.
= Эn-.
4. Восстановители – это вещества, в состав которых входят атомы, отдающие электроны. В реакции они окисляются, при этом степень окисления повышается:
Э – n 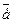 = Эn+.
= Эn+.
5. Окислительно-восстановительная реакция – сопряженный процесс: окисление всегда сопровождается восстановлением и, наоборот.
6. Баланс электронов: в окислительно-восстановительной реакции число электронов, отдаваемых восстановителем, равно числу электронов, присоединяемых окислителем.
Не нашли, что искали? Воспользуйтесь поиском: