
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Восстановители и окислители
Восстановителями и окислителями, как следует из теории ОВР (п.п.3 и 4), могут быть как простые вещества, так и сложные.
Атомы большинства металлов на внешнем энергетическом уровне имеют 1-2 электрона. Поэтому в химических реакциях они их легко отдают, т.е. окисляются, проявляя свойства восстановителя. Наилучшими восстановителями являются щелочные металлы.
В отличие от простых веществ металлов простые вещества неметаллы проявляют свойства как окислителей, так и восстановителей. Исключение составляет только фтор, который, обладая наибольшей электроотрицательностью, проявляет только свойства окислителя. Среди всех неметаллов лучшими окислителями являются галогены и кислород.
Окислительно-восстановительные свойства сложного вещества зависят от степени окисления центрального атома (атома, изменяющего свою степень окисления в результате ОВР).
Важнейшие окислители и восстановители приведены в табл. 9.1.
Таблица 9.1.
Важнейшие восстановители и окислители
Восстановители
Э – n 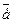 = Эn+ = Эn+
| Окислители
Э + n 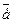 = Эn- = Эn-
|
| 1. Атомы металлов. 2. Анионы неметаллов в минимальной степени окисления S2-, Cl-…(до свободных элементов). 3. Катионы металлов в низких степенях окисления Fe2+, Mn2+, Cu+… 4. H2, CO | 1. Атомы неметаллов (элементы главной подгруппы VI-VII групп) 2. Катионы металлов в высоких степенях окисления Fe3+, Cu2+… 3. Ионы, молекулы, содержащие атомы элементов в высоких степенях окисления HNO3 (N+5), KClO3 (Cl+5) KMnO4 (Mn+7), K2Cr2O7 (Cr+6) |
Не нашли, что искали? Воспользуйтесь поиском: