
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Факторы, влияющие на протекание окислительно-восстановительных реакций
Характер протекания окислительно-восстановительных реакций зависит от химической природы взаимодействующих веществ и от условий проведения реакций:
- концентрации реагента:
0 +1 +2 0 +1
Zn + H2SO4(разб) = ZnSO4 + H2↑ окислитель Н
0 +6 +2 0 +6
Zn + 2H2SO4(конц) = ZnSO4 + S + 2H2O окислитель S;
- температуры реакции:
на холоде Fe + H2SO4(конц) → реакция не идёт
0 +6 +3 +4
при кипячении 2Fe + 6H2SO4(конц) = Fe2(SO4)3 + 3SO2↑ + 6H2O;
- наличия катализатора:
-3 0 0 -2
без катализатора 4NH3 + 3O2 = 2N2 + 6H2O
-3 0 +2 -2
с катализатором 4NH3 + 5O2 = 4NО + 6H2O;
- влияния характера среды:
в реакциях, протекающих в водных растворах, часто принимают участие молекулы воды или ионы Н+ и ОН-, которые не только способствуют передаче электронов от восстановителя к окислителю, но и связывают компоненты данных превращений.
Кислая среда максимально усиливает окислительные свойства окислителя. Для её создания чаще всего используется H2SO4(разб):
+7 +4 +2 +6
2KMnO4 + 5Na2SO3 + 3H2SO4 = 2MnSO4 + 5Na2SO4 + K2SO4 +3H2О
+7 +2
 Mn + 5
Mn + 5 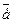 = Mn 2
= Mn 2
+4 +6
S – 2 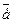 = S 5
= S 5
В нейтральной среде:
+7 +4 +4 +6
2KMnO4 + 3Na2SO3 + H2O = 2MnO2 + 3Na2SO4 + 2КОН
+7 +4
 Mn + 3
Mn + 3 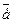 = Mn 2
= Mn 2
+4 +6
S – 2 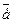 = S 3
= S 3
Щелочная среда (для ее создания используются растворы KOH или NaOH):
+7 +4 +6 +6
2KMnO4 + Na2SO3 + 2КОН = 2К2MnO4 + Na2SO4 +H2О
+7 +6
 Mn + 1
Mn + 1 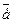 = Mn 2
= Mn 2
+4 +6
S – 2 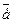 = S 1
= S 1
Не нашли, что искали? Воспользуйтесь поиском: