
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Лабораторна робота № 8 Приготування титрованого розчину йоду за точною наважкою хімічно чистого препарату.
Кристалічний йод містить домішки хлору і брому, а також гігроскопічну воду. Очищають його за допомогою сублімації. Одержаний таким способом йод використовують, як вихідну речовину. Кристали йоду розтирають з йодидом калію та оксидом кальцію. Оксид кальцію поглинає воду, а йодид калію зв'язує хлор і бром у сполуки:
Cl2+2KI  2KCl+I2 ICl+KI
2KCl+I2 ICl+KI  KCl+I2
KCl+I2
Br2+2KI  2KBr+I2 IBr+KI
2KBr+I2 IBr+KI  KBr+I2
KBr+I2
Суміш йоду, KI і CaO вміщують у стакан, який накривають годинниковим склом або у круглодонну колбу, наповнену водою. Нагрівають суміш у стакані, при цьому йод сублімується, а потім конденсується на поверхні годинникового скла (круглодонній колбі). Чистий йод знімають із холодної поверхні скляною паличкою і переносять у скляний бокс, який зберігають у ексикаторі над хлоридом кальцію.
Щоб приготувати 500,0 см3 0,05 М розчину I2 (для лабораторних робіт використовують саме такий розчин) необхідно взяти наважку:
m(I2)= 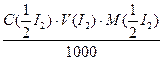
або m(I2)= 
Йод є речовиною леткою, його пари отруйні, крім того, пари йоду визивають корозію металевих деталей приладів. Всі операції з йодом слід виконувати під тягою.
Йод малорозчинний у воді, тому його розчиняють в концентрованому розчині КІ, з яким він утворює розчинний комплексний іон червоно-бурого кольору [I3]-.
Щоб розчинення I2 відбулося досить легко і швидко, необхідно брати не менш ніж трикратну кількість КІ в порівнянні з масою йоду. Крім того при зважуванні необхідно враховувати леткість йоду. Тому краще зважувати йод, попередньо розчинивши його, оскільки йод в розчині КІ менш леткий.
При цьому поступають наступним чином. Зважують в бюксі ~10г КІ на технічних терезах і розчиняють в 10-15 мл дистильованої води. Після того як розчин в бюксі буде кімнатної температури (при розчиненні КІ відбувається поглинання тепла), закривають бюкс кришкою і точно зважують бюкс на аналітичних терезах. Після цього у витяжній шафі пересипають в бюкс з розчином КІ зважену на технічних терезах масу І2 - 3,1г, закривають бюкс кришкою і точно зважують бюкс на аналітичних терезах. Різниця між результатами обох зважувань дає точну величину наважки чистого йоду. Обережним перемішуванням розчину в закритий бюкс додають воду до повного розчинення кристаликів йоду, після чого переливають розчин через лійку у вимірювальну колбу місткістю 500мл. Ретельно ополіскують бюкс дистильованою водою, промивні води переносять теж у вимірювальну колбу, доводять водою об’єм розчину в колбі до риски, перемішують концентрацію розчину йоду  обчислюють за формулою:
обчислюють за формулою:
 C(
C( I2)=
I2)= 
де m(I2)- маса наважки I2; М 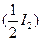 - молярна маса еквівалента I2; V(I2)- об’єм розчину, який приготували.
- молярна маса еквівалента I2; V(I2)- об’єм розчину, який приготували.
Якщо титрований розчин йоду готують з неочищеного препарату, то спочатку готують розчин приблизної концентрації, а потім визначають точну концентрацію титруванням якою-небудь вихідною речовиною або титрованим розчином натрію тіосульфату.
Не нашли, что искали? Воспользуйтесь поиском: