
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Химические свойства
| І. Кислотные свойства карбоновых кислот: | |
| 1.1. Диссоциация: | СН3СООН ↔ СН3СОО- + Н+ |
| 1.2. Образование солей: | |
| ý взаимодействие со щелочами: | СН3СООН + NaOH → СН3СООNa + H2О |
| ý взаимодействие с оксидами щелочных и щелочноземельных металлов: | 2 СН3СООН + СаO → (СН3СОО)2Са + H2О |
| ý взаимодействие с активными металлами: | 2 СН3СООН + Са → (СН3СОО)2Са + H2↑ |
| ý взаимодействие с аммиаком: | СН3СООН + NН3 → СН3СООNН4 |
| ý взаимодействие с солями: | СН3СООН + NaHCO3 → СН3СООNa + H2О + CO2↑ |
| 2. Реакции замещения гидроксила карбоксильной группы: | ||
| Ä Образование сложных эфиров (реакция этерификации): | 
| |
| С глицерином ВМЖК образуют жиры: | 
| |
| Ä Взаимодействие с пентахлоридом фосфора РСІ5 (образование галогенангидридов) | 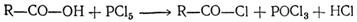
| |
| Ä Образование амидов при действии аминов или аммиака: | 
| |

| ||
| Ä Образование ангидридов (реакция дегидратации) при действии водоотнимающих средств Р2О5: | СН3СООН + СН3СООН → СН3СО – О – СОСН3 + Н2О ангидрид уксусной кислоты | |
| 3. Реакции замещения атома водорода в α-положении: | ||
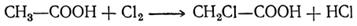
| ||
4. Реакции окисления:
þ Карбоновые кислоты устойчивы к действию окислителей. Исключение – муравьиная кислота, которая окисляется аммиачным раствором Аg2О при нагревании:
НСООН + Аg2О → 2 Аg↓ + СО2↑ + Н2О
þ β-окисление карбоновых кислот. Происходит в клетках живых организмов. При этом под действием соответствующих ферментов постепенно сокращается углеродный скелет радикала на два атома углерода, начиная от карбоксильного конца. Двууглеродный фрагмент образует с КоА ацетил-КоА, который в цикле трикарбоновых кислот (цикл Кребса) превращаясь в АТФ и её структурные аналоги, является источником химической энергии. Пример: окисление масляной кислоты, составной части молочного жира:
 СН3 – СН2 – СН2 – СООН → СН3 – СН = СН – СООН → СН3 – СНОН – СН2 – СООН
СН3 – СН2 – СН2 – СООН → СН3 – СН = СН – СООН → СН3 – СНОН – СН2 – СООН
масляная кислота кротоновая кислота β-гидроксимасляная кислота
СН3 – СО – СН2 – СООН → СН3 – СООН + СН3 – СООН
ацетоуксусная кислота уксусная кислота
| 5. Восстановление и каталитическое гидрирование кислот (происходит трудно) | |
| С2Н5 – СОН + Н2 → С2Н5 – СН2ОН Пропаналь 1-пропанол | С2Н5СООН + Н2 → С2Н5 – СОН Пропановая кислота 1-пропанол |
5. Реакция декарбоксилирования – реакция отщепления группы СО2 от карбоксила карбоновых кислот и их производных (аминокислот, кетокислот, гидроксикислот). Различают термическое и ферментативное декарбоксилирование. При термическом декарбоксилировании соли карбоновых кислот сплавляют со щелочами:
СН3СООNa + NaOH → CH4 + Na2CO3
Ферментативное декарбоксилирование – важный биохимический процесс превращений карбоновых кислот в клетках живых организмов.

Методы получения карбоновых кислот:
| ð Окисление первичных спиртов: | 
|
| ð Окисление альдегидов: | R – COH + [O] → R – COOH |
ð Окисление ненасыщенных углеводородов:
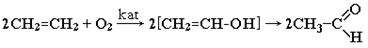

Не нашли, что искали? Воспользуйтесь поиском: