
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Загальна характеристика 5 страница
| o | а) Цис |
| o | б) Ала, Вал |
| o | в) Тре, сер |
| o | г) Три |
31. Назвіть послідовність амінокислот у тетрапептиді: фенілаланіл - серіл - метіоніл - треонін:
| o | а) фенілаланін, серін, метіонін, треонін |
| o | б) серін, фенілаланін, метіонін, треонін |
| o | в) треонін, метіонін, серін, фенілаланін |
| o | г) треонін, метіонін, серін, фенілаланін |
32. Оксіамінокислоти:
| o | а) Гли, Цис, Мет, Глу |
| o | б) Ліз, Арг, Гіс |
| o | в) Вал, Лей, Фен, Три |
| o | г) Сер, Тре, Тир |
33. Формула тірозину:
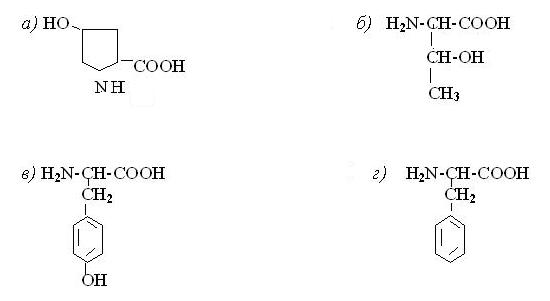
34. Формула метіонина:
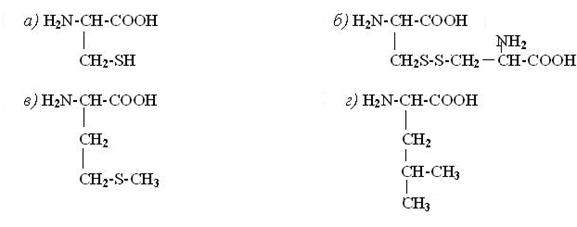
35. Формула фенілаланіну:

80. Полярні позитивно заряджені амінокислоти:
| o | а) Вал, Лей, Ізолей, Мет, Фен, Три, Про, Ала |
| o | б) Гли, Сер, Цис, Асп, Тре, Глу, Тир |
| o | в) Асп, Глу |
| o | г) Ліз, Арг, Гіс |
81. Формула аспаргінової кислоти:

85. Циклічні амінокислоти:
| o | а) Асп, Глу |
| o | б) Гли, Сер, Цис, Тре, Глу |
| o | в) Вал, Лей, Ізолей, Мет, Ала |
| o | г) Тир, Три, Фен, Гіс, Про |
86. Формула цістеїну:

36. Якими методами можна розділити суміш АК?
| o | а) хроматографією |
| o | б) ліофілізацією |
| o | в) фракційним висолюванням |
| o | г) діалізом |
37. Що таке ізоелектрична точка білків?
| o | а) стан білків, у якому їх молекула стає негативно зарядженою |
| o | б) значення рН середовища, за якого білок стає найбільш іонізованим |
| o | в) значення рН, за якого заряд білка наближається до ноля, білок не переміщується в електричному полі, легко денатурується |
| o | г) значення рН середовища, за якого білок має розчинність |
38. Що таке ефект Тіндаля?
| o | а) поява променів під час проходження світла через справжній розчин |
| o | б) поява конусу світла під час пропускання пучка світла через колоїдний розчин білків |
| o | в) випадання білків у осад в ізоелектричній точці |
| o | г) перехід білка із гідрофільного в гідрофобний стан |
39. Що таке гідроліз білків?
| o | а) розщеплення білків на АК або пептиди за участю води під дією ряду факторів |
| o | б) ферментативний розпад білків на АК |
| o | в) кислотне розщеплення білків на складові частини |
| o | г) розпад білкових структур шляхом кип’ятіння у лужному середовищі |
40. Які білки належать до складних?
| o | а) фосфопротеіни, металпротеіни, глікопротеіни, ліпопротеіни, ферменти, нуклеопротеіни тощо |
| o | б) альбуміни, глобуліни, протаміни, ліпопротеіни |
| o | в) фосфатиди, хромопротеіни, альбуміни, колаген, протеіноіди |
| o | г) металопротеіни, хромопротеіни, глобуліни, актоміозин |
41. За яких умов розчиняються альбуміни?
| o | а) у напівнасичених розчинах сульфату амонію |
| o | б) у спиртах, ацетоні, ефірі |
| o | в) у дистильованій воді, слабокислих розчинах |
| o | г) в азотній і трихлороцтовій кислотах |
42. Які сполуки входять до складу фосфопротеінів?
| o | а) АК, пентози і Фк |
| o | б) Білки і Фк |
| o | в) АК, пуринові та піримідинові основи, Фк |
| o | г) АК, фосфоліпіди і Фк |
43. Які білки є представниками фосфопротеїнів?
| o | а) фосфатиди, цереброзиди, глюкозофосфат |
| o | б) білки ЦНС і м’язів |
| o | в) казеїноген, вітелін, овальбумін, іхтулін |
| o | г) казеіноген, вітелін, кератин, іхтулін, колаген, еластин |
44. Із яких компонентів складаються хромопротеіни?
| o | а) із простого білка і зв’язаного з ним забарвленого небілкового компонента |
| o | б) із простого білка і мікро- та мікроелементів |
| o | в) із альбумінів, глобулінів, заліза |
| o | г) із гістонів, протамінів і металів |
45. Які білки є хромопротеінами?
| o | а) каталаза, цитохроми, проламіни, протаміни |
| o | б) глютеліни, альбуміни, глобуліни, казеіноген |
| o | в) міоглобін, гемоглобін, гемосидерін, цитохроми, каталаза |
| o | г) овальбумін, лактоальбумін, гістони, гемоглобін, міоглобін |
46. Які білки є складними?
| o | а) трикомпонентні білки |
| o | б) двокомпонентні білки, які складаються із простого білка і небілкового компонента (простетичної групи) |
| o | в) білки, що містять два і більше пептидних ланцюгів |
| o | г) білки, що мають крім первинної, вторинної і третинної структур ще четвертинну |
47. Які сполуки відносяться до простих білків?
| o | а) глютеліни, фосфопротеїни, глобуліни, альбуміни, протеноїди |
| o | б) протаміни, гістони, альбуміни, глобуліни, проламіни, глютеліни, протеноїди |
| o | в) альбуміни, глобуліни, нуклеопротеіни, глюкопротеіни |
| o | г) гістони, протаміни, цереброзиди, гангліозиди |
48. Яка основна роль міоглобіну в м’язах?
| o | а) транспорт оксигену і вуглекислого газу |
| o | б) накопичення оксигену та забарвлення м’язів у червоний колір |
| o | в) безпосередня участь у синтезі АТФ |
| o | г) забезпечення передачі оксигену з гемоглобіну крові в тканини утворення запасів оксигену, забезпечення механізмів дихання м’язів |
49. Які рідини чи тканини організму містять мукоїди?
| o | а) кров |
| o | б) синовальна рідина суглобів, хрящі та рогівка ока |
| o | в) спинномозкова рідина (ліквор) |
| o | г) сполучна тканина шкіри, підшкірна клітковина і внутрішні органи |
50. Що таке ліпопротеіни?
| o | а) комплекс білка з ЖК |
| o | б) комплекс білка з ліпідами |
| o | в) складний білок, побудований із простих білків, пентоз, холестерину. |
| o | г) комплекс білка з фосфатидами |
51. Які рідини чи тканини організму містять муцини?
| o | а) сполучна тканина |
| o | б) шкіра |
| o | в) різні слизи |
| o | г) рогівка ока |
52. Які білки належать до металопротеінів?
| o | а) біополімери, що містять іони будь-якого металу |
| o | б) складні білки, до складу яких входить залізо, мідь або інші метали |
| o | в) комплекси білків з одно- або двовалентними металами |
| o | г) сполуки білків з мікроелементами |
53. Який метал входить до складу феритину?
| o | а) мідь |
| o | б) залізо |
| o | в) цинк |
| o | г) кадмій |
54. Що таке глікопротеіни?
| o | а) складні білки, простетична група яких є вуглеводним похідним |
| o | б) сполуки, що складаються із простих білків і ліпідів |
| o | в) складні білки, що містять білки і полісахариди |
| o | г) складні білки, що містять білкову частину і аміносахариди |
55. Функції білків в організмі:
| o | а) пластична |
| o | б) енергетична |
| o | в) захисна |
| o | г) всі перелічені функції |
56. Хромопротеїди (гемоглобін, міоглобін) містять:
| o | а) простий білок і гем |
| o | б) простий білок і ліпіди |
| o | в) простий білок і вуглевод |
| o | г) простий білок і нуклеїнові кислоти |
57. Фактори, що викликають незворотні зміни білків:
| o | а) температура вища за 65°С |
| o | б) низка температура (до 0°С) |
| o | в) температура тіла людини |
| o | г) обробка слабкою кислотою |
58. Що обумовлює біологічну цінність білків:
| o | а) наявність незамінних амінокислот |
| o | б) наявність замінних амінокислот |
| o | в) наявність оксиамінокислот |
| o | г) наявність кетокислот |
59. Які фактори знижують біологічну цінність білків?
| o | а) наявність небілкової частини |
| o | б) наявність нуклеопротеїдів |
| o | в) наявність макроелементів |
| o | г) наявність мікроелементів |
78. Охарактеризувати фактори, що визивають зворотні зміни у білках:
| o | а) додання водовіднімаючих речовин |
| o | б) додання цукру |
| o | в) додання кислоти |
| o | г) додання ацетону |
79. Що таке "ідеальний" білок:
| o | а) білок, що міститься у жіночому молоці, яєчному білку, гіпотетичний білок |
| o | б) білок, що міститься у печінці та нирках |
| o | в) білок, що міститься у м'ясі та рибі |
| o | г) білок овочів та фруктів |
83. Які основні функції виконують білки в організмі:
| o | а) пластична |
| o | б)захисна |
| o | в)транспортна |
| o | г) усі перелічені |
84. Як впливає технологічна обробка продуктів на здатність білків підлягати дії травних ферментів
| o | а) підвищує її |
| o | б) знижує |
| o | в)не впливає |
| o | г) потребує додаткових умов для перетравлення |
87. Яка з структур білка тіла людини є найбільш поширена:
| o | а) третинна структура |
| o | б) вторинна структура |
| o | в) первинна структура |
| o | г) четвертинна, третинна |
88. До чого призводить нестача повноцінних білків у раціоні людини
| o | а) зменшується зріст |
| o | б) слабшає імунітет |
| o | в) погіршується розвиток психічної діяльності |
| o | г) усі перелічені наслідки |
89. Полярні незаряджені амінокислоти:
| o | а) Асп, Глу |
| o | б) Ліз, Арг, Гіс |
| o | в) Вал, Лей, Ізолей, Мет, Фен, Три, Про, Ала |
| o | г) Глі, Сер, Тре, Цис, Глу, Тир, Асп |
90. Формула лізину:

91. У чому полягає відмінність гемоглобіну від міоглобіну:
| o | а) у складі білку глобіну |
| o | б) у складі гемів |
| o | в) у кількості гемів у кожній молекулі хромопротеїду |
| o | г) у тій функції, що вони виконуютьта кількості гемів у кожній молекулі хромопротеїду |
92. Які функції виконують білки у організмі:
| o | а) пластичну та регуляторну |
| o | б) енергетичну та каталітичну |
| o | в) захисну |
| o | г) усі перелічені функції |
93. Полярні незаряджені амінокислоти:
| o | а) Ліз, Арг, Гіс |
| o | б) Асп, Глу |
| o | в) Вал, Лей, Ізолей, Мет, Фен, Три, Про, Ала |
| o | г) Глі, Сер, Тре, Цис, Асп, Глу, Тир |
94. Дати визначення сполуки – білки:
| o | а) це високомолекулярні органічні сполуки, що містять амінокислоти |
| o | б) органічні сполуки, що містять прості білки |
| o | в) органічні сполуки, що крім білків містять небілкові речовини |
| o | г) Усі перелічені компоненти |
95. Чому рослинні білки гірше підлягають дії травних ферментів?
| o | а) тому, що клітковина погіршує їх проникнення до клітин |
| o | б)тому, що у рослинах багато води |
| o | в) тому, що у рослинах є водорозчинні вітаміни |
| o | г) тому, що до складу деяких рослин входять полісахариди |
96. Білок якого харчового продукту вважаються „ідеальним”?
| o | а) зерна бобових |
| o | б) риби |
| o | в) курячого яйця |
| o | г) молока синього кита |
РОЗДІЛ 3. ХІМІЯ НУКЛЕЇНОВИХ КИСЛОТ
Загальна характеристика
Нуклеїнові кислоти були відкриті в 1868 році швейцарським хіміком Ф. Мішером. Учений виділив ці речовини з ядер кліток і назвав їх нуклеїном (від лат. nucleus - ядро). Однак більш докладне вивчення цих сполук було проведено лише наприкінці 40-х років нашого сторіччя. Великий внесок у розшифровку складу і ролі нуклеїнових кислот внесли хіміки П. Левін, Е. Чаргафф, Дж. Уотсон, Ф. Лемент, Б. В. Кедровський, А. М. Бєлозерський, А. С. Спірін і інші.
Нуклеїнові кислоти - це клас полімерів, відповідальних за збереження і передачу генетичної інформації, а також її реалізацію в процесах синтезу клітинних білків. Вони універсальні компоненти всіх живих організмів. Нуклеїнові кислоти являють собою речовини білого кольору, у вільному стані погано розчинні у воді.
Ці сполуки мають високу молекулярну масу (мільйони Да), містять близько 15 % нітрогену і 10 % фосфору, відрізняються різко вираженими кислотними властивостями (за рахунок фосфорної кислоти) і при фізіологічному значенні рН несуть високий негативний заряд, унаслідок чого рухливі в електричному полі.
Хімічний склад і будова
Молекула нуклеїнової кислоти являє собою полінуклеотид, що складається з великого числа мононуклеотидів. Мононуклеотиди можуть по-різному розташовуватися в молекулі полінуклеотида, що обумовлює різноманіття нуклеїнових кислот у природі.
Кожен мононуклеотид складається з азотистої основи (пуринової або піримідинової), вуглеводу - пентози (рібози або дезоксирібози) і фосфорної кислоти. Мононуклеотиди позначають за назвою азотистої основи, що входить до їхнього складу: цитидинмонофосфат (ЦМФ) або цитидинмонофосфорна кислота; урідинмонофосфат (УМФ) або урідинмонофосфорна кислота; аденозінмонофосфат (АМФ) або аденозінмонофосфорна кислота; гуанозінмонофосфат (ГМФ) або гуанозінмонофосфорна кислота.
Найбільше значення з азотистих основ мають дві пуринових основи (похідні пурину) - аденін (6-амінопурин) і гуанін (2-аміно-6-гідроксипурин) і три піримідинових (похідні піримідину) - тимін (5-метилурацил), цитозин (2-гідрокси-6-амінопіиримідин) і урацил (2,6-гідроксипіримідин), що у складі нуклеїнових кислот представлені в кетоформі. До складу нуклеїнових кислот входять вуглеводи: рибоза, дезоксірибоза.
В молекулі дезоксірибонуклеїнової кислоти, крім цих вуглеводів, міститься глюкоза.
Пуринові або піримідинові основи, рибоза і дезоксирибоза і фосфорна кислота зв'язані в молекулах нуклеотидів однаково. Пентози приєднуються до нітрогену основ через глікозидні зв'язки у пуринових основ у дев'ятому положенні, у піримідинових - у третьому.
При гідролізі мононуклеотидів утворюється два види продуктів: сполуки азотистої основи з пентозою і вільна фосфорна кислота або азотиста основа і пентозофосфорний ефір. При цьому вуглевод знаходиться посередині молекули мононуклеотиду, будучи сполучною ланкою між азотистою основою і фосфорною кислотою.
Сполуки азотистої основи (наприклад, аденіну) з пентозою називають нуклеозидом. Нуклеозиди являють собою двокомпонентні речовини, приєднуючи фосфорну кислоту вони перетворюються в мононуклеотиди - трикомпонентні сполуки. Фосфорна кислота приєднується до нуклеозидів за рахунок складноефірних зв'язків зі спиртовим гідроксилом пентози.
За складом вхідних у нуклеїнові кислоти вуглеводів розрізняють дезоксирибонуклеїнову (ДНК) і рибонуклеїнову (РНК) кислоти.
Дезоксирибонуклеїнова кислота. ДНК локалізується в основному в ядрах кліток (у хромосомах) і лише незначна кількість її виявлена в мітохондріях і хлоропластах. Молекулярна маса складає (0,5 – 20) × 106 Да й вище. Основна функція ДНК полягає в тому, що вона є носієм-хоронителем генетичної інформації. У ній закодовані всі спадкоємні властивості організму, у першу чергу всі структури білків і, отже, особливості обміну речовин. Це обумовлено визначеною послідовністю розташування азотистих основ у структурі ДНК.
До складу ДНК входять азотисті основи: аденін (А), гуанін (Г), тимін (Т) і цитозин (Ц), вуглевод - дезоксирибоза і фосфорна кислота. Первинна структура молекули являє собою унікальну послідовність з'єднаних між собою мононуклеотидів за типом 3,5,-зв'язку. У нуклеотидах виявлені фосфодиефирні зв'язки, що утворюються між ОН-групою в положенні 5' дезоксирибози одного нуклеотида і ОН-групою в положенні 3' пентози іншого (рис. 3.1.).
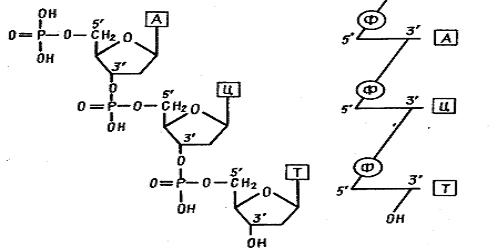
Рис. 3.1. Фрагмент первинної структури ДНК
При цьому азотисті основи певним чином з'єднуються між собою за принципом компліментарності (доповнення): пуринові основи доповнюють піримідинові. Наприклад, аденін завжди з'єднується тільки з тиміном, а гуанін - з цитозином.
Молекулярний вміст у ДНК пуринів дорівнює вмістові піримідинів, тобто вміст аденіну дорівнює вмістові тиміну (А = Т або А/Т =1), вміст гуаніну дорівнює вмістові цитозину (Г = Ц або Г/Ц = 1), сумарний вміст аденіну і гуаніну дорівнює сумарному вмістові цитозину і тиміну (А + Г) = (Ц + Т) або (А + Г): (Ц + Т) = 1.
Крім того, встановлено, що кількість аміногруп, що входять до складу ДНК пуринових основ (аденіну і гуаніну), дорівнює кількості аміногруп (6), що входять до складу піримідинових основ (цитозину і тиміну) (рис. 3.2.). Між аденіном і тиміном утворюються два водневі зв'язки, а між гуаніном і цитозином - три.
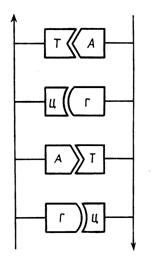
Рис. 3.2. Компліментарність основ у ДНК
Усі ці дані дозволили американським хімікам Дж. Уотсону і Ф. Лементу створити модель вторинної структури ДНК, що являє собою двотяжну антипаралельну спіраль. Схематично це можна показати у виді кручених сходів (рис.3.3).
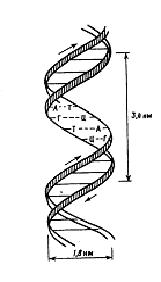
Рис. 3.3. Схематичне зображення подвійної спіралі ДНК
Крім первинної і вторинної структур, розрізняють також і третинну структуру нуклеїнових кислот, зв'язану з просторовим розташуванням ДНК.
Рибонуклеїнова кислота. Будова РНК за характером зв'язків між окремими нуклеотидами ланцюга така ж, як і в молекулі ДНК. Залишок пентози одного нуклеотиду в РНК з'єднується складноефірним зв'язком із залишком фосфорної кислоти іншого мононуклеотиду.
Більшість типів РНК, на відміну від ДНК, являє собою однотяжну спіраль. Нитка РНК закручується сама по собі в спіраль, утворює водневі зв'язки між азотистими основами аденін-урацил-гуанін-цитозин. РНК зосереджена в основному в цитоплазмі, але нерідко зустрічається і у ядрі. Особливо багаті на РНК ядерце і рибосомальна фракція мікросом.
РНК виконує дещо інші функції, ніж ДНК. Вона "зчитує" інформацію з ДНК про порядок чергування азотистих основ і несе її в цитоплазму. РНК відповідальна за специфічність синтезованих молекул.
У клітинах існує три головних різновиди РНК: матрична - інформаційна (М-РНК), рибосомальна (Р-РНК) і транспортна (Т-РНК).
Матрична (М-РНК) синтезується в ядрі і присутня як у ядрі, так і в цитоплазмі. Вона складає 4-10 % РНК клітини. Молекулярна маса М-РНК коливається від 3 × 105 до 2 × 106 Да. Цей вид РНК містить чотири азотистих основи: аденін, гуанін, цитозин і урацил. М-РНК відіграє роль сполучної ланки між ядерною ДНК і рибосомами, вона передає генетичну інформацію від ДНК на поліпептидний ланцюг білка, що синтезується. Ферментативним шляхом відбувається "переписування" інформації з хромосомної ДНК. Після одержання інформації М-РНК переходить на рибосоми і стає матрицею для синтезу білка. Синтез кожного білка в клітині забезпечується специфічною М-РНК.
Рибосомальна (Р-РНК) у клітині тісно зв'язана з білками рибосом, утворює рибонуклеопротеїни. Вона складає 75-80 % усієї РНК клітки. Молекулярна маса Р-РНК - від 5 ´ 105 до 1,2 ´ 106 Да.
Транспортна (Т-РНК) знаходиться головним чином у цитоплазмі, де вона складає 10-15 % РНК клітини. Молекулярна маса Т-РНК - від 1,8 ´ 104 до 3,5 ´ 104 Да. Поряд з аденіном, гуаніном, урацилом і цитозином Т-РНК містить визначену кількість так званих мінорних основ. Функція Т-РНК полягає в доставці до рибосом визначених амінокислот. Кожна амінокислота має свою особливу Т-РНК.
Основні характеристики нуклеїнових кислот представлені в таблиці 3.1.
Таблиця 3.1.
Основні характеристики нуклеїнових кислот
| Вид нуклеїно-вих кислот | Основне місце локалізації | Функція | Молекул яр-на маса, Да | Складові компоненти | Форма | |
| вуглевод | азотиста основа | |||||
| ДНК | Ядро | Носій спадкової інформації | Мільйони | Дезокси- рибоза | Аденін (А) Гуанін (Г) Цитозин (Ц) Тимин (Т) | Подвійна спіраль |
| І-РНК (інформа- ційна) | Ядро і цитоплазма | Передача інформації з ДНК | Варіює | Рибоза | А, Г, Ц, У | Лінійна |
| Р-РНК (рибосо- мальна) | Цитоплазма | Місце переда- чи інформації з І-РНК | Високопо- лімери (105–106) | Рибоза | А, Г, Ц, У | Містить сферичні частки |
| Т-РНК (транс- портна) | Цитоплазма | Транспорт амінокислот до місця синтезу білку | Рибоза | А, Г, Ц, У | Спірале- видна |
КОНТРОЛЬНІ ПИТАННЯ І ЗАВДАННЯ:
1. Що таке нуклеопротеїни, який їхній склад і біологічне значення?
2. Яке будівля ДНК? Розповісти про її значення.
3. Назвіть особливості будівлі і функції різних видів РНК.
4. Напишіть формули пуринових і пиримідинових основ.
5. Напишіть мононуклеотиди ДНК, з'єднаєте них між собою.
6. Напишіть пари азотистих основ - Аденін-Тимін, гуанін-цитозин, з'єднайте водневими зв'язками.
Тести для контролю знань і самопідготовки
1. Хто відкрив і виділив перші НК?
| o | а) Ф. Мішер |
| o | б) Ф. Мішер, Н. Лобавін |
| o | в) О. Данилевський, Е. Фішер |
| o | г) А. Бєлозерський. |
2. Із яких речовин побудовані мононуклеотиди?
Не нашли, что искали? Воспользуйтесь поиском: