
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Загальна характеристика 7 страница
Механізм активації ферментів іонами металів полягає в тому, що в одних випадках вони входять до складу простетичної групи ферментів і полегшують утворення фермент-субстратного комплексу, а в інших - сприяють приєднанню коферменту до апоферменту або забезпечують утворення четвертинної структури ферменту.
Прості хімічні сполуки діють як алостеричні активатори. Приєднуючись до алостеричного центра ферменту, вони змінюють третинну структуру білкової молекули. У результаті цього активний і субстратзв’язуючий центри ферменту здобувають найбільш вигідну для взаємодії із субстратом конфігурацію.
Деякі ферменти виробляються в неактивній формі у виді проферментів, або ензимогенів (попередників). Їхній активний центр замаскований додатковою ділянкою поліпептидного ланцюга, тому субстрат не може з ним з'єднатися. Видалення такої додаткової ділянки приводить до вивільнення активного центру і можливості утворення фермент-субстратного комплексу. Так, профермент пепсину - пепсиноген активується соляною кислотою з відщіпленням невеликого пептидного ланцюга. У результаті утворюється активний протеолітичний фермент - пепсин.
Інгібітори гальмують дію ферментів. Розрізняють два види інгібування: незворотне й зворотне. Незворотне інгібування зв'язано з дією таких речовин, що порушують усю структуру ферменту, у тому числі активного центру (наприклад, дія сильних кислот і основ, солей важких металів).
Зворотне інгібування відбувається в період безпосередньої взаємодії ферменту з інгібітором, видалення якого знову повертає ферментові активність. Таке інгібування може протікати за конкурентним і неконкурентним типом.
Конкурентне гальмування можливе в тому випадку, коли інгібітор містить хімічні групи, подібні із субстратом, тобто є його структурним аналогом і здатний взаємодіяти з активним центром ферменту. В основі цього виду гальмування лежить конкуренція між субстратом і інгібітором за приєднання до активної групи ензиму. Такий інгібітор, зв'язуючись з ферментом, утворює інгібітор-ферментний комплекс. Однак це відбувається лише у випадку, якщо концентрація інгібітору перевищує кількість субстрату.
При збільшенні концентрації субстрату він витісняє інгібітор з активного центра ферменту, що відновлює свою каталітичну функцію. Таким чином, дія конкурентних інгібіторів може бути ослаблена або усунута шляхом збільшення кількості субстрату.
При неконкурентному гальмуванні інгібітор взаємодіє не з активним субстратним центром ферменту, а з алостеричним. Внаслідок цього змінюється структура ферменту, у тому числі й активного центру, до якого вже не може приєднатися субстрат. У цьому випадку концентрація інгібітору не має ніякого значення. Видалення інгібітору не завжди приводить до відновлення властивостей ферменту.
Інгібітори ферментів зустрічаються в тканинах організму. У підшлунковій залозі виявлена речовина білкової природи, що гальмує активність трипсину. Відома також сполука, що гальмує активність пепсину. Ці речовини називають антиферментами, їхня дія носить зворотний характер. У визначених умовах антиферменти відщеплюються від ферментів, що веде до відновлення активності останніх.
4.4. ЗАГАЛЬНІ УЯВЛЕННЯ ПРО МЕХАНІЗМ ДІЇ ФЕРМЕНТІВ
В основі дії ферментів як біологічних каталізаторів лежить їхня здатність прискорювати реакції за рахунок зменшення енергії активації субстрату.
Механізм дії ферментів вивчений поки недостатньо. Існуючі в даний час дані дозволяють висловити тільки деякі загальні положення щодо цього питання.
Запуск реакції можна здійснити шляхом подолання сил відштовхування між молекулами, що обумовлено зовнішніми електронами. Ферменти деформують електронні оболонки субстратів, полегшуючи в такий спосіб взаємодію між ними. Енергія, необхідна для того, щоб привести молекули в активний стан, називається енергією активації. Вона використовується для подолання енергетичного бар'єра. Цей процес може здійснити каталізатор. Наприклад, енергія активації, необхідна для розкладання пероксиду водню 2Н2О2 → 2Н2O + О2, без каталізатора складає 75,2 кДж/моль, із застосуванням каталізатора - колоїдної платини - 50,2 кДж/моль, за участю ферменту каталази печінки - 8,3 кДж/моль. Таким чином, роль звичайного каталізатора (і в ще більшому ступені біологічного) полягає в тому, що він знижує енергію активації субстрату.
Існують дві теорії механізму дії ферментів: теорія проміжних сполук і адсорбційна.
Теорія проміжних сполук. Суть процесу - в утворенні фермент-субстратного комплексу (мал. 4.2.). При безпосередній взаємодії субстрату з активним центром ферменту останній певним чином впливає на субстрат, викликаючи перебудову його хімічних зв'язків і тим самим активізуючи його.


Рис. 4.2. Схема утворення фермент-субстратного комплексу
Як приклад, можна привести механізм дії фумарази (F), яка каталізує реакцію утворення яблучної кислоти з фумарової кислоти:
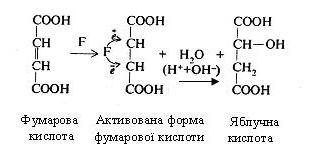
Подвійний зв'язок, що є у фумаровій кислоті, представлений електронними парами. При взаємодії фумарової кислоти з фумаразою відбувається утворення фермент-субстратного комплексу, у результаті чого функціональні групи активного центру ферменту сприяють перерозподілові електронів подвійного зв'язку. Внаслідок цього один з вуглецевих атомів здобуває електрон і заряджається негативно, а інший, віддаючи електрон, - позитивно. Таким чином, молекула фумарової кислоти стає активованою і легко може приєднувати іони Н+ і ОН- (іони води) за типом електростатичного зв'язку і перетворитися в яблучну кислоту.
У фермент-субстратному комплексі одночасно відбуваються два процеси: зміна його електронної густини, що викликає поляризацію зв'язків, а також геометрична деформація (напруга) окремих зв'язків як у молекулі субстрату, так і в активному центрі ферменту. Ці процеси сприяють подоланню активаційного бар'єра перехідного стану фермент-субстратного комплексу. На першій фазі ферментативного каталізу між субстратом і ферментом виникає сполука, у якій реагенти зв'язані один з одним ковалентним або іонним зв'язком. В другій фазі субстрат під впливом приєднаного до нього ферменту змінюється і стає більш доступним для відповідної хімічної реакції. На третій фазі відбувається сама хімічна реакція і, нарешті, продукти реакції, що утворилися, на четвертій фазі вивільняються з фермент-субстратного комплексу.
Якщо позначити фермент буквою F, субстрат - S, активований субстрат - S1 і продукт реакції - Р, то зазначену послідовність процесу можна виразити схемою:

Фермент зв'язується із субстратом в оборотній реакції з утворенням фермент-субстратного комплексу. У процесі утворення останнього і на подальших стадіях ферментативного каталізу відбуваються кількаразові зміни третинної структури ферменту, що приводять до послідовного зближення із субстратом і орієнтації в просторі тих активних груп, що взаємодіють одна з одною на різних етапах перетворення субстратів. Зміна третинної структури білка можлива тільки при участі всього (або майже всього) поліпептидного ланцюга, що утворює молекулу білка. Отже, у каталітичному процесі бере участь уся молекула ферменту при упорядкованій взаємодії його центрів, що забезпечує послідовне здійснення багатостадійних процесів ферментативного каталізу. Спрямованість реакцій залежить від зміни енергії при реакції, від різниці вільних енергій вихідних речовин і речовин, що утворюються.
Існує ще одна особливість дії ферментів: в організмі перетворення речовин до кінцевих продуктів відбувається в кілька етапів, кожний з яких каталізується окремим ферментом. Наприклад, синтез жирних кислот забезпечується групою ферментів, до складу якої входить сім ферментів.
Сума енергії активації проміжних реакцій нижче енергії активації, необхідної для одночасного розщеплення субстрату.
Адсорбційна теорія. Відповідно до цієї теорії, речовини, що реагують, адсорбуються на поверхні ферменту, що сприяє збільшенню їхньої концентрації, зближенню реакційноздатних груп. Речовини, що знаходяться на поверхні ферменту (адсорбенту), можуть утримуватися за рахунок простої фізичної адсорбції, обумовленої силами міжмолекулярної взаємодії і більш міцного хімічного зв'язку. Каталізатор своїм силовим полем викликає визначені зміни в структурі реагуючих речовин, що приводить до підвищення реакційної здатності субстрату і збільшенню швидкості реакції.
Кожен фермент містить певні хімічні угруповання, завдяки яким він вступає в з'єднання із субстратом і здійснює свою каталітичну дію.
Такими групами є SH-групи, залишки гістидину, серину, тирозину і т.д. Ці групи розташовані в молекулі ферменту на різних ділянках, але взаємодіють між собою і є відповідальними за каталітичну діяльність ферменту. Ці групи одержали назву функціональних груп ферментів.
У молекулі ферменту є комбінація різних хімічних угруповань, що утворюють активний центр у молекулі ферменту, завдяки якому здійснюється його каталітична дія.
Якщо в субстраті є заряджені групи, утворення FS-комплексу відбувається завдяки електростатичній взаємодії іонних зв'язків між позитивно зарядженими групами ферменту, і навпаки.
Якщо субстрат не має заряджених груп, то приєднання ферменту до субстрату відбувається внаслідок утворення водневих зв'язків або гідрофобної взаємодії.
Кофактори, виконуючи каталітичну функцію, залишаються хімічно незмінними в результаті каталітичної реакції.
4.5. РЕГУЛЯЦІЯ ФЕРМЕНТАТИВНИХ РЕАКЦІЙ
Склад і активність ферментів залежать від характеру їжі. І. П. Павлов і його учні установили, що при годівлі собак м'ясом ферментативна активність і кислотність їхнього шлункового соку значно вище, ніж при годівлі молоком.
Тривале і надлишкове вигодовування голодуючій тварині деяких амінокислот, наприклад триптофану, викликало заміну в молекулі ферменту альдолази одних амінокислот іншими, що спричинило за собою зміни структури і функції ферментів.
Активність ферментів обумовлена різними факторами. Так, наприклад, дефіцит вітамінів приводить до порушення синтезу коферментів, внаслідок чого порушуються відповідні біохімічні процеси.
Приведені дані свідчать про пристосувальну здатність організму до визначеного характеру харчування шляхом зміни складу травних соків.
Ензими, що постійно присутні в організмі, називаються конституційними. За певних умов в організмі утворюються нові ферменти. Вони одержали назву адаптивних. Так, вигодовування тваринам тирозину підсилює синтез ферменту тирозинамінотрансферази. При підвищеному вмісті білків у харчовому раціоні зростає активність ферменту ентерокінази, який каталізує розщеплення пептидів, а також перетворення трипсиногену в трипсин. Трипсин у свою чергу активує трансформацію хімотрипсиногену в хімотрипсин; у такий спосіб виникає ланцюгова каталітична реакція. У цьому процесі ентерокіназа відіграє роль пускового механізму адаптації ферментів, що розщеплюють білки.
Зменшення кількості білка в харчуванні спочатку приводить до зниження активності ентерокинази, а потім до гальмування дії трипсину і хімотрипсину.
Адаптивні ферменти називаються ще і індуцибільними (від лат. іnductіo - введення), а речовини, що сприяють появі індуцибільних ферментів - індукторами. Іноді індуктор викликає появу не одного, а декількох ферментів, що зв'язано з утворенням різних проміжних сполук, що теж можуть відігравати роль індукторів.
Підвищення активності ферментів під впливом визначених індукторів підсилює біосинтез нових ферментів або змінює активність існуючих, а при дії на організм шкідливих факторів (наприклад, іонізуючі випромінювання) може відбутися якісна зміна каталітичних властивостей ферментів.
Найважливіший вид регуляції активності ферментів у клітинах - інтенсивність їхнього синтезу, що залежить від діяльності генетичного апарата.
Біохімічним і фізіологічним механізмами регуляції активності ферментів є зміна їхньої активності, головним чином, через алостеричні центри. Цей процес відбувається під впливом на ферменти специфічних речовин, функція яких полягає в координації обмінних реакцій у клітинах і їхній адаптації до мінливих умов внутрішнього і зовнішнього середовища. До таких речовин відносяться гормони, що синтезуються в залозах внутрішньої секреції, і тканинні гормони (гістогормони), що утворюються в клітинах і не мають спеціалізованої гормональної функції. Так, у мозковому шарі надниркових залоз синтезується гормон адреналін, що через ланцюг біохімічних реакцій активує фермент, який каталізує розщеплення глікогену в печінці і м'язах.
Інтенсивність утворення тих або інших гормонів регулюється нервовою системою. Таким чином, в організмі здійснюється східчастий контроль за дією ферментів, що безпосередньо запускають біохімічні процеси.
Один з видів забезпечення надійності хімічних реакцій у клітках полягає в утворенні ізоферментів (ізоензимів), що каталізують однакові реакції, але відрізняються за чутливістю до активаторів і інгібіторів.
Ізоферменти мають неоднакову будову, що й обумовлює розходження їхніх властивостей. Отже, якщо в клітинах змінюються умови, то ізоферменти можуть "підстраховувати" здійснення важливих біохімічних процесів. Співвідношення різних ізоензимів може характеризувати наявність порушень обміну в клітинах, його широко використовують в медичній практиці для діагностики.
Як вже було відзначено раніше, у клітинах функціонують цілі мультиферментні системи. У таких системах кінцевий продукт послідовних ферментативних перетворень гальмує перший фермент (шляхом зв'язування з його алостеричним центром), у результаті чого швидкість усього ферментативного процесу визначається постійною концентрацією кінцевого продукту. Перший фермент такої мультиферментної системи одержав назву регуляторного, або алостеричного ферменту, а інгібуючий - ефектору, або модулятора. На регуляторний фермент може впливати як негативний модулятор, що викликає його інгібування, так і позитивний, що збільшує активність ферменту.
Таким чином, регуляторний вплив на активність ферментів роблять субстрат, продукти розщеплення, ізоформи, ферменти, що потребують активаторів. Координація процесів обміну, які каталізуються ферментами, здійснюється гормонами й іншими регуляторними факторами, утворення й активність яких контролюються нервовою системою.
4.6. НОМЕНКЛАТУРА Й КЛАСИФІКАЦІЯ ФЕРМЕНТІВ
Діюча нині номенклатура і класифікація ферментів були затверджені в 1961 році на V Міжнародному біохімічному конгресі в Москві.
В основу номенклатури були покладені наступні принципи:
а) закінчення -аза варто використовувати тільки для простих ферментів; для мультиферментних комплексів рекомендований термін система (наприклад, піруватдегідрогеназна система);
б) у найменуванні повинний бути відбитий механізм реакції, назва субстрату і коферменту, тип реакції, яка каталізується.
З урахуванням цих правил замість колишньої назви, наприклад, "лактатдегідрогеназа" рекомендують систематичну назву лактат-НАД-оксидоредуктаза, що містить три позиції: субстратом є лактат (молочна кислота), коферментом - НАД (нікотинамідаденіндинуклеотид), фермент оксидоредуктаза каталізує перенос водню від субстрату до акцептора, тобто зазначений тип реакції.
Усі ферменти підрозділяються на шість класів: оксидоредуктази, трансферази, гідролази, ліази, ізомерази, лігази (синтетази). Кожен клас має підкласи.
Оксидоредуктази. До цього класу віднесені усі ферменти (дегідрогенази, оксидази й ін.), які каталізують окиснювально-відновні реакції. Ці реакції здійснюються ланцюгом ферментів і проміжних переносників водню або електронів від первинного субстрату до кінцевого акцептора - кисню. Особливістю оксидоредуктаз є їхня здатність прискорювати велике число найрізноманітніших окиснювально-відновних реакцій, що забезпечує з'єднання коферменту з багатьма апоферментами. При цьому щоразу утворюється оксидоредуктаза, специфічна стосовно того або іншого субстрату. Оксидоредуктази беруть участь у хімічних реакціях, зв'язаних з вивільненням енергії.
Трансферази. Ферменти цього класу здійснюють внутрі- і міжмолекулярний перенос окремих функціональних груп. У залежності від характеру угруповань, що переносяться, розрізняють метилтрансферази - переносять метильні групи - СН3, амінотрансферази - здійснюють перенос амінних груп - NH2, фосфотрансферази - транспортують залишок фосфорної кислоти.
Гідролази. Ферменти цього класу забезпечують розщеплення внутрімолекулярних зв'язків органічних сполук при участі води. До цього класу відноситься велика група ферментів, у тому числі майже всі ензими шлунково-кишкового тракту: естерази, фосфатази, пептидази й ін.
Ліази. До цього класу відносяться ферменти, які каталізують зворотні реакції відщіплення різних груп від субстратів негідролітичним шляхом. Розщеплення йде за зв'язком С-С, С-N, С-О і т.д. До таких ферментів відносяться, наприклад, декарбоксилази, які відщеплюють СО2 від карбонових кислот.
Ізомерази. Ці ферменти каталізують різні типи реакцій ізомеризації. Вони також каталізують процеси внутрімолекулярних перетворень: перенос водню, фосфатних і ацильних груп, зміну просторового розташування атомних угруповань, переміщенні подвійних зв'язків і т.д. Наприклад, L-ізомери перетворюються в D-ізомери, глюкоза - у фруктозу і т.д.
Лігази або синтетази. Ферменти цього класу беруть участь у всіх реакціях синтезу різних сполук. Вони прискорюють реакції утворення органічних сполук. Одним з таких природних донаторів енергії є аденозинтрифосфат (АТФ). Енергія, що виділяється при відщіпленні залишків фосфорної кислоти, використовується для процесів біосинтезу.
4.7. ВИКОРИСТАННЯ ФЕРМЕНТІВ В ХАРЧОВІЙ ПРОМИСЛОВОСТІ
У харчовій промисловості ферменти використовуються для одержання продуктів із заданими властивостями. При цьому можуть використовуватися мікробні ферменти; ферменти, виділені з деяких органів, наприклад, з печінки, підшлункової залози, шлунка. Більш зручним і ефективним є використання іммобілізованих ферментів.
Іммобілізовані ферменти. Іммобілізація ферментів - це включення об'єкта (ферменту) в ізольовану фазу, що відділена від фази вільного розчину, але здатна обмінюватися з нею молекулами.
Іммобілізовані ферменти одержують шляхом зв'язування з носіями розчинних ферментів або кліток, що володіють ферментативною активністю, тобто роблять сорбцію ферменту на носії і включення в структуру носіїв-гелів.
Іммобілізація наближає умови їхнього функціонування до природного.
Перевага їхнього використання полягає в тому, що їх можна видаляти з реакційного середовища, тобто контролювати хід реакції і багаторазово його використовувати. Використання іммобілізованих ферментів дозволяє проводити кожен процес безупинно, пропускаючи розчини субстратів через реактори з іммобілізованими ферментами.
Іммобілізовані ферменти мають високу каталітичну активність, її можна змінювати, змінюючи спосіб зв'язування і вид носія. Продукти реакції не забруднюються кристалічними ферментами.
За допомогою іммобілізованих ферментів одержують амінокислоти, ароматичні кислоти, цукри, органічні розчинники, антибіотики, їх використовують для очищення стічних вод і водоймів.
У промисловості застосовують ферменти мікробного походження: протеолітичні, ліполітичні, амілолітичні, гідролази, що розщеплюють пектин, целюлозу і геміцелюлозу.
Характеристика оксидоредуктаз і використання ферментів у виробництві харчової продукції
Глюкозооксидаза є аеробною дегідрогеназою. Молекула ферменту у якості коферменту містить дві молекули ФАД (флавінаденіндинуклеотид). Вона каталізує відщіплення Н2 від субстрату і перенос його на О2 повітря з утворенням перекису водню. Субстратом є глюкоза, що перетворюється в глюконову кислоту, а перекис водню, що утворився, розщеплюється каталазою на воду і атомарний оксиген. Глюкозооксидаза синтезується цвілевими грибами.
Цей фермент широко використовується в харчовій промисловості, а також у клінічній хімії для аналізів. Глюкозооксидаза дозволяє видаляти оксиген і глюкозу з субстратів. Вона використовується для видалення кисню з тих харчових речовин, фарбування і аромат яких погіршуються в результаті окисних процесів (пиво, фруктові соки, продукти, що містять жири).
Цей фермент використовують також у тих випадках, коли продукти піддають висушуванню, у ході якого відбувається взаємодія глюкози з білками з утворенням темнопофарбованих продуктів (реакція Майяра). Це має місце при одержанні яєчного і молочного порошку.
У харчовій промисловості глюкозооксидаза як ендогенний фермент цвілевих грибів знаходить застосування при ферментації глюконової кислоти для одержання D-глюконата кальцію.
Ксантиоксидаза каталізує окиснювання різних за хімічною природою субстратів, наприклад, ксантину і формальдегідів. Ця реакція має низьку специфічність. Як акцептор електронів виступає кисень повітря. Донором електронів є формальдегід. Як індикатор використовується метиленовий синій. Ця реакція використовується в молочній промисловості для тестування сирого і пастеризованого молока. У результаті достатньої пастеризації відбувається денатурація ксантиноксидази і знебарвлення метиленового синього не відбувається.
Дифенолоксидаза бере участь в окиснюванні тирозину, фенолу, крезолу. Кінцевими продуктами є темнозабарвлені сполуки - меланіни. Фермент виявлений у грибах, картоплі, фруктах. Функціональною групою фенолоксидази є Сu. Важливе значення мають інгібітори цього ферменту, тому що ферментативне побуріння фруктів, соків і інших рослинних матеріалів при їхній переробці є великою проблемою.
Процес потемніння фруктів, соків, продуктів їхньої переробки під впливом дифенолоксидази може бути уповільнений вітаміном С, двоокисом сірки, сульфітом натрію, додаванням повареної солі. Зменшують активність цього ферменту попередня теплова обробка овочів і фруктів, зокрема, бланшування. У ряді випадків дія дифенолоксидази призводить до появи бажаного фарбування, аромату харчових продуктів, наприклад, при ферментації чаю.
Аскорбатоксидаза діє на аскорбінову кислоту, тобто окисляє її в дегідроаскорбінову кислоту. Цей фермент виявлений у багатьох вищих рослинах. Він містить мідь як функціональну групу, що змінює свою валентність у ході каталізу.
Через її дію відбувається руйнування вітаміну С при технологічній обробці. Інгібіторами цього ферменту є деякі амінокислоти (гліцин, цистеїн, аспарагінова і глутамінова кислоти), карбонові й оксикарбонові кислоти (щавлева, лимонна, винна), пектини, флавоноїди і дубильні речовини, кверцитин, антоціани, катехіни. Аскорбатоксидаза при технологічній обробці продуктів не тільки зменшує вміст аскорбінової кислоти, а і впливає на фарбування й аромат соків.
Каталаза - оксидоредуктаза - дегідрує молекулу перекису водню з утворенням води й атомарного оксигену. Як функціональну групу містить ферринпротопорферин ІХ. Молекула ферменту містить чотири гемінові групи, кожна з яких зв'язана з білком. Каталаза інгібується речовинами, що утворюють комплекси з центральним атомом заліза, наприклад, ціанідом, сульфідом, фторидом, CO, NO, ціанамідом і ін. Виявлена у всіх клітинах з аеробним типом обміну речовин. У харчовій промисловості використовують її препарати з печінки і цвілевих грибів у тих випадках, коли спочатку проводиться обробка перекисом водню, а потім він повинен бути вилучений. Наприклад, при пастеризації і стерилізації молока, при відбілюванні волосся, шкір, дезінфекції хірургічного матеріалу.
Пероксидаза сприяє розщепленню перекисів. У її складі, у залежності від джерела, міститься або червоний, або зелений гемін. Пероксидаза з хрону відносно стійка при нагріванні. Прогрівання ферменту при 850С на протязі 30 хвилин приводить до втрати лише половини активності. Її активність гальмують солі важких металів. Використовується для оцінки якості процесу пастеризації. Її достатність визначається за активністю цього ферменту. При ферментації чаю і тютюну цей фермент сприяє утворенню забарвлених і ароматичних компонентів.
Ліпоксигеназа каталізує реакцію: ненасичена жирна кислота + О2 ® перекис ненасиченої жирної кислоти. Характеризується високою специфічністю і діє лише на ненасичені жирні кислоти, що знаходяться в цис-формі. Лінолева, ліноленова і арахідонова кислоти окисляються з однаковою швидкістю. Міститься в пшениці, насінні олійних культур, бобових, люцерні, соєвому борошні. При переробці харчових продуктів використовують інгібітори ліпоксигенази, що взаємодіють з вільними радикалами, що утворюються як проміжні продукти при дії цього ферменту на ненасичені жирні кислоти. Цей фермент руйнує каротин, ароматичні сполуки продуктів. Він сприяє прогірканню жирів. При використанні ліпоксигенази в хлібопечінні поліпшується колір м'якушки і збільшується обсяг хліба.
Ліпаза відноситься до гідролаз. Вона каталізує розщеплення ефірів гліцеролу і вищих жирних кислот. Причому швидкість розщеплення залежить від довжини ланцюга жирних кислот. Джерелом для одержання промислових препаратів ліпази є підшлункова залоза, цвілеві гриби, молоко. Активаторами ліпази є солі жовчних кислот, особливо таурохолат. У молоці ліпаза сприяє утворенню ароматичних речовин, а ліпаза пшениці і інших злаків сприяє псуванню борошна. Мікробні препарати ліпази використовуються для гідролізу жирів у тих випадках, коли необхідне омилення при збереженні біологічно активних жиророзчинних речовин (наприклад, токоферолу).
Пектинестераза каталізує розщеплення пектину з утворенням метанолу і пектата. Фермент активується іонами Na+ і Ca2+. Пектинестераза володіє високою субстратною специфічністю, гідролізуючи майже винятково метильні групи пектинових сполук. Вона є важливим складеним компонентом ферментних препаратів, що використовуються для освітлення фруктових і виноградних соків, а також для одержання низькомолекулярних пектинів, використовуваних при виготовленні желе. Цей фермент разом з іншими ферментами відіграє важливу роль при дозріванні фруктів і ягід, сушінню льна, коноплі, ферментації чаю і тютюну.
Глікозидази каталізують розщеплення олігосахаридів і глікозидів. Вони каталізують гідроліз і трансглікозидування, що відіграє важливу роль при синтезі полісахаридів у рослинах. Їх одержують у промислових умовах із пророслого ячменя. Глікозидази поділяють на кілька типів. Специфічність цих типів визначається розміром кільця гелікона, конфігурацією ОН- груп у кільці і конфігурацією глікозидного гідроксилу. До них відносяться: a-Д- глікозидаза, b-Д- глікозидаза, a-Д-галактозидаза та ін. a-Д- глікозидаза не має промислового значення. b-Д- глікозидаза сприяє видаленню гіркоти із соків цитрусових, а також сприяє звільненню з b-глікозидів ароматичних компонентів.
Гліканази відрізняються від глікозидаз більшою довжиною ланцюга субстратів, на які вони діють. На основі субстратної специфічності розрізняють наступні важливі гліканази: a-амілаза (субстрат - крохмаль, декстрини); b-амілаза (субстрат - крохмаль, декстрини); глюкоамілаза (субстрат - крохмаль, декстрини, мальтоза); інулаза (субстрат - інулін); полігалактуроназа (субстрат - пектин, полігалактуронова кислота).
a -амілаза розщеплює зв'язок -1,4 в полісахаридах, що містять три і більш залишків глюкози. Міститься в слині, соку підшлункової залози, у пророслих зернах, у цвілевих грибах і бактеріях. Для прояву максимальної активності ферменту необхідна присутність кофактора Са2+. Цей фермент сприяє швидкому зменшенню в'язкості крохмального клейстеру, тому його називають декстриногенною амілазою. Використовується при виготовленні крохмальної патоки, сусла і затору.
b -амілаза каталізує розщеплення крохмалю з утворенням мальтози і декстринів. Оскільки під дією b-амілази відбувається звільнення мальтози з амілази й амілопектину, її називають цукровою амілазою. Міститься у вищих рослинах. Джерелами ферменту є ячмінь, жито, пшениця, соєві боби. Використовується у виробництві сусла і затору, крохмальної патоки і як хлібопекарський поліпшувач. Крім того, із крохмалю за допомогою амілаз готують сиропи, що застосовуютьсяі при виготовленні кондитерських виробів і лікерів.
Глюкоамілаза єдина з всіх амілаз швидко гідролізує крохмаль до глюкози, причому вона гідролізує і a-1,4 і a-1,6 зв'язки. Джерелами цього ферменту є цвілеві гриби. Використовується в спиртовому виробництві.
Застосовуються амілази у пивоварній промисловості. Під дією амілаз перетворюється крохмаль головним чином у мальтозу, якщо як джерело амілази використовується ячмінний солод. При використанні для оцукрювання крохмалю ферментів цвілевих грибів крохмаль розщеплюється до глюкози. Характерне розходження між пивоварним і спиртовим виробництвом полягає в тому, що в пивоварстві солод служить одночасно субстратом і джерелом ферменту, оскільки містить як крохмаль, так і амілази.
Не нашли, что искали? Воспользуйтесь поиском: