
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Рівні структурної організації білкових молекул
Первинна структура білків – це конфігурація поліпептидного ланцюга, яка формується в результаті утворення кислотоамідного (пептидного) зв’язку між залишками амінокислот. При синтезі пептиду α-карбоксильна група однієї амінокислоти взаємодіє з α-аміногрупою другої амінокислоти, утворюючи пептидний зв’язок із виділенням молекули води:

 |
Пептидний зв’язок, що утворюється іміногрупою проліну, відрізняється від інших пептидних зв’язків – у атома азоту пептидної групи відсутній водень, замість нього є зв’язок із радикалом, як наслідок, один бік циклу включається в пептидний каркас:
 |
При взаємодії двох амінокислот утворюється дипептид, трьох – трипептид і так далі аж до утворення величезного поліпептиду. Умовно прийнято, що пептиди, які містять від 2 до 20 амінокислотних залишків, належать до олігопептидів; ті, що мають від 20 до 50 амінокислотних залишків, – до поліпептидів. Пептидні ланцюги, які об’єднують понад 50 амінокислот і мають молекулярну масу, більшу за 6000, належать до білків.
Амінокислотні залишки у пептидних ланцюгах різних білків чергуються не випадковим чином, а розташовані в певному порядку. Назви пептидів складаються з назв амінокислот, які входять до їх складу. Амінокислотний залишок, який має вільну α-аміногрупу, називається N-кінцевим, а той, що має вільну α-карбоксильну групу – С-кінцевим. Пептиди записують і читають із N-кінця до С-кінця. Наприклад, у тетрапептиді тир-ліз-глу-про N-кінцевою амінокислотою є тирозин, а С-кінцевою – пролін. Наведемо реакцію утворення цього тетрапептиду:
 | ||
 |
Оскільки до складу пептидів α-амінокислоти входять у формі ацилів, то в назві пептидів вони набувають характерного для ацилів закінчення -іл(-ил) замість ін(-ин), тобто «тирозил» замість «тирозин», «лізил» замість «лізин», «глутаміл» замість «глутамінової кислоти» і т.ін. Найменування пептидів складається з назви першої N-кінцевої амінокислоти із закінченням -іл(-ил), наступних амінокислот із таким самим закінченням і повної назви амінокислоти, яка має вільну α-карбоксильну групу (С-кінцева амінокислота). Отже, наведений вище тетрапептид має назву тирозил-лізил-глутаміл-пролін. У структурних формулах пептидів амінокислоту з кінцевою α-аміногрупою (N-кінцева амінокислота) пишуть ліворуч, а з кінцевою α-карбоксильною групою (С-кінцева амінокислота) – праворуч.
Первинна структура кожного індивідуального білка закодована в молекулі ДНК і реалізується в ході транскрипції (передача закодованої в ДНК інформації молекулам мРНК) та трансляції (синтезу білка).
Пептидні зв’язки дуже міцні, для їхнього хімічного неферментативного гідролізу використовують жорсткі умови: гідроліз білка проводять у концентрованій сірчаній кислоті при температурі близько 110 °С упродовж 24 годин. У живій клітині пептидні зв’язки можуть розриватися за допомогою протеолітичних ферментів, що мають назву протеази або пептидгідролази.
Із виявлених особливостей у будові пептидного зв’язку Л. Полінгом і Р. Корі були сформульовані три постулати (принципи формування пептидного зв’язку):
1) атоми, що утворюють пептидний зв’язок, є копланарними (розміщені в одній площині); обертання атомів або груп атомів навколо пептидного зв’язку неможливе;
2) принцип еквівалентності внеску амінокислотних залишків в утворення пептидного зв’язку і тим самим в утворення поліпептидного ланцюга (виняток – пролін);
3) принцип максимуму водневих зв’язків. У білках атоми водню та кисню практично завжди розміщуються у транс-конформації. Це зумовлює можливість утворення в поліпептидному ланцюгу максимуму водневих зв’язків.
Первинну структуру білка стабілізують (підтримують):
- пептидні зв’язки (між амінокислотними залишками);
- дисульфідні зв’язки (між вільними –SH-групами цистеїну).
Первинна структура білка несе інформацію про його просторову структуру.
Вторинна структура білків – локальна конформація, зумовлена обертанням окремих ділянок поліпептидного ланцюга навколо одинарних ковалентних зв’язків.
Основні зв’язки, які стабілізують вторинну структуру, – водневі зв’язки між атомами пептидних груп амінокислот у складі одного й того самого пептидного ланцюга або між різними пептидними ланцюгами.
Види вторинної структури:
· α-спіраль (правозакручена)
В α-спіралі водневі зв’язки утворюються між атомом кисню карбонільної групи і воднем амідного азоту 4-ї від нього амінокислоти. Водневі зв’язки розташовані паралельно осі спіралі і повторюються багато разів, тому міцно утримують спіралеподібну структуру у дещо напруженому стані (як стиснуту пружину). Бічні радикали амінокислотних залишків розміщуються по периферії спіралі й не беруть участі в утворенні вторинної структури. α-спіраль має певні характеристики: ширину, відстань між двома витками спіралі. Крок спіралі (один повний виток) 5,4Å (0,54 нм) становлять 3,6 амінокислотних залишків на виток, а на один амінокислотний залишок припадає 0,15 нм. Кут підіймання спіралі 26°, через 5 витків спіралі (18 амінокислотних залишків) структурна конфігурація поліпептидного ланцюга повторюється. Це означає, що період повторюваності (або ідентичності) α-спіральної структури становить 2,7 нм.
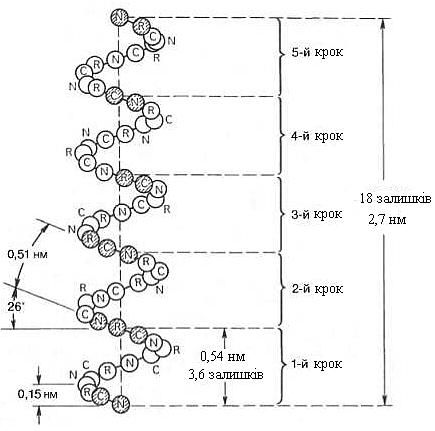 |
Рисунок 2 – Структура та параметри α-спіралі
Білок не може мати в ланцюгу 100 % α-спіралей і зберігати глобулярність. Він у цьому випадку буде фібрилярним. Більш того, якщо є α-спіраль, вона знаходиться, як правило, в одній, двох або декількох окремих ділянках ланцюга.
Порушення спіральної структури може бути спричинене багатьма факторами. Наприклад, наявністю залишку проліну, циклічна структура якого вносить перегин у пептидний ланцюг; наявністю локального електростатичного відштовхування, зумовленого кластером позитивно заряджених R-груп лізину й аргініну, або кластером негативно заряджених R-груп глутамінової й аспарагінової кислот та іншими причинами. Неспіральна частина пептидного ланцюга може мати структуру складчастого листа або статистичного клубка.
· β-структура формується між лінійними ділянками пептидного каркасу одного поліпептидного ланцюга, утворюючи при цьому складчасті структури. Стабілізується β-структура водневими зв’язками між С=О та NH-групами. Поліпептидні ланцюги або їхні частини можуть формувати паралельні або антипаралельні β-структури. У паралельному складчастому листі обидва пептидні ланцюги або дві різні ділянки одного й того самого пептидного ланцюга мають у просторі однаковий напрям (збігаються N- і С-кінці пептидних ланцюгів). В антипаралельному складчастому листі ланцюги спрямовані у протилежні боки (N- і С-кінці пептидних ланцюгів мають протилежний напрям). У деяких білків β-структури можуть формуватися за рахунок утворення водневих зв’язків між атомами пептидного каркасу різних поліпептидних ланцюгів. У природних білках і пептидах трапляються обидві структури, але антипаралельна є більш стабільною,тому і більш поширеною.
 |
Рисунок 3 – Паралельні (А) та антипаралельні (Б)
Не нашли, что искали? Воспользуйтесь поиском: